(2019.10.14~25.) 2주간 임상 57건 승인...GSK 대상포진 백신도
최근 2주간 57건의 임상시험이 승인됐다. 라니티딘으로 위장 약 시장 변동이 큰 와중에 종근당은 급·만성 위염 천연물 신약 개발에 일보 전진했다. 일동홀딩스 계열사는 PARP 저해 기전의 항암신약 개발에 도전한다. 씨제이헬스케어는 케이캡정 적응증 확대, GSK는 대상포진백신 3상시험을 새로 승인받았다.
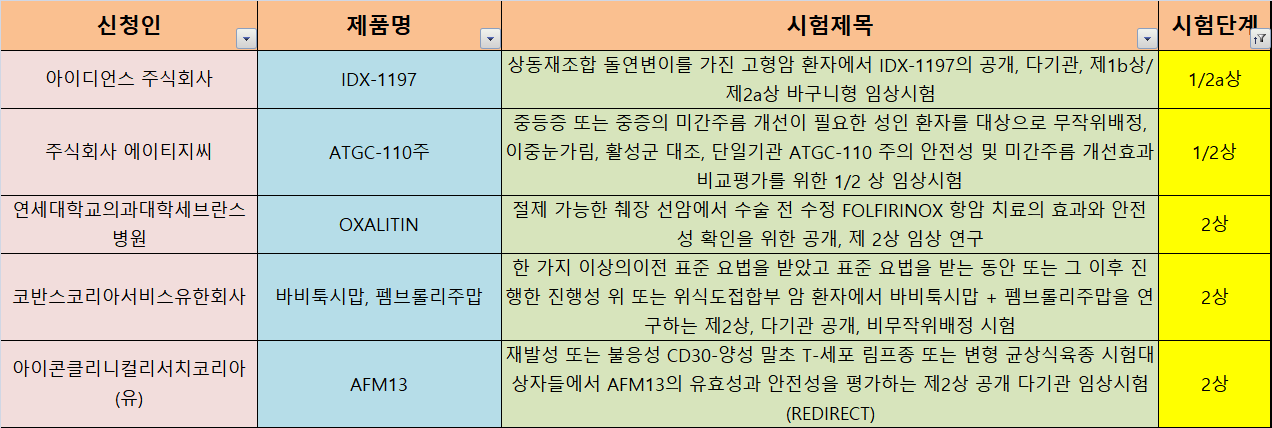
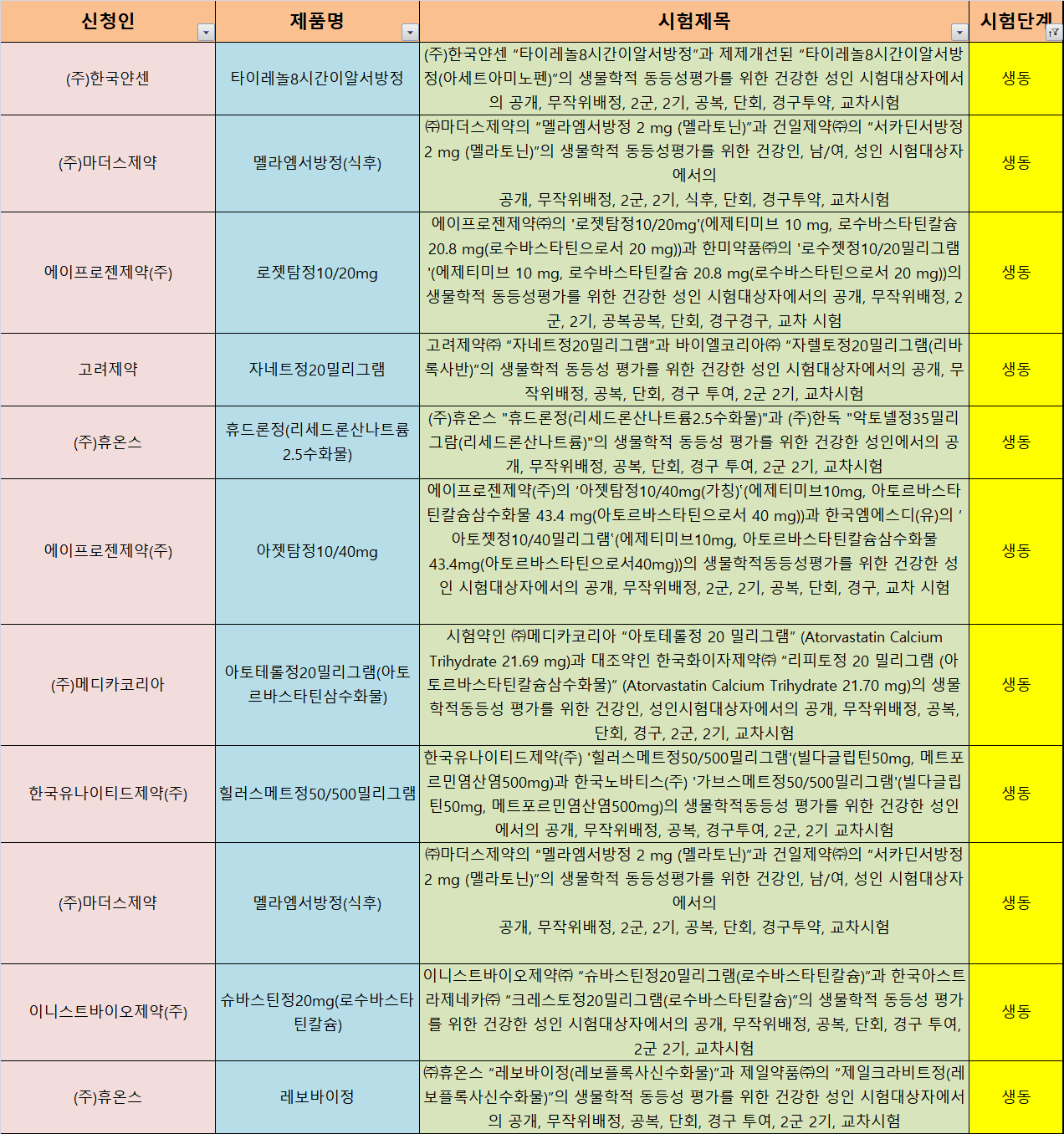
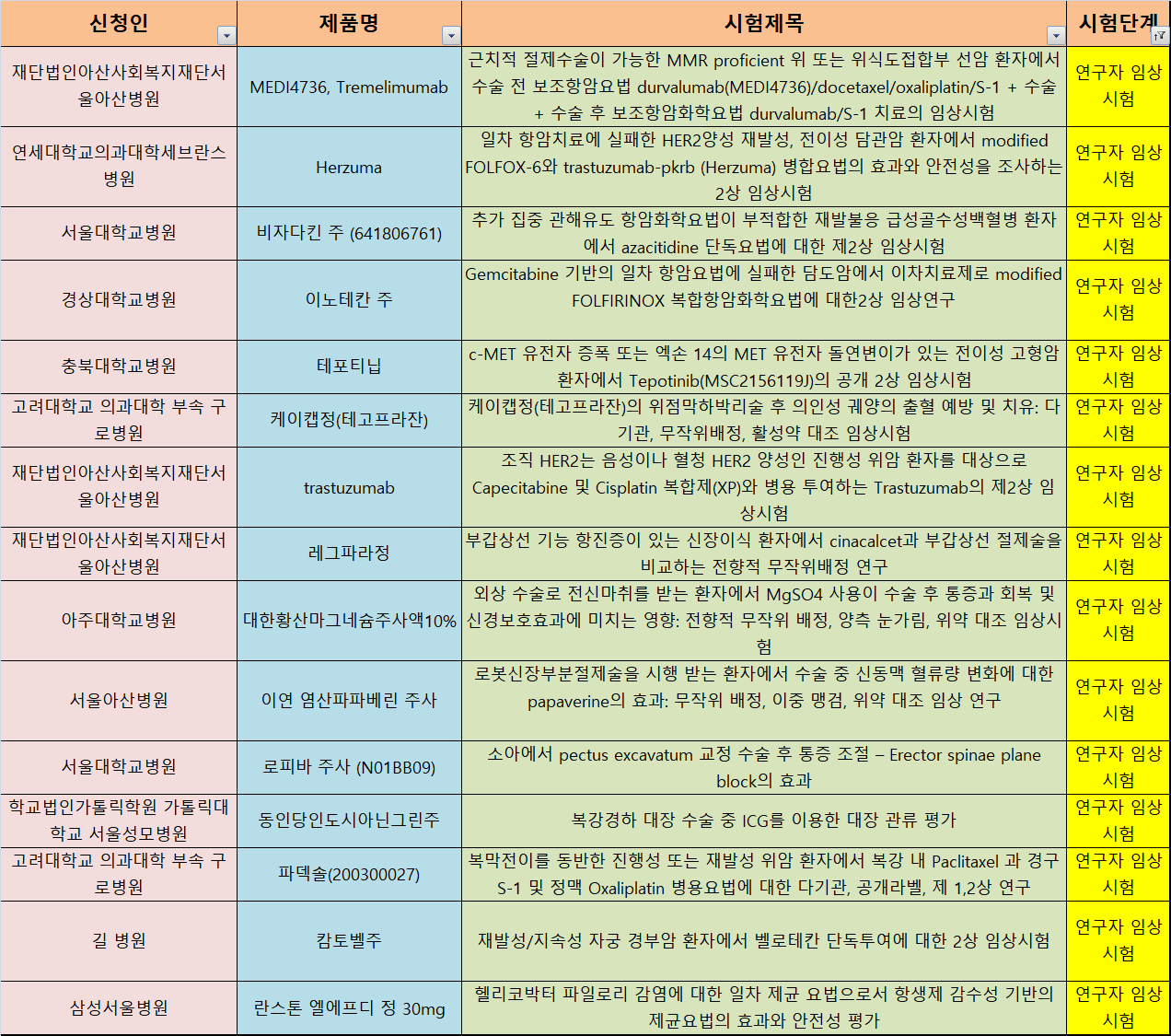
27일 식품의약품안전처 '의약품 안전나라' 임상승인현황에 따르면 지난 14일부터 25일까지 총 57건의 임상시험이 새로 승인받았다. 신청인(중복 포함)별로는 제약·바이오기업 30건, 의료기관 17건, CRO 10건 등이었다. 제약·바이오기업의 경우 국내사 21건, 다국적사 9건이었다. 시험단계별로는 ▶ 연구자 임상시험 15건 ▶ 3상 12건 ▶ 생동성 시험 11건 ▶ 1상 8건 ▶ 2상 · 3b상 각 3건 ▶ 1/2a상 2건 ▶ 1b상 · 2/3상 · 3a상 각 1건씩 있었다.
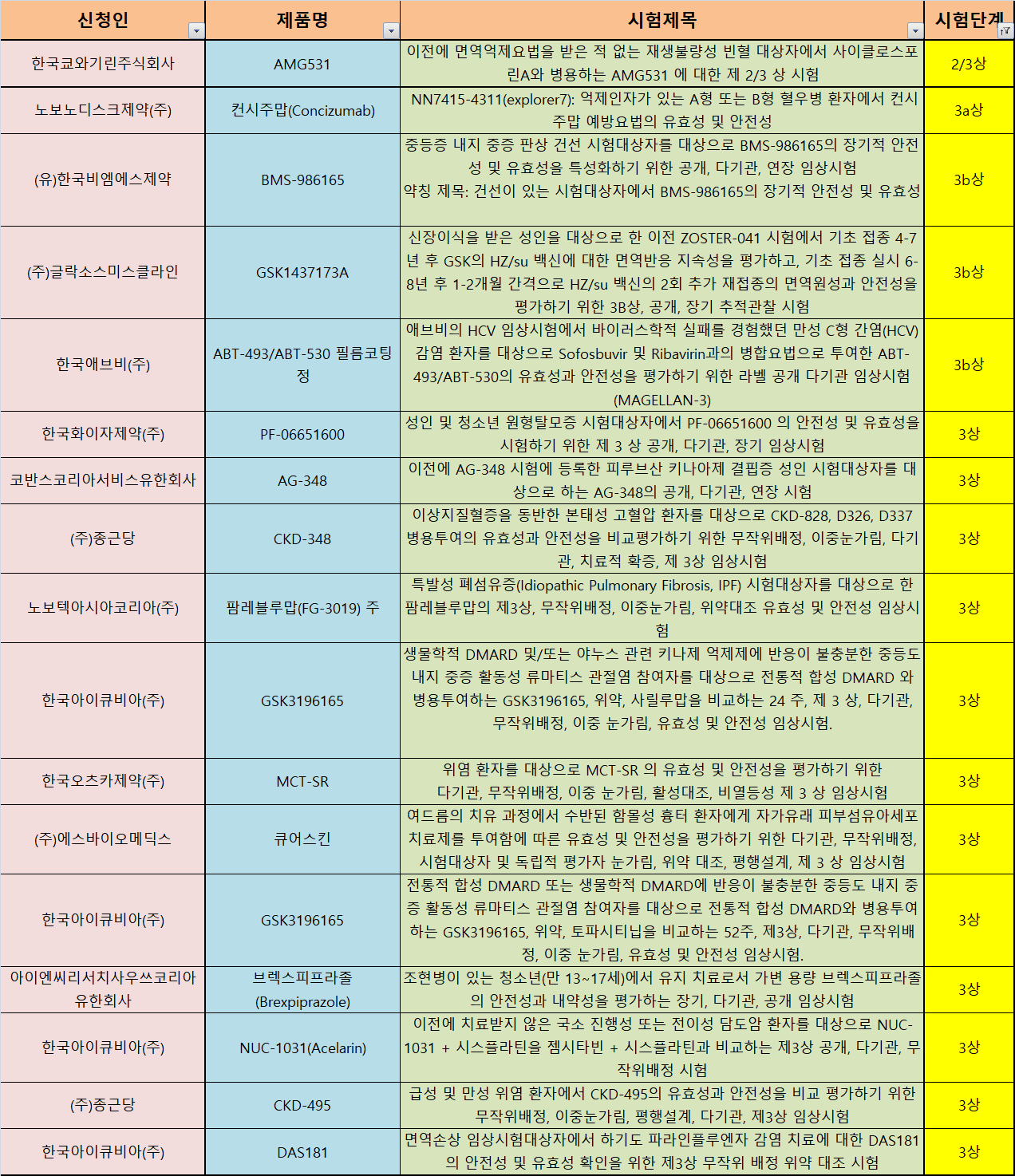
종근당은 육계 건조엑스(20~35→1) 성분의 급·만성위염 치료제이자 천연물의약품인 'CKD-495'의 임상 3상을 지난 14일 승인받았다. 급·만성 위염 환자 279명에게 유효성과 안전성을 비교 평가할 계획이다.
육계 성분이 함유된 의약품은 다수지만, 이 성분만으로 천연물의약품을 개발하는 건 종근당이 처음이다. 육계는 녹나무와 육계나무의 줄기 껍질을 말린 약재로 종근당은 2012년부터 CKD-495를 연구·개발해왔다.
쑥을 원료로 한 애엽건조엑스 제제인 동아에스티의 천연물신약 스티렌도 위염 환자에게 쓰이며 140여 억 원의 처방실적을 기록 중이다. 2012년 레일라 이후 천연물 신약은 출현하지 않고 있는데, CKD-495가 허가를 득한 후 시장 입지를 어떻게 차지할지 주목된다.
종근당은 고혈압, 이상지질혈증을 적응증으로 한 개량신약복합제도 개발 중이다. 23일 CKD-348의 3상시험을 승인받았지만, 기업 비밀 사유로 성분명은 공개하지 않은 것으로 보인다.
한국오츠카제약은 레바미피드 성분 자사 오리지널약 '무코스타' 서방정을 개발 중이다. 지난 21일 위염 환자를 대상으로 MCT-SR의 유효성과 안전성을 보기 위한 3상을 승인받았다. 그런데 올 3월부터 '레바미피드 서방형 제제 150mg'을 MCT-SR로 간주하는 임상 1상을 2건 진행 중이었다. 무코스타는 2017년 156억 원, 2018년 160억 원의 처방 실적을 거뒀다.
무코스타는 위궤양과 급·만성 위염의 급성 악화기로 미란, 출혈, 발적, 부종 위점막 병변의 개선에 쓰이는데 1일 3회 투여하거나 위궤양이면 아침, 저녁 및 취침 전 등에 투여해야 해 복용 편의성이 낮았다. 기존 용량 대비 150mg로 함량을 높이고 복용 횟수를 줄일 수 있는 '서방형 제제'가 출시되면 경쟁력이 생길 전망이다.
일동홀딩스 계열 아이디언스는 항암제 신약후보물질 'IDX-1197'에 대한 1b/2a상을 승인받았다. 기존 진행 중인 1a상에 비해 타깃 암종을 확대할 계획이다. 아이디언스는 지난 5월 설립된 NRDO(No Research, Development Only) 형태의 신약개발 전문기업이다.
'PARP(Poly ADP-ribose polymerase)'는 암세포의 DNA 단일 가닥에 손상이 생겼을 때 복구를 돕는 역할을 한다. IDX-1197은 이 PARP의 작용을 억제해 암세포가 스스로 사멸하도록 유도하는 기전을 가진다.

연구 결과, IDX-1197이 타 PARP저해제에 비해 더 다양한 종류의 암에 우월한 효과를 나타내 기존 유사 약물보다 폭넓은 활용 범위를 가진 신약으로 개발할 수 있는 가능성을 확인했다. 이번에 승인된 1b/2a 임상부터는 아이디언스의 주도로 진행될 예정이다.
씨제이헬스케어는 건강한 성인 남성 36명을 대상으로 '케이캡'(코드명 CJ-12420, 성분명 테고프라잔)을 케이캡과 아토르바스타틴 병용, RAPA114와 아토르바스타틴 병용 군과 약물상호작용을 비교 평가하는 국내 1상을 승인받았다.
지난 4월에는 케이캡과 클리피도그렐 병용, RAPA113·클리피도그렐 병용 군과 약물상호작용을 비교 평가하는 1상을 승인받았다. PPI 제제가 신체 대사효소 CYP2C19를 통해 대사될 때 클리피도그렐 등 타 약제와 병용 시 약효를 저해하는 한계점이 있었다. 케이캡 등 P-CAB 기전은 이 CYP3A4로 약물상호작용이 적은 편이다.
이번 아토르바스타틴, 클로피도그렐 등 각 임상 1상은 PPI 제제와 케이캡의 차별점을 확인하기 위한 차원에서 진행되는 것으로 관측된다.
또 씨제이는 제2형 당뇨병 치료제 개량신약 'CJ-30066'의 1상을 승인받았다. 회사 측은 기업 비밀로 인해 성분을 공개하지 않았다. 회사 관계자는 "허가받기까지 5년이 소요될 것으로 보인다"고 전했다.
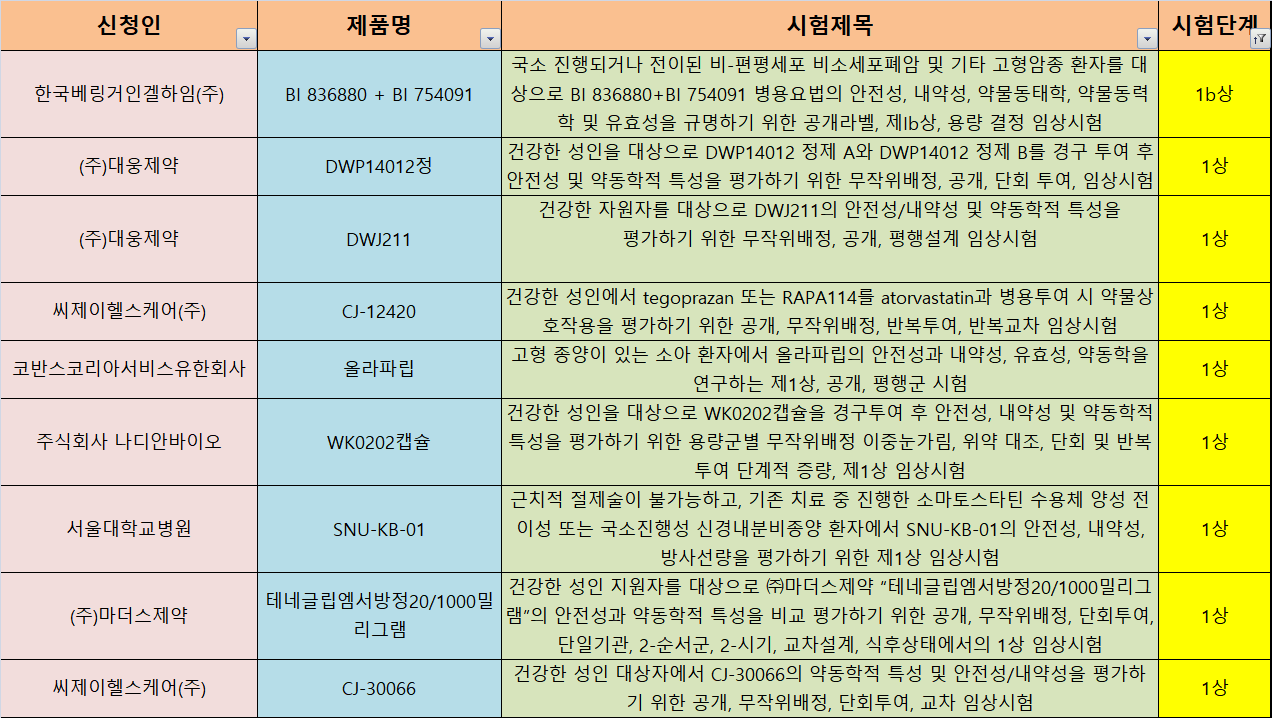
한국비엠에스제약(이하 BMS)은 선택적 티로신 키나제2(TYK2) 억제 후보물질 'BMS-986165'를 가지고 중등증 내지 중증 판상 건선 환자에 대한 임상 3b상에 착수한다. 지난 6월 동일 질환자에게 유효성과 안전성을 따지는 3상을 승인받은 바 있는데, 이번 임상은 장기적 안전성과 유효성을 특성화시키기 위한 목적으로 마련됐다.
TYK2는 면역과 염증 조절을 관리하는 JAK 효소 4가지 중 하나인데 TYK2만 선택적으로 억제한 후 건선을 치료하는 약물이다. 건선은 물론 루푸스, 크론병 등의 자가면역질환과 관련이 있는 것으로 알려졌다. BMS가 'BMS-986165'를 가지고 식약처에 승인받은 임상은 루푸스, 크론병, 판상 건선, 궤양성 대장염 등 8건에 달한다.
국내 원형탈모 환자를 대상으로 한 원형탈모 치료 신약 JAK억제제 'PF-06651600'의 임상 3상도 승인됐다. 한국화이자제약(이하 화이자)의 신약이다. 이 물질은 JAK3(야누스 인산화효소3) 경구용 선택적 저해제로 면역과 염증 조절을 관리하는 효소다. 류마티스성 관절염, 크론병 등 자가면역질환과 관련이 있는 것으로 알려져 여러 임상이 시도 중이다.
한국애브비는 전유전자형 C형간염 치료제 마비렛(성분명 글레카프레비르+피브렌타스비르)의 추가 임상 3상을 진행한다. 다국가 임상인데, 국내 C형 감염자 1명이 대상이다.
애브비의 HCV 임상시험에서 바이러스학적 실패를 경험했던 만성 C형 간염(HCV) 환자를 대상으로 Sofosbuvir(소발디정, 소포스부비르) 및 Ribavirin(바이라미드캡슐, 리바비린)과 병합요법으로 투여한 마비렛의 유효성과 안전성을 평가한다. 현재 우리나라 보험인정기준에선 소발디정과 바이라미드캡슐 병용요법은 다클린자정, 순베프라캡슐 병용요법을 사용할 수 없는 경우에 복용하도록 규정됐다.
우리나라에는 아직 시판되지 않은 GSK의 대상포진 백신 싱그릭스(Shingrix)의 임상 3상이 추가 진행될 전망이다. GSK 관계자는 싱그릭스 국내 도입에 대해 "한국은 출시 우선국으로 조기 시판허가 · 출시를 위해 박차를 가하고 있다"고 했다.
이번 임상은 코드명 GSK1437173A(대상질환 대상포진)에 대해 신장이식을 받은 성인을 대상으로 한 이전 ZOSTER-41 시험에서 기초 접종 4~7년 후 GSK의 HZ/su(대상포진) 백신에 대한 면역반응 지속성을 평가하고, 기초 접종 실시 6~8년 후 1~2개월 간격으로 Hz/su(대상포진) 백신의 2회 추가 재접종의 면역원성과 안전성을 평가한다.
EU(유럽연합)의 clinicaltrials register(임상시험 정보 등록)에 의하면 ZOSTER-41 시험은 신장 이식을 한 성인에게 GSK의 HZ/su (대상포진) 백신에 대해 면역원성과 안전성을 평가한 바 있다.
혈우병 피하주사제 임상도 진행된다. 정맥주사만 있던 혈우병 치료제에 피하주사는 환자들에게 새 치료 기회로 주어지게 된다. 노보노디스크는 항-조직인자경로(TFPI) 억제 기전의 '컨시주맙' 3상을 승인받았다.
억제인자가 있는 A 또는 B형 혈우병 환자를 대상으로 컨시주맙 예방요법의 유효성과 안전성을 평가한다. 컨시주맙은 항체 유무 관계없이 한 달에 1회 투여할 수 있는 특징을 갖고 있다.
관련기사
- 종근당, 급·만성 위염 치료제 'CKD-495' 3상 돌입
- NASH 등 치료제 없는 질환 신약 임상 박차
- 2주간 임상승인 40건 육박...일동, 치매 신약 3상
- 종근당 대장암·제일 P-CAB 계열 신약개발 임상 박차
- 케이캡·슈가논, 적응증 확보 임상 박차
- 한미-단장증후군 신약·대웅-도네페질 패치 임상착수
- 일동 '아이디언스', 항암신약 'IDX-1197' 1b/2a상 승인
- 인공지능과 NRDO...장수기업의 '신박한 R&D'
- 일동 아이디언스, 항암신약 파이프라인 'IDX-1197' 확보
- 일동홀딩스, 신약개발회사 아이디언스 설립
- 다케다 P-CAB '보신티' 허가...케이캡과 대결?
- 한국 제약사들도 면역항암제 개발 열기 '후끈'
- 새 조합 고혈압 3제 복합제...펜 타입 엔브렐 시밀러 주목
- 삼성바이오에피스, 솔리리스 시밀러 개발임상 착수
- 나보타를 남성형 탈모치료제로?...연구자 임상 주목
- C형간염약 마비렛, 8주 치료 길 열려
- 휴미라 장착 애브비, 7년간 처방약 500% 성장
- C형간염, 범유전자형 약물 최적?…"상호작용 등 고려해야"
- 마비렛, C형간염치료제 시장서 급부상
- C형간염 치료제 마비렛, “범유전자형 환자 대상 8주 완치 확인”
- 범유전자형(1~6형) 만성 C형간염 8주 치료...'마비렛'
- GC녹십자 대상포진백신 ‘CRV-101’, 1상 중간결과 공개
- 대상포진 백신 조스타박스, 신경통 유효성 67%
- 의약품 생산실적 살펴보니…녹십자·대웅 성장률↑
- 듀피젠트, RSA 이중 트랙...헴리브라 안건 상정안돼
- 혈우병치료 새 지평 열 헴리브라의 '장대높이뛰기'
- 편두통신약 '라스미디탄' 임상 속도…나녹셀엠주도
- 한림, 자가면역 신약 '류마티스' 넘어 '간 이식' 반응 확인
- '케이캡' 네 번째 적응증은 '헬리코박터 제균', 치료영역 확대
- 적응증 확대 케이캡…PPI 막강 방어선 돌파할까?
- 일동 "우리 미래 먹거리는 R&D… 과제 진행에 박차"
- 케이캡 독주 'P-CAB', 후발자는 적응증 확보 · 출시 예고
- 라니티딘 떠나고 레바미피드 서방·파모티딘 복합정 '등장'

