복용편의성 개선, 실적증대 기대… 위궤양제 시장 판세는
희귀암 '상피성 육종' 치료 타즈베릭, 여포성 림프증 임상
한 눈에 보는 임상 승인·품목 허가 - 12월 3주차 (12.14~18.)
불순물 'NDMA' 함유로 판매 금지된 라니티딘 제제의 공백을 메꾸려는 품목허가가 줄잇고 있다. 레바미피드 성분의 서방제와 파모티딘을 주성분으로 한 복합제 일반약인데 새 옵션으로 자리매김하겠다는 판단이다. 복용편의성을 개선한 게 특징이다.

올 초 미국 식품의약국(FDA)로부터 신속 승인을 받았지만 국내 품목허가는 받지 못한 상피양 육종, 여포성 림프종 신약 '타즈베릭(성분명 타제메토스타트)'의 임상이 신규 승인됐다. 푸르설티아민 성분 비타민B1 제제가 패혈증 보조치료제로 효과있을 지 탐색하는 연구자 임상도 추진된다.
레바미피드 시장에 '서방정' 내밀 유한양행… 3개사 동행
'파모티딘' 복합 일반 약 인트로바이오, 판매 어디에 맡길까
지난 한 주 34품목이 신규 허가받았다. 분류별로 전문 약 18품목, 일반 약 16품목이다. 신약은 없었고 자료제출의약품이 5품목 허가받았다. 각각 함량을 증감해 개량신약으로 인정된 4품목, 동일투여경로인데 새로운 제형이 인정된 1품목이다.
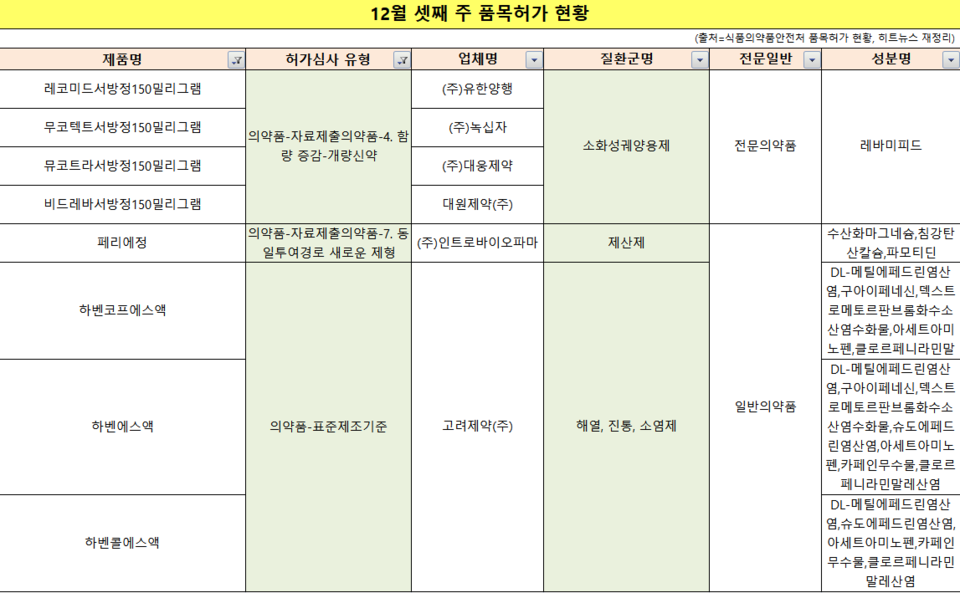
유한양행·녹십자·대웅제약·대원제약이 항궤양제 '레바미피드' 서방정을 지난 17일 동시허가받았다. 이 제제는 1991년 허가된 한국오츠카제약 '무코스타정'이 오리지널이다.
무코스타는 ▲위궤양 ▲급성위염, 만성위염의 급성악화기 개선에 쓰이고 1회 100mg을 1일 3회 경구투여한다. 위궤양은 아침, 저녁 및 취침 전에 복용해야 한다.
서방정 제품들은 복용횟수를 개선했다. 성인은 1일 2회, 아침과 저녁에 1정씩 복용하면 된다. 3회 복용을 2회로 줄인 셈으로 유한양행 자회사 '애드파마'가 개발했다. 애드파마는 개발을 맡았고 허가부터 생산은 유한양행이 한다. 공동개발에 투자한 녹십자와 대웅제약, 대원제약 등이 유한양행과 위수탁 계약을 맺었다.
레바미피드는 항궤양제 시장에서 처방 실적이 오르고 있다. 라니티딘과 용도가 흡사하기 때문으로 올 3분기 누적 832억원의 처방액을 기록, 전년동기대비 24.6% 올랐다. 이중 무코스타가 131억원으로 시장의 16%를 차지한다.
파모티딘 성분의 복합제 일반약도 첫 허가받았다. 동일성분의 츄어블정이 있지만 목넘길 수 있는 '정제'로 만들었다. 인트로바이오파마의 '페리에정'으로 위산과다 및 속쓰림과 가슴앓이 경감에 쓸 수 있다. 위산작용을 억제하는 파모티딘, 수산화마그네슘, 침강탄산칼슘 성분이 복합됐다.
품목 허가현황에 따르면 지난해 10월 이후 '파모티딘' 성분으로 새로 77품목이 허가받았다. 일반의약품도 27품목 허가받았다. 아울러 인트로바이오파마는 2007년 설립된 의약품 제형 기술개발 특화 제약사다. 자사를 '개발 및 생산 주력사'로 소개하는 대신 영업·마케팅 조직이 없어, 국내 상위사에 판매를 맡길 수 있다.
레바미피드 서방제와 파모티딘 복합 일반의약품이 동일 제제는 물론, 위궤양제 시장 판세에 영향을 줄 지 지켜봐야 한다.

40년 업력을 가진 고려제약은 감기약 브랜드 '하벤' 라인업 확대에 나섰다. 지난 16일부터 ▲하벤콜에스액 ▲하벤에스액 ▲하벤코프에스액 등 감기 증상 완화할 액제를 연달아 허가받았다.
고려제약은 '하벤'을 캅셀, 시럽, 정제 등을 갖춰 주력 제품으로 판매해왔다. 연질캡슐 8품목 뿐 아니라 나잘스프레이와 액제 등 보완에 나섰다.
희귀종양 치료제 '타즈베릭' 국내 도입 염두에 두었나
천연물 기반 골관절염 소염 진통제 '보자닉스' 임상 개시
한 주간 승인된 임상시험은 13건이다. 목적에 따라 ▲신약 허가용 5건 ▲제네릭 허가 4건 ▲복합제 개발 2건 ▲자료제출 약 허가 1건 ▲연구용 임상 1건이다.
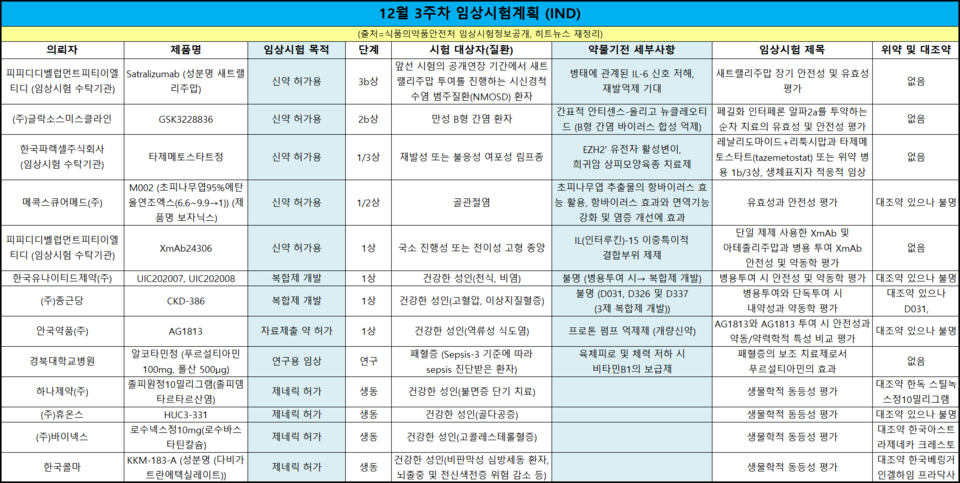
미국의 항암·유전자치료제 제약사 에피자임이 개발 중인 상피양 육종 치료제 '타즈베릭(성분명 타제메토스타트)'이 국내 여포성 림프종 환자를 대상으로 한 임상시험을 승인받았다. 임상 수탁기관인 한국파렉셀이 주관, 국내 25명의 환자가 참여한다.

상피양 육종은 젊은 성인에 발생하는 '희귀유형의 연부조직 종양'으로, 사지부위 피하 연조직에서 발생하는 것으로 알려졌다. 암세포 성장을 돕는 EZH2 메틸전이효소 활성을 차단해 암세포 성장을 억제한다.
올 1월 상피양 육종 치료제로 미 FDA(식품의약국) 가속승인 된 이후, 6월 성인 재발성 또는 불응성 여포성 림프종 환자 치료제로도 가능케됐다.
육종 관련 치료제 반응률이 높지 않았으나, 타제메토스타트는 육종 환자에 객관적 반응률 11~15%를 이끈 바 있어 미충족 수요를 채워줄 것으로 현지에서 기대를 모았다.여포성 림프종 환자들을 위한 2차 약제로 적응증을 넓히겠다는 계획이다.
국내 바이오벤처가 천연물 기반 골관절염 소염 진통제의 임상 1·2상을 승인받고, 동시 진행한다. 메디콕스 자회사 메콕스큐어메드가 자체 개발 중인 '보자닉스'다. 임상 1상은 건강한 성인 대상으로 내약성을, 2상은 비스테로이드성소염진통제(NASIDs)와 효능을 비교하는 방식으로 한다.
회사는 첫 환자 등록을 내년 1분기부터 개시, 오는 2022년 임상 3상 시험 신청을 목표로 하고 있다. 보자닉스는 초피나무엽 추출물 성분으로 항 바이러스 효과와 함께 면역기능 강화와 염증 개선에 효과가 있는 것으로 전해진다. 회사 측은 보자닉스가 항체의약품 '악템라'와 작용기전이 유사하다고 주장했다.

육체가 피로하거나 체력이 떨어질 때 활성비타민군 '비타민B1'을 보급해주는 푸르설틴아민 제제를 패혈증 보조 치료제로 탐색해보려는 연구자 임상도 눈에 띈다. 이인규 경북대학교병원 교수는 패혈증 보조 치료제로서 동화약품의 알코타민정(성분명 푸르설티아민)의 효과를 알아보려는 임상을 승인받았다.
알코타민은 푸르설티아민 100mg, 폴산 500μg이 함유됐으며 일반의약품이지만 처방 용도로 쓰인다. 이 임상은 연구자 주도 임상으로, 환자 174명 대상으로 진행한다. 이 교수는 지난 2018년에도 푸르설티아민이 제 2형 당뇨병 환자의 관상동맥 석회화에 끼치는 영향을 연구하는 임상을 승인받고 진행한 바 있다.

