테빔브라주, PD-1에 결합하는 단클론항체
백금 기반 화학요법 치료 실패, 재발, 진행 식도편평세포암 환자 대상

식품의약품안전처(처장 오유경)는 베이진코리아의 식도편평세포암 치료신약 '테빔브라주100밀리그램(성분 티슬렐리주맙)'를 허가했다고 20일 밝혔다.
테빔브라주는 면역관문 수용체로 알려진 세포예정사(PD-1)에 결합하는 단클론항체(mAb, IgG4)로, '이전에 진행하던 백금 기반 화학요법 치료를 지속할 수 없거나, 투여 이후에 재발 또는 진행된 절제 불가능, 재발성, 국소진행성 또는 전이성 식도편평세포암 성인 환자'를 대상으로 허가됐다.
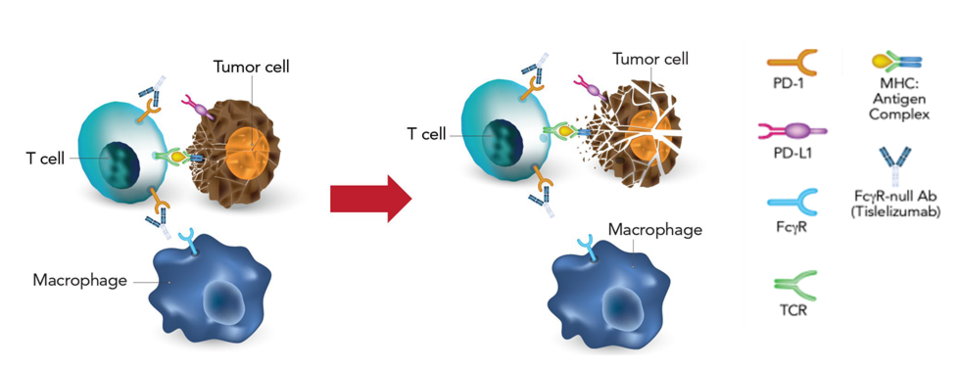
식약처 관계자는 "PD-1은 CD28 계열에 속하는 억제성 면역관문 수용체로, 면역조절에서 중추적인 역할을 수행해 면역항암제의 주 타깃으로 작용해 왔다"며 "암세포는 면역세포의 공격을 회피하기 위해 PD-L1을 표면에 발현시켜 면역세포(T세포)의 PD-1과 결합하는데, 테빔브라주는 PD-1과 PD-L1의 결합을 방해해 면역세포가 암세포를 제거할 수 있도록 돕는다"고 설명했다.
관련기사
- 베이진코리아, 박계현·정재홍 전무 영입... 모양 갖추기 한창
- 베이진은 왜, 82년생 대표를 뽑았을까 본인에게 물었더니
- 노바티스 손잡은 中 베이진의 꿈, R&D 인프라 갖춘 빅파마
- [허가/임상]부광, 조현병 신약 '라투다' 허가…베링거, 비만약 3상승인
- 테빔브라, 식도편평세포암 2차 치료제로 FDA 허가
- 2010년 생 R&D 전문 제약사 베이진, '바이오코리아 공습'
- "후보물질 10개 임상진입...한국은 모든 임상단계서 중요한 파트너"
- Interview with Beigene: Partnering with Korea for Innovative Cancer Treatment
- "테빔브라, 복막 전이 위암ㆍⅢB기 폐암 치료 개선 기대"
황재선 기자
jshwang@hitnews.co.kr
바이오헬스케어 산업의 본질을 탐구하여 독자의 눈높이에 맞춰 전달하겠습니다.

