용어 혼선으로 '1+3법안 초점' 가려져...정책 혼선의 첫 출발
공동생동은 민원서비스 용어, 위탁생동 용어로 통일해야
대한민국 제네릭의약품 정책은 미로에 갇혔다. 어떤 이는 품질 문제를 거론하고, 다른 어떤이는 절대적 품목수를 지목하며, 또다른 어떤이는 위탁제조(CMO) 등 관련 법과 부조화를 지적한다. 히트뉴스는 '발사르탄'을 핵심어 삼아 미래 정책 수립과 시행에 걸림돌이 되는 '불순물' 먼저 걷어내 보려한다. 안개가 걷히면 시야가 선명해 질 수 있다는 믿음으로.
① 제네릭 의약품 정책과 산업 실제 파악의 가림막
법적 정의가 없는 '위탁생동' '공동생동' '공동임상'이란 용어의 사용이 혼란스럽다. 용어의 혼재, 혼용은 제네릭의약품 정책과 산업의 실제를 바로보지 못하게 막는 가림막으로 작동하고 있는 현실이다.
식약처가 공동생동과 위탁생동을 합쳐 사용하는 '위탁(공동)생동'의 용어도 혼란에 일조한다.
생동품목의 위탁제조에 대해서는 '위탁생동'이라고도 하고 '공동생동'이라고도 부르며, 이를 합친 표현으로 '위탁(공동)생동'이라고도 사용하고 있다.
사실 공동생동은 위탁생동그룹 의약품들을 개별민원으로 처리하지 않고 동시에 처리해주는 식약처의 민원서비스에 가깝다.
서영석 의원이 대표발의한 소위 '1+3 약사법 개정안'은 위탁생동 수탁사의 수탁제조품목을 3개 이내로 제한하려는 내용이다. 수탁제조가 제한되므로 위탁제조가 제한되고, 직접 제조의 필요성이 커진다. 생동시험비용은 일시적이지만 직접제조를 위한 시설투자엔 막대한 비용이 든다. 제안이유에서도 알 수 있듯이 제약산업계를 뒤흔들 수 있는 큰 목표를 가지고 있다.
서영석 의원은 이번 약사법 개정안의 제안이유를 생동자료의 공유를 무제한으로 허용한 결과로 생동자료공유 의약품의 과도한 난립, 리베이트 등의 불법 유통 및 제약기업의 연구개발 능력 약화 등이 우려되는 상황이므로 생동자료 작성자가 생동자료를 공유할 수 있는 횟수를 3회로 제한해 위탁제조에 따른 유통 문란과 제품 개발 능력 약화 문제를 해소하고 제약산업의 경쟁력을 강화하려는 것으로 설명하고 있다.
이 법안에 대해 '위탁생동의 제한'이라고 표현하기도 하고, '공동생동의 제한'이라고 표현하기도 한다.
위탁생동을 '제한'하는 것은 쓸 수 있는 표현이지만 공동생동을 '제한'하는 것은 옳은 표현이 아니다. 민원서비스의 주체가 식약처인데 식약처를 제한하는 것은 맞지 않기 때문이다. 위탁생동을 제한하는 것은 위탁제조를 제한하는 것이며 위탁제조의 제한은 CMO양성정책과 반대방향의 정책이다.
위탁생동의 제한 추진에 더해 자료제출의약품의 위탁제조도 제한해야 한다는 주장도 제기된다. 그런데 자료제출의약품의 위탁제조에 대해서는 위탁임상이라는 용어는 사용하지 않고 공동임상이라고 일컫고 있다.
비용이 많이 들어가는 임상시험의 성격상 비용을 공동부담하는 느낌으로 다가오는 공동임상 용어를 쓰는 것이 편해서가 아닐까 싶다.
그런데, 예를 들어 코로나19 백신 한·중 공동임상 추진 등 '공동임상'은 제조측면의 관점과는 전혀 다른 개념의 용어이다. 위탁생동을 공동생동으로도 혼용해서 사용하는 관행이 임상으로 옮겨가면서 이상한 쓰임새가 되고 있는 것이다.
서영석의원이 제안이유에서도 밝혔듯이 1+3법안의 핵심은 의약품 위탁제조의 제한이다. 제약산업계를 뒤흔들 수 있는 것은 공동생동의 제한이 아니고 위탁제조의 제한이다.
지금부터라도 1+3법안의 효용성도 중요하지만 위탁제조의 제한이 가져오는 문제점도 제대로 따져보기 위해 용어부터 올바르게 정립할 필요가 있다.
1개 의약품의 허가권자는 단일하다. 공동허가권자는 있을 수 없다. 일반적으로 임상시험과 생물학적동등성시험의 의뢰자도 단일하다.
사업적으로 임상비용이나 생동비용을 공동부담할 수 있지만 법적 권한과 책임의 문제가 있으므로 비용조달주체를 전부 의뢰자로 인정하지 않는다.
그래서 임상시험과 생동시험을 통해 작성된 임상시험자료와 생동시험자료는 의뢰자가 소유권을 가지고 있고, 사업적 이해관계와 정책적 필요에 의해 시험자료는 자신도 사용하면서 타 업체에 허여할 수 있다. 의뢰자는 단일하지만 자료허여를 통해 공동소유가 가능하다.
'공동'의 용어는 지금까지 주로 생동시험과 관계되어서 사용되었다. 제조환경의 동일성이 중요한 생물학적 동등성시험의 특성상 생동시험자료의 허여는 동일 제조소를 전제로 이루어진다. 생동시험자료를 허여받은 업체는 허여해준 업체에 위탁제조를 맡기고 허여해준 업체는 수탁제조를 해준다.
즉, 생동시험자료의 공동소유는 허여받은 업체로서는 생동대상품목을 생동시험을 하지 않고 위탁제조하여 판매하기 위한 것으로 이를 관행적으로 위탁생동이라고 한다.
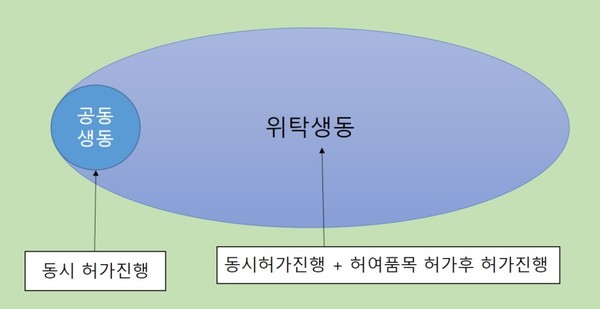
위탁생동으로 허가받는 방법은 2가지로 나눌 수 있는 데 허여해준 의약품과 같이 허가신청하는 것과 허여해준 의약품이 허가된 이후에 신청하는 것이 있다.
허여해준 의약품과 같이 허가신청을 하는 것을 따로 공동생동이라고 하는 데 이는 보험약가 제도상 생동자료를 허여해준 의약품과 허여받은 의약품들이 같은 시점에 약가를 신청해야 할 필요가 있는 제약업체들의 애로사항을 해소하기 위해 식약처가 운영하는 민원서비스라고 할 수 있다.
허가신청 민원은 개별적으로 처리하는 것이 원칙이나 식약처는 공동생동 품목의 경우 관련 업체들의 관할 행정기관(식약처, 지방식약청)들이 동시에 처리해주는 서비스를 해주고 있다.


