식약처, 21일 '바이오의약품 인허가 지원 워크숍'
업계 접근성 대폭 강화... "사전상담 거친 의약품 개발 단계 상승"

식품의약품안전처가 지난 11월 '혁신제품 사전상담' 전용 통합플랫폼을 구축했다. 혁신제품 사전 상담 신청 수요가 급증하면서 나온 후속 조치의 일환으로 업계의 이목이 집중되고 있다.
21일 오후 1시 서울 프레지던트 호텔에서 열린 '바이오의약품 인허가 지원 워크숍'에서 식약처 조창희 사전상담과 연구관은 "사전 상담을 거친 이후 의약품의 개발 단계가 상승한 것으로 나타났다"며 "총 상담 건수와 업계 만족도도 지속적으로 상승하고 있다"고 밝혔다.
식약처에 따르면 2020년 8월 사전상담과 신설 이후 2024년까지의 누적 운영 성과를 집계한 결과 총 447개 제품(의약품 200개, 의료기기 247개)을 대상으로 사전상담이 진행됐다.
식약처가 이 중 응답을 완료한 203개 품목(의약품 133개, 의료기기 70개)에 대한 개발 진행 상황을 분석한 결과 최초 상담 당시 비임상 단계에 있던 제품 중 임상 단계 등으로 개발이 진전된 사례는 의약품 85건, 의료기기 45건으로, 전체의 약 64%에서 개발 단계 진척이 이뤄졌다.
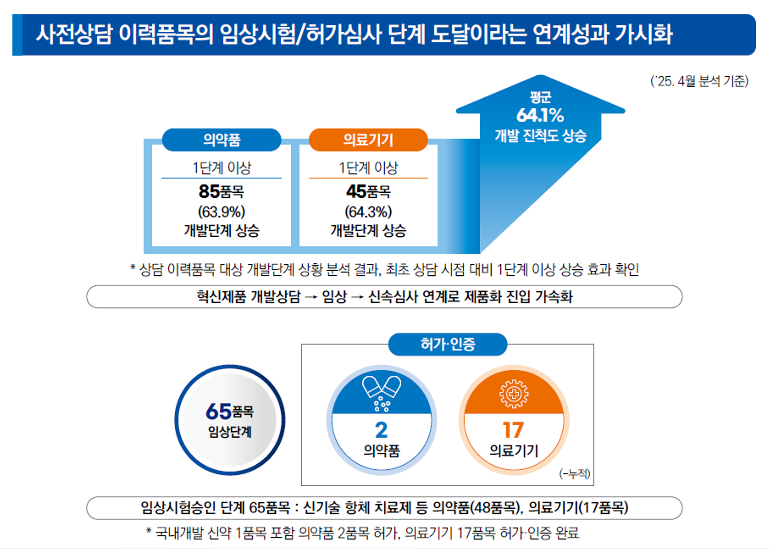
조창희 연구관은 "이중 작년 허가된 위식도역류질환 국산 신약(자큐보정)과 올해 허가된 국산 신약(엑스코프리)도 사전 상담 절차를 거쳤다"고 하면서 "혁신제품 사전상담 제도가 국내 신약 개발의 초기 개발 과정에도 도움이 됐다는 의미"라고 밝혔다.
식약처는 이날 '혁신제품 사전상담 시스템'을 개편했다고 밝혔다. 11월 1일부터 전용 통합플랫폼을 구축한 것으로 '원스톱' 시스템을 적용해 접근성을 높였다는 것이 식약처 설명이다.
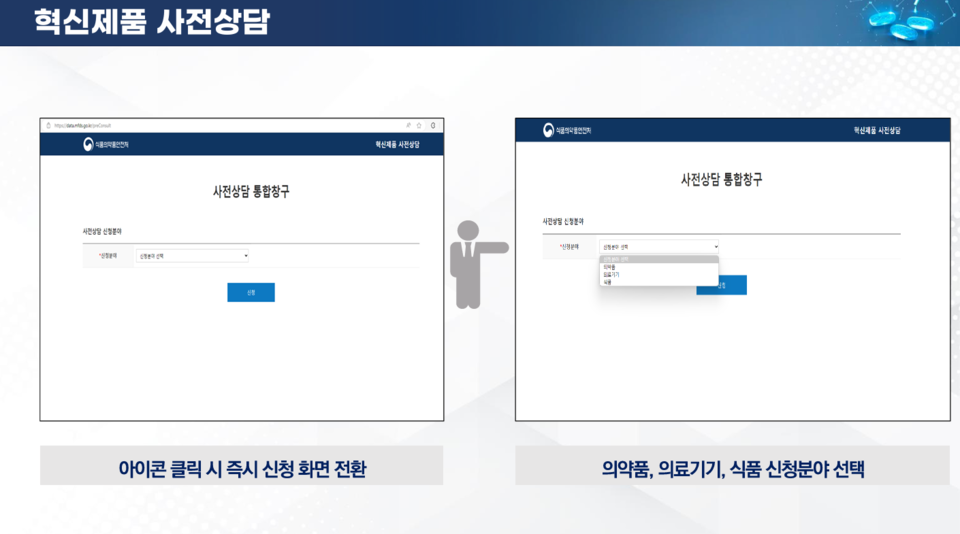
조창희 연구관은 "혁신제품 사전상담의 최초 로그인부터 상담신청까지 바로 할 수 있도록 원스톱 전용 플랫폼을 구축했다"며 "과거에는 홈페이지에서 각 카테고리별로 접근했지만 접근성이 떨어지고 절차가 복잡하다는 의견이 많아 홈페이지 전면에 배너를 노출하고 클릭하면 전용 플랫폼으로 이어지도록 설계했다"라고 설명했다.

과거에는 '식품의약품안전처 누리집 → 국민소통 → 적극행정 → 혁신제품 사전상담' 순서로 접근해 '의약품ㆍ바이오의약품ㆍ의료기기 분야 선택 후 사전상담' 신청을 하는 방식이었다.
그러나 11월부터는 식약처 메인 홈페이지에 '혁신제품 사전상담' 코너를 클릭하면 '사전상담 통합창구'로 바로 연결된다.
조창희 연구관은 "관련 내용을 작성하고 구비서류를 첨부하면 신청 이후 30일 이내에 결과 통지를 받아볼 수 있다"며 "사전 상담 결과가 법적 효력을 가지는 것은 아니지만 업계 만족도가 높아 개편을 결정했다"고 강조했다.
식약처가 이날 공개한 '혁신제품 상담 사례'도 눈길을 끌었다. A사는 "전이성 췌장암 치료제 임상 2상 임상시험 결과로 3상 임상시험 조건부 허가가 가능한가"라고 물었다.
이와 관련 식약처 사전상담과는 "개발 품목의 적응증 관련 대체 가능한 치료제가 다수 존재한다"며 "그런 점을 고려할 때 약사법에 따르면 조건부 허가가 어려울 것으로 판단된다"고 답했다.
업계에서는 이번 개편을 환영하는 분위기가 엿보이고 있다. 업계 관계자는 "제약사들이 조건부 허가 등 신약 개발 단계에서 규제기관의 입장을 파악하지 못하고 초기부터 개발을 하는 것은 무모한 시도"라며 "이번 개편은 사전상담 허들을 낮춰 업계에 개발 가이드라인을 명확히 제시한다는 측면에서 환영할 만한 대목이다"이라고 밝혔다.
이어 "다만 답변 내용이 더욱 상세할 수 있도록 상담의 질적인 변화도 함께 이뤄질 필요가 있다"라며 "짧은 답변보다는 관련 규정과 가이드라인을 상세하게 안내하고 그것이 개발 과정에서 일관성을 가지도록 한다면 업계와 식약처가 윈윈할 수 있는 시스템이 자리잡을 것"이라고 덧붙였다.

