바이오협회, FDA 2015년부터 올해 9월 누적 바이오시밀러 허가 분석
휴미라 10개·스텔라라 8개 등 블록버스터 중심
한국이 지금까지 미국 식품의약국(FDA)으로부터 18개의 바이오시밀러 허가를 받은 것으로 집계됐다. 미국에 이어 2번째로 많은 수다.
한국바이오협회 바이오경제연구센터는 FDA가 2015년부터 지난 9월까지 허가된 바이오시밀러 허가 현황을 살펴본 결과 이 같이 나타났다.
FDA가 2015년 첫 바이오시밀러를 승인한 이후 2025년 9월 말까지 누적 허가 건수는 총 75개였다. △2015년 1개, △2016년 3개, △2017년 5개, △2018년 7개, △2019년 10개, △2020년 3개, △2021년 4개, △2022년 7개, △2023년 5개, △ 2024년 18개, △ 2025년 9월말까지 12개가 허가됐다.
특히 2025년 9월말까지 허가된 12개의 바이오시밀러를 허가기업의 국적별로 구분해보면 한국이 4개로 가장 많았고, 인도 3개, 중국 2개, 프랑스 1개, 독일 1개, 영국 1개로 나타났다.
센터는 올해 FDA에서 허가된 바이오시밀러 개발기업의 국적 특징은 미국 기업이 없고, 인도 및 중국 기업의 약진이 두드러지는 것이라고 분석했다.
인도는 바이오콘 바이오로직스에서 3개 모두 허가 받았고, 중국은 상하이 헨리우스 바이오텍과 바이오테라 솔루션이 각각 1개씩 허가됐다. 특히 중국기업은 작년에 처음 FDA 허가를 받은 이래, 바이오시밀러 허가 신청이 계속 늘어나고 있다고 전했다.
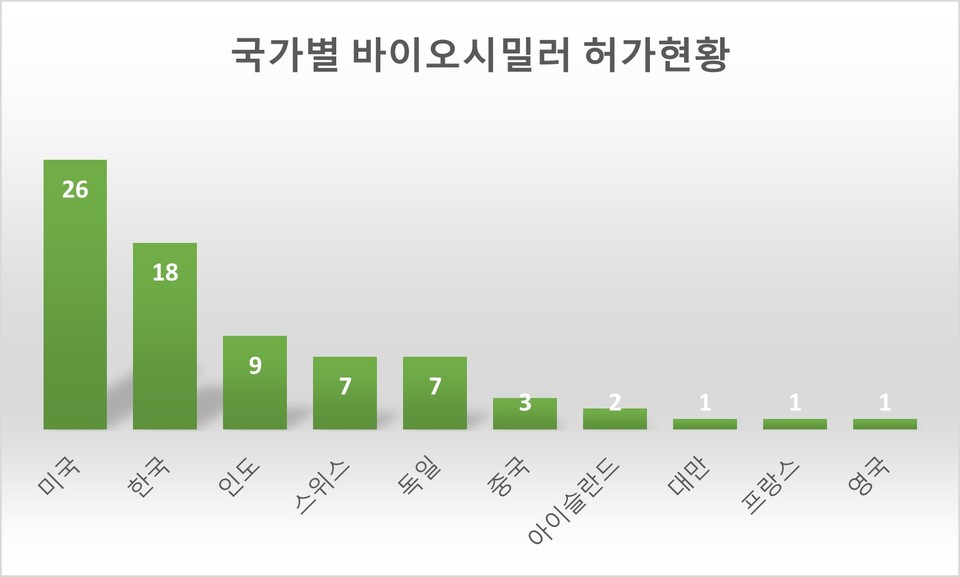
이와 함께 국가별로 바이오시밀러 허가현황을 보면 미국이 26개로 가장 많았고, 이어 한국 18개, 인도 9개, 스위스와 독일이 각각 7개, 중국 3개, 아이슬란드 2개, 대만·프랑스·영국이 각각 1개로 집계됐다.
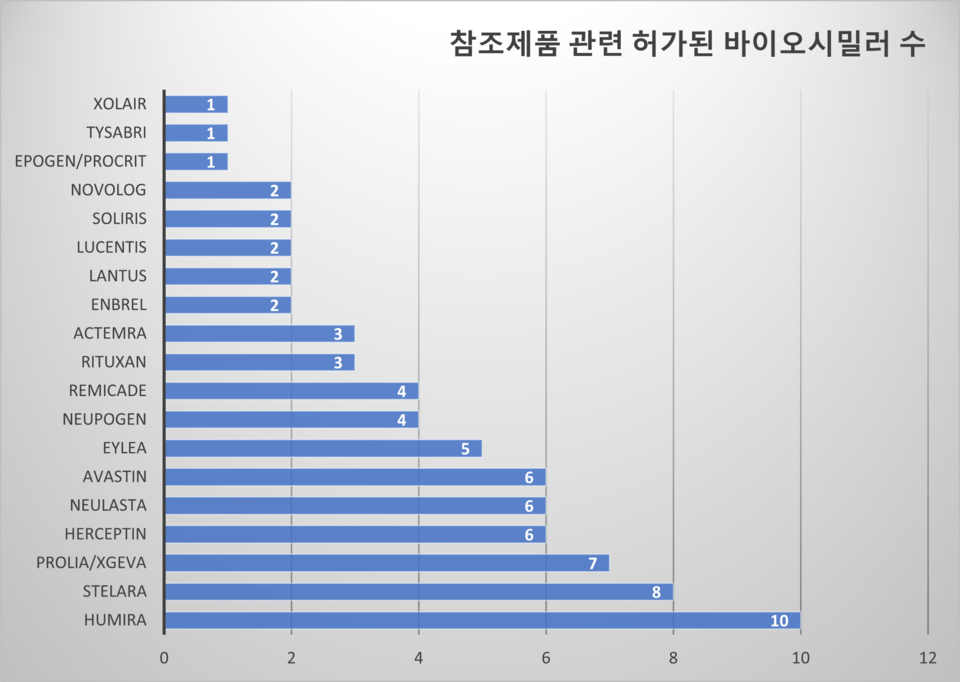
참조제품별 승인 현황을 보면 휴미라가 10개로 가장 많았고, 스텔라라 8개, 프롤리아 7개, 허셉틴, 뉴라스타, 아바스틴이 각각 6개였다. 이어 아일리아 5개, 뉴포젠과 레미케이드가 각각 4개, 리툭산과 악템라가 3개, 엔브렐, 란투스, 루센티스, 솔리리스, 노보로그가 각각 2개 승인됐다.

