심평원, 제8차 약제급여평가위원회 결과…2차 약제 영향 가능성도
백혈병약 '빅시오스리포좀주' 등재 한발 앞으로

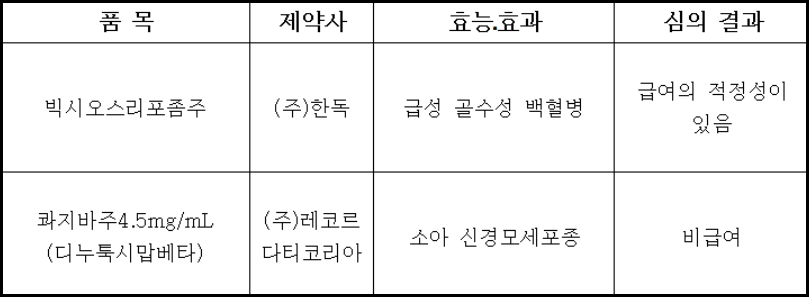
허가·평가·협상 연계 시범 사업 약제 '콰지바(성분 디누툭시맙베타)'가 약제급여평가위원회에서 비급여 판정을 받으면서 급여 등재에 어려움을 겪고 있다. 예상보다 늦어진 암질환심의위원회 통과에 이은 두 번째 난관이다.
건강보험심사평가원은 8일 2024년 제8차 약제급여평가위원회의 심의 결과를 공개했다.
보건복지부는 식품의약품안전처의 허가부터 평가 및 협상을 연계함으로써 총 300일이 넘는 급여 등재 기간을 단축시켜 약제의 신속한 시장 진입을 돕겠다는 목표로 시범 사업을 시작했다.
콰지바는 허가·평가·협상 연계 시범 사업 1호 대상 약제로, 지난해 8월 식약처의 글로벌 혁신 제품 신속심사(GIFT) 대상으로 지정됐으며, 지난 5월 급여기준이 설정되고, 6월 품목 허가를 획득했다. 만 12개월 이상의 소아 대상 '이전에 유도 화학요법 이후 부분 반응 이상을 보인 후 골수 제거 요법과 줄기세포 이식을 받은 이력이 있는 고위험군 신경모세포종' 및 '재발성 또는 불응성 신경모세포종'에서다.
다만 이번 약평위를 통과해 국민건강보험공단과 약가협상을 빠르게 완료하고, 1년여만에 급여권에 진입할 수 있을 것이라는 기대와 달리 급여 등재에 많은 시간이 소요되는 것으로 보인다. 또 다른 시범 사업 약제인 입센코리아의 '빌베이'는 허가가 지연되고 있다.
이런 상황에서 정부는 오는 12일까지 허가평가협상 연계 시범 사업의 2호 대상 약제를 모집한다. 예상과 달리 늦게 들려오는 급여 등재 소식과 제약업계가 1차 대상 약제 등재 프로세스에 주목하고 있는 만큼 2차 대상 약제 신청에 영향이 있을지 주목된다.
한독의 '빅시오스리포좀주(성분 시타라빈/다우노루비신)'은 첫 도전 만에 약평위를 통과하고, 약가협상 단계를 앞두고 있다. 급여 적정성을 인정받은 적응증은 '급성 골수성 백혈병'이다.
한편, 심평원은 혁신 신약 가치 보상 등을 통한 환자 접근성 제고와 관련된 약가 제도를 개선하고자 약평위 논의를 거쳐 '신약 등 협상 대상 약제의 세부 평가기준'을 개정했다고 밝혔다. △질병 부담이 큰 중증 난치 질환에 사용되는 약제까지 위험분담제(RSA) 적용 △추가 청구액 15억원 미만 RSA 약제 급여 확대 절차 간소화 △ICER 임곗값 평가 소요 중 하나인 혁신성 의미 구체화 및 성과 기반 환급형 RSA 적용 약제 임상 성과 평가 절차 기준 마련 등이다.
관련기사
- 허가·평가·협상 연계 시범사업 약 '콰지바, 8월 약평위 상정될까
- 반환점 돈 '허가·평가·협상' 연계 1호 약제... 정부, 2차 모집
- 허가-평가-협상 병행 시범사업 약제 '콰지바주' 허가
- 허가급여병행 '콰지바' 급여기준 설정...'루타테라', 허초승인 적용
- "허가-등재 첫 급행열차 탄 레코르다티는 1926년 설립된 제약회사"
- 코로나 확산에 진단키트 '품귀'… 의정갈등 속 제약 2Q 실적 '별로'
- 심평원, 병원 소속 임직원 대상 ESG 경영 최신 동향 소개
- 신약 '혁신성' 세부기준 신설…RSA 약제 급여 확대 절차 간소화
- "신약 평가기준 아쉽다, 실제 사례에 혁신가치 기조 반영되길"
- "외국약가 재평가 기준 마련 중... 약가조정은 내년 하반기"
- 2차 허가·평가·협상 연계 시범사업에 9개 약제 신청
- 코로나 치료제 등재에 밀린 신속도입 1호 약제 '콰지바'
- Nine Drugs Apply for Korea’s Second Pilot Project for Expedited Drug Approvals
- "중증·희귀질환약 신속등재 시범사업 1호 약제부터 지지부진"

