심평원, 29일 제4차 암질심 심의 결과 공개
퍼제타·카보메틱스 등 8개 치료제 급여기준 확대
허가-평가-협상 병행 시범사업 대상인 '콰지바(성분 디누툭시맙)'가 암질환심의위원회에서 급여기준이 설정됐다. 예상보다는 더딘 속도지만 남은 단계인 평가와 협상이 병행되면서 급여등재가 신속하게 진행될 것으로 전망된다.
이와 함께 치료 횟수 규제 개선 방안이 논의됐던 신경내분비종양 치료제 '루타테라(성분 루테튬(177Lu)옥소도트레오타이드)'에 허가범위 초과 사용승인 제도가 적용될 것으로 보인다.
건강보험심사평가원은 29일 2024년 제4차 암질환심의위원회의 심의 결과를 공개했다.
루타테라는 2022년 3월 급여 목록에 등재됐다. 다만 비급여 2회를 포함한 연간 6회의 급여 횟수 제한으로 인해 환자들이 독일, 말레이시아 등으로 해외 치료를 떠나야 한다며 올해 1월 국민 청원에 언급됐다.
심평원은 '허가 또는 신고 범위 초과 약제 비급여 사용승인 제도'를 검토하고, 이번 암질심에서 루타테라에 적용하는 것으로 심의했다.
루타테라의 추가 사용을 원하는 요양기관은 △다학제적위원회 심의 후 신청 △암질심 심의 △요양기관에 사용승인 결과 통보 △요양기관 사용내역 연 1회 제출 등의 절차를 거쳐 추가 치료가 가능하다.
고위험성 신경모세포종 치료제 '콰지바(성분 디누툭시맙)'도 암질심을 통과하면서 급여 등재에 한발 다가섰다. 콰지바는 '허가-평가-협상' 1호 약제로, 급여 등재를 위한 기간을 단축해 신속하게 시장에 진입할 것으로 보인다.
콰지바의 적응증은 만 12개월 이상의 소아 대상 '이전에 유도 화학요법 이후 부분 반응 이상을 보인 후 골수 제거 요법과 줄기세포 이식을 받은 이력이 있는 고위험군 신경모세포종' 및 '재발성 또는 불응성 신경모세포종'이다.
넥사틴주(옥살리플라틴) +로이코소듐주(류코보린) 등 + 중외5에프유주(플루오로우라실) 등 또는 넥사틴주(옥살리플라틴) + 젤로다정등(카페시타빈)는 국소 진행성 직장암의 전체선행항암화학요법에 급여기준이 설정됐다.
트리세녹스주(삼산화비소) + 베사노이드연질캡슐(트레티노인)은 새롭게 진단된 저위험(백혈구 수 ≤10×109/L) 급성전골수구성백혈병 성인 환자에서 트레티노인을 병용하는 관해유도 및 공고요법에 급여기준이 설정됐다.
이와 함께 심평원은 작년 12월 의사협회, 병원협회 등 각 의학회로부터 문제제기 되고 있는 급여기준에 대하여 개선의견을 수렴해 약제, 행위, 치료재료 전반에 걸쳐 의료계, 학회 등과 긴밀한 소통을 통해 개선 검토를 적극적으로 진행하고 있다고 밝혔다.
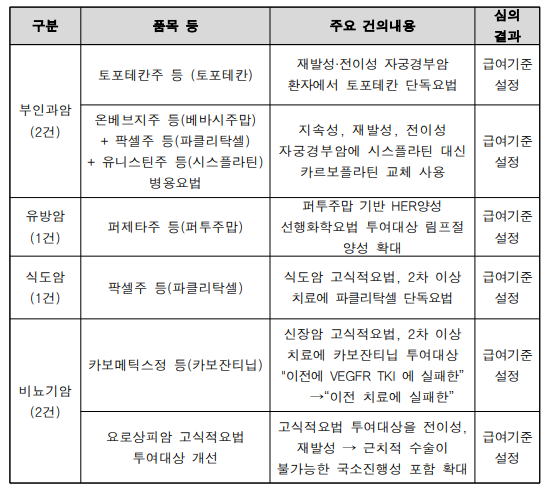
이와 관련 항암제 건의 항목은 TFT를 구성해 세부논의를 거친 후 위원회에서 심의하게 되며 이번 6개 항목을 심의했다. 부인과암과 유방암, 식도암, 비뇨기암 등에서 총 6개 항목이다.
관련기사
- "소아암 환자, 약도 정보도 없어… 특수상황 고려한 제도 필요"
- 울고 불고 난리쳐야만 움직이는, 외면 받는 K-약제급여 사이클
- "허가-등재 첫 급행열차 탄 레코르다티는 1926년 설립된 제약회사"
- 시흥시 제약사 제조소에서 화재…근로자 등 2명 부상
- 허가-평가-협상 병행 시범사업 약제 '콰지바주' 허가
- 반환점 돈 '허가·평가·협상' 연계 1호 약제... 정부, 2차 모집
- 허가·평가·협상 연계 시범사업 약 '콰지바, 8월 약평위 상정될까
- 허가·평가·협상 1호인데… 신경모세포종 치료제 '콰지바' 비급여 결정
- 코로나 치료제 등재에 밀린 신속도입 1호 약제 '콰지바'
- "해외에선 가능, 국내는 복잡… 허가초과 제도의 딜레마"
- [WCLC] 루타테라, 전이성 BPNET 환자 실제임상서 생존기간 21개월 확인

