2026년 제1차 암질환심의위원회 심의 결과
카보메틱스·자카비 급여 기준 확대 통과

길리어드코리아의 미만성 거대 B세포 림프종(DLBCL) 치료제 '예스카타(성분 악시캅타젠실로류셀)'가 2차 치료에서 급여기준이 미설정됐다.
렉라자와 병용요법으로 주목받는 한국얀센의 '리브리반트(성분 아미반타맙)'도 암질환심의위원회 문턱을 넘지 못했다.
건강보험심사평가원은 21일 2026년 제1차 암질심 회의를 열고 △예스카타 △임델트라 △리브리반트 △자카비 △포말리스트 △카보메틱스 △사이람자 등 항암제의 급여 기준을 심사했다.
예스카타는 지난해 8월 DLBCL 환자의 2·3차 치료에서 국내 허가를 획득했다. 허가 적응증은 '1차 화학면역요법 치료 이후 12개월 이내에 재발하거나 불응하는 DLBCL 성인 환자의 치료' 및 '2차 이상의 전신 치료 후 재발성 또는 불응성 DLBCL 및 원발성 종격동 B세포 림프종이 있는 성인 환자 치료제'다.
노바티스의 '킴리아'와 얀센 '카빅티' 이후 국내에서 세번째로 허가 받은 CAR-T 치료제다. 이중 킴리아와 DLBCL에서 동일한 적응증을 보유하고 있는데 예스카타가 2차 치료제로 적응증을 획득하면서 급여 등재 시 3차 이상에서 사용되던 킴리아 대비 사용범위가 넓을 것으로 예상됐었다.
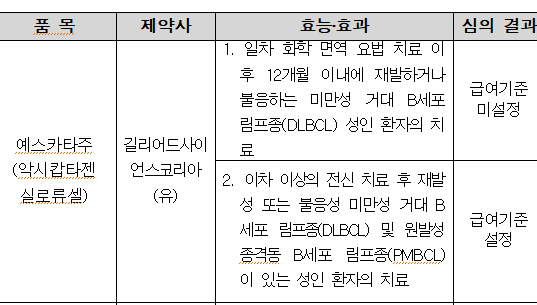
그러나 이번 암질심에서 예스카타는 '일차 화학 면역 요법 치료 이후 12개월 이내에 재발하거나 불응하는 DLBCL 성인 환자의 치료'에서 재도전을 준비하게 됐다. 이차 이상의 전신 치료 후 재발성 또는 불응성 미만성 거대 B세포 림프종(DLBCL) 및 원발성 종격동 B세포 림프종(PMBCL)이 있는 성인 환자의 치료에는 급여기준이 설정됐다.
리브리반트는 △EGFR 엑손 20 삽입 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 성인 환자의 1차 치료로서 카보플라틴 및 페메트렉시드와의 병용요법 △EGFR 엑손 19 결손 또는 엑손 21(L858R) 치환 변이된 국소 진행성 또는 전이성 비소세포폐암 성인 환자의 1차 치료로서 레이저티닙과의 병용요법 △이전에 EGFR TKI를 포함하여 치료받은 적이 있는 EGFR 엑손 19 결손 또는 엑손 21(L858R) 치환 변이된 국소 진행성 또는 전이성 비소세포폐암 성인 환자에서의 카보플라틴 및 페메트렉시드와의 병용요법 등에서 모두 급여기준 설정에 실패했다.
이번 암질심에서는 급여기준 확대를 신청한 약제들이 모두 급여기준 설정이 결정됐다.
입센코리아의 '카보메틱스(성분 카보잔티닙)'은 '이전에 VEGF 표적요법으로 치료 받은 적이 있는 진행성 신장세포암 환자에서의 단독요법'으로 급여 기준 확대에 한발 다가섰다. 회사 측은 지난해 5월 약가협상 불발 이후 '면역항암제 치료 경험이 있는 신세포암 환자'에서도 재도전 할 계획이다.
한국노바티스의 야누스 키나아제(JAK) 억제제 '자카비(성분 룩소리티닙인산염)'는 골수섬유증·이식편대숙주질환에 더해 진성적혈구증가증으로 급여기준이 설정됐다. 삼양홀딩스·대웅제약·종근당 등 3개 회사가 제네릭 출시를 노리는 가운데 급여 기준 확대로 처방량을 늘릴 수 있을지 주목된다.
이외 급여기준 확대를 신청한 포말리스트캡슐(한국BMS제약)과 사이람지주(한국릴리)도 기준 설정에 성공했다.

