전진숙 의원, 국내신약 역차별 우려 급여 적정성 재평가 기준 지적
복지부 "외자사 역차별·통상문제 우려...천연물 약가우대 검토" 답변
기등재의약품의 생사 여탈을 좌우하는 급여 적정성 평가를 앞두고 국내 개발 신약에 대한 역차별 조항이 도마 위에 올랐다. 천연물 신약 연구개발과 산업화를 위한 약가우대 부활도 검토 대상으로 꼽혔다.
국회 보건복지위원회 소속 더불어민주당 전진숙 의원은 최근 복지위 서면질의을 통해 급여 적정성 재평가 방향에 대한 복지부 입장을 질의했다.
전 의원은 먼저 "급여 적정성 재평가 대상 선정기준 중 'A8국가 2개국 등재 미만'은 국내개발 신약 및 천연물 신약에 대한 역차별로 이 기준을 수정하거나 폐기해야 한다는 지적이 있다"고 짚었다.

2025 급여 적정성 재평가 대상은 '올로파타딘염산염'(알레르기용약) 등 8개 성분으로, 이 가운데 '위령선·괄루근·하고초'(해열진통소염제)와 '애엽추출물'(소화성 궤양용제) 등 천연물 신약이 포함돼 있다.
복지부는 청구현황 및 제외국 급여 현황, 정책적 사회적 이슈, 기타 필요성 등을 종합적으로 고려해 평가 대상을 선정한다는 원칙을 세웠지만, 업계는 A8 국가 중 2개국 미만에 등재된 기등재약을 급여 적정성 평가 대상으로 선정한 기준은 해외 진출 여력이 부족한 국내 산업 현실과 맞지 않다는 애로사항을 호소해 왔다.
복지부는 그러나 "국내 개발 신약만 평가 대상에서 제외하는 것은 외국 제약사에 대한 역차별 및 통상 문제 소지가 있어 신중한 검토가 필요하다"며 "선별급여 체계 하에서 암상적 유용성이 없는 약제 급여를 유지하는 것은 적절하지 않다"는 입장을 표명했다.
전 의원은 이와함께 "천연물 신약의 경우 '천연물신약 개발법'에 따른 산업화 촉진과 사회적 요구도를 반영해 급여 유지할 필요가 있다는 지적도 있다"며 복지부 방침을 물었다.
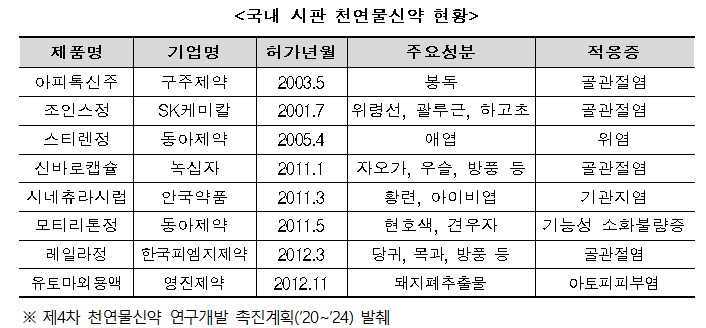
복지부에 따르면 '천연물신약 연구개발촉진법'이 제정된 후 국내에서 천연물 신약으로 허가를 받은 품목은 총 8개 품목이다. 정부는 천연물 신약의 연구개발 및 산업화를 장려할 목적으로 '천연물신약 연구개발 촉진법'을 제정하고 별도 허가 기준을 운영해 왔으나, 천연물 신약 연구개발 성과가 미진하다는 감사원 지적에 따라 2017년 천연물 신약의 정의와 별도 허가·심사기준 등이 삭제됐다.
한편 천연물 신약의 경우, 화합물의약품과 동일한 기준으로 임상적 유용성을 평가하기 어렵지만 약 20년 간 진료 현장에 처방돼 임상근거를 축적한 만큼, 천연물 특성을 반영한 별도 평가기준이 필요하다는 의견도 있었다.
복지부는 이와 관련 "국내외 임상진료지침, 연구문헌 등을 종합적으로 검토한 결과 임상적 유용성이 불분명한 것으로 판단될 경우 사회적 요구도를 평가하게 된다"며 "진료현장의 의견이 충분히 반영되도록 노력하겠다"고 밝혔다.
'천연물신약 연구개발 촉진법' 취지에 따라 약가 혜택을 부활하는 방안에 대해서는 "천연물 기반 의약품 개발 촉진을 지원할 수 있도록 현장 의견 등을 종합적으로 고려해 약가 우대 방안을 검토하겠다"고 답했다.

