심평원, 제1차 암질환심의위원회 개최
급여결정신청 4개 신약 중 3개 급여기준 미설정
올해 첫 열린 암질환심의위원회에서 BMS의 신약 '인레빅캡슐'만이 급여기준이 설정됐다. 자카비 이후 10년만에 국내 출시된 솔수섬유증 치료제다.
건강보험심사평가원은 1일 2023년 제1차 암질환심의위원회를 개최하고 급여결정을 신청한 신약을 심의했다.
4개의 신약의 급여결정 신청을 살펴본 결과 인레빅캡슐만 급여기준이 설정됐다. 해당 약제는 전에 룩소리티닙으로 치료를 받은 성인환자의 △일차성 골수섬유증, △진성적혈구증가증 후 골수섬유증, △본태성혈소판증가증 후 골수섬유증과 관련된 비장비대 또는 증상 치료에 사용된다.
골수섬유증은 골수의 과도한 섬유성 증식과 함께 정상적인 조혈기능이 저하되는 희귀혈액암으로, 국내 환자 수는 1700여명 정도로 추산되고 있다. 2차 치료옵션이 부재한 상황에서 인레빅이 항암제 첫 급여관문인 암질심을 통과함에 따라 의료현장의 기대감이 올라갈 것으로 전망된다.
인레빅은 약제급여평가위원회와 건강보험공단과의 협상, 건강보험정책심의위원회 결정 및 고시 등의 단계를 밟게 된다.
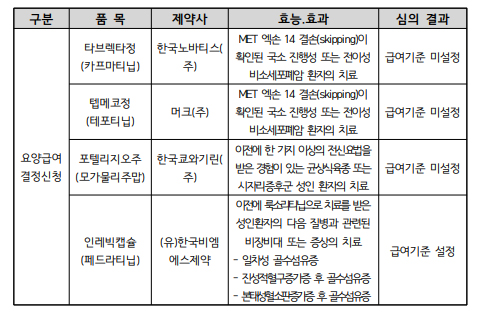
반면 3개의 신약은 암질심 문턱에서 주저앉았다.
MET 엑손 14 결손(skipping)이 확인된 국소 진행성 또는 전이성 비소세포폐암 환자 치료에 사용되는 한국노바티스 '타브렉타'와 머크의 '텝메코'는 나란히 고배를 마셨다.
타브렉타는 작년 8월에 암질심 심의결과에서도 급여기준이 미설정됐으며 이번에는 경쟁약인 텝메코도 같이 급여기준이 미설정됐다.
타브렉타는 경제성평가 면제 위험분담제 조건을 충족해 급여결정을 신청했지만 암질심 심의결과 2상 임상만으로 임상적 유효성을 평가할 수 없다며 진도가 나가지 못하면서 작년 국정감사에서도 급여등재를 촉구한 바 있다.
하지만 이번에도 암질심에서는 급여기준을 미설정했다.
한국쿄와기린의 '포텔리지오주'는 이전에 한 가지 이상의 전신요법을 받은 경험이 있는 균상식육종 또는 시자리증후군 성인 환자의 치료제로, 급여기준이 설정되지 않았다.

