단독 · 메트포르민 병용 · 메트포르민+DPP-4 억제제 병용
혈당조절 안 되는 환자에 병용 지속관찰할 목적, 연장임상
한 눈에 보는 임상 승인·품목 허가 - 3월 3주(03.15~19.)

대웅제약이 제2형 당뇨병 치료 물질 '이나보글리플로진'에 3개 적응증을 장착하기 위한 임상 연구개발에 박차를 가하고 있다. 기존 치료제로 혈당이 조절되지 않는 환자들에게 도움될 '계열 내 최고 신약'으로 만들겠다는 계획이다.
신풍제약은 1회 투여 만으로도 6개월보다 더 약효가 이어질 골관절염 주사제를, 일동제약은 고혈압-이상지질혈증 4제 복합제 개발에 속도를 내고 있다.
한미약품은 지난 18일 국내 33번째 신약으로 롤론티스를 허가받은 것에 대해 "미국 등에서도 허가받아 글로벌 시장에서 성공하는 신약으로 키우겠다"는 목표를 밝혔다.
신풍제약, 6개월 이상 효과 골관절염 치료 HA제제 3상 승인
일동제약, 한미약품+종근당 이어 4제 복합제 개발 뒤쫓는다
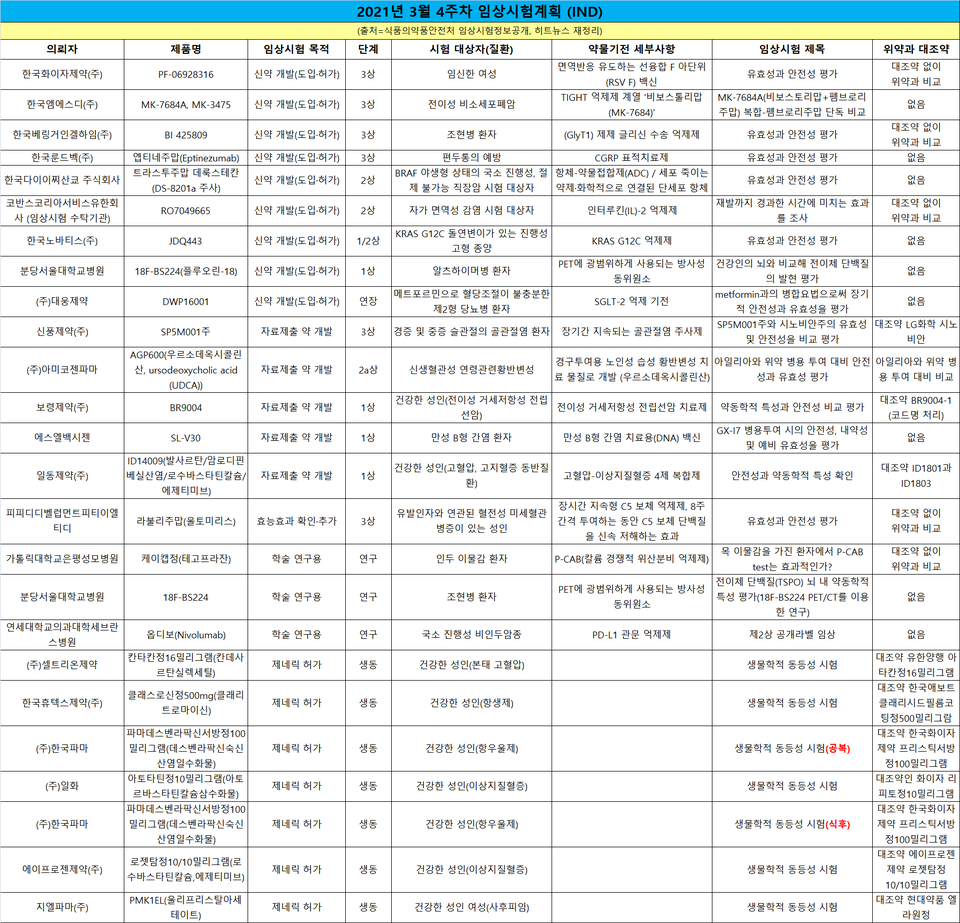
히트뉴스(www.hitnews.co.kr)가 3월 3주(15~19일) 임상시험 현황을 집계한 결과 25건이 신규 승인됐다. 목적별로 ▲신약 개발·도입 등 9건 ▲제네릭 허가를 위한 생동 7건 ▲자료제출 약 개발 5건 ▲학술 연구용 3건 ▲효능효과 확인·추가 1건 순이다.
이 가운데 대웅제약이 제2형 당뇨병 치료 물질 '이나보글리플로진(DWP16001)' 관련 연장 임상시험을 지난 16일 승인받았다. 메트포르민으로 혈당조절이 불충분한 제2형 당뇨병 환자에서 '메트포르민과 병합요법으로 DWP16001'의 장기적 안전성과 유효성을 평가할 목적'의 '연장 임상시험'이다.
회사는 지난해 9월 같은 취지의 3상을 승인받아 환자를 모집하고 있다. 연장 임상은 대상환자에게 지속 투여해 관찰할 목적으로 풀이된다.
이와 관련, 건강한 남성 대상으로 이나보글리플로진과 메트포르민 병용 시 약물상호작용을 평가하는 1상을 2019년 진행했는데 이달 12~17일 온라인으로 열린 미국 임상약리학회에서 관련 결과가 발표됐다.
시험책임자인 장인진 서울대병원 임상약리학과 교수 발표에 따르면, 이나보글리플로진 또는 메트포르민 단독투여 대비 이나보글리플로진∙메트포르민을 함께 투여했을 때 약물 혈중 농도를 비교한 임상 결과 유의미한 혈중 농도 차이가 없어 두 약물이 서로 영향을 주지 않음이 확인됐다.

이를 바탕으로 대웅제약은 메트포르민 병용 요법 3상과 연장 임상을 승인받게 됐다. 현재 대웅제약은 ▲이나보글리플로진 단독 요법 ▲이나보글리플로진과 메트포르민의 병합요법 ▲이나보글리플로진과 메트포르민 그리고 DPP-4 억제제 계열 제미글립틴의 병합요법까지 적응증 3개를 동시에 개발하고 있다.
이나보글리플로진은 콩팥에서 포도당 재흡수에 관여하는 SGLT-2를 선택적으로 억제해 포도당을 소변으로 배출시키는 방식으로 작용하는 후보물질이다. 대웅제약은 이 물질을 SGLT-2 억제제 계열 내 최고(Best-in-class) 신약으로 개발하겠다며, 오는 2023년 국내 발매를 목표로 하고 있다.
신풍제약이 1회 투여 만으로 약 6개월 이상 약효가 지속되는 '1회 제형 골관절염치료제(SP5M001주)' 3상 임상시험을 지난 16일 승인받았다. 경증·중등증 슬 골관절염 환자 대상으로 LG화학의 '시노비안주' 대비 유효성과 안전성을 비교 평가할 계획이다.
신풍제약은 "미변형 히알루론산 나트륨(HA)보다 생체 내에서 오래 지속되고 다른 가교 결합물에 비해 높은 생체적합성을 나타내, 1회 주사에 의해 관절에서 장시간 ▲지속되는 진통 효과 ▲연골보호효과 ▲활막 염증 억제효과를 보일 것"이라고 SP5M001주를 소개했다.

신풍제약은 휴메딕스와 공동 개발해 1회 투여 만으로 약 6개월 간 약효가 지속되는 골관절염치료제를 지난 2019년 '하이알원샷(1회 제형)'이라는 품목으로 발매했다.
하이알원샷보다 이 약물 효과 유지기간을 길게 해 골관절염 치료제 시장에서 주도권을 잡으려 할 것으로 관측된다.
일동제약도 고혈압·이상지질혈증 4제 복합제를 개발하고 있는데, 고혈압 치료 발사르탄, 암로디핀에 이상지질혈증 치료 로수바스타틴, 에제티미브를 조합으로 확인됐다.

지난 17일 안전성과 약동학적 특성을 확인하는 관련 임상 1상을 승인받았다.
한미약품은 자사의 암로디핀+로사르탄 성분 고혈압 복합제 '아모잘탄'에 역시 자사의 이상지질혈증 치료 복합제로 로수바스타틴+에제티미브 '로수젯'을 조합한 '아모잘탄엑스큐'를 지난해 11월 허가받아 국내 제약사 중 시장에 가장 먼저 진입했다.
종근당도 자사 텔미사르탄+암로디핀 성분 고혈압복합제 '텔미누보'에 이상지질혈증 치료 로수바스타틴과 에제티미브를 더한 'CKD-348'을 개발 중인데 최근 상표권 '텔미누보젯'을 출원한 것으로 확인됐다. 한미약품과 종근당이 일동제약의 상업화보다는 앞선 것으로 보이는데, 국내 제약사 간의 4제 복합제 시장 경쟁이 치열할 전망이다.
33번째 신약으로 허가 '롤론티스'…글로벌 공략에도 기대감
3월 3주(15~19일) 식품의약품안전처로부터 38품목이 허가받았다. 이 중 한미약품의 호중구 감소증 치료제 '롤론티스프리필드시린지주(에플라페그라스팀)'가 33번째 국내 신약이 됐다.
롤론티스는 한미약품이 개발해 2012년 미국 스펙트럼에 라이선스 아웃했다. 한미약품의 플랫폼 기술인 '랩스커버리'가 적용돼, 항암화학요법을 받는 암 환자에서 발생하는 호중구감소증의 치료 또는 예방 용도로 투여되는 약효 지속형 바이오 신약이다.
롤론티스는 한국에서 세계 최초로 허가됐는데, 스펙트럼과 한미약품은 롤론티스의 미국 시판허가 절차를 진행하고 있다. 미 식품의약국(FDA)은 롤론티스 원액을 생산하는 평택 바이오플랜트의 '승인 전 실사'를 오는 5월에 할 예정이다. 한미약품에 따르면 호중구감소증 치료제 국내 시장 규모는 800억원대, 글로벌 시장은 3조원대로 추정된다.
권세창 한미약품 사장은 보도자료를 통해 "한국에서의 세계 첫 허가를 시작으로 미국 등에서도 허가를 획득해 글로벌 시장에서 성공하는 한국의 첫번째 바이오신약이 될 수 있도록 최선을 다하겠다"고 말했다.

