유방암 치료제 8품목 최다, 바이오의약품은 4품목 불과
올해 허가받은 항암제는 총 30품목이며, 이중 국내 제약사는 10품목을 허가받은 것으로 나타났다.
30품목중 26품목은 케미칼 의약품이고 바이오 의약품은 4품목에 불과했다.
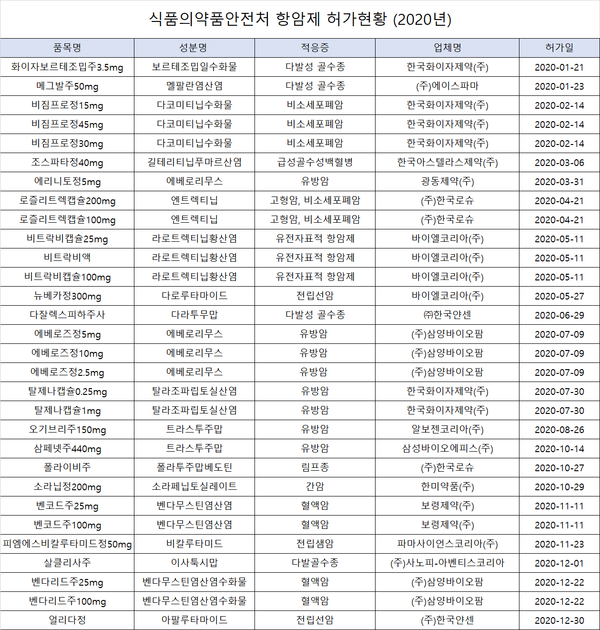
식품의약품안전처의 2020년 항악성 종양제 허가현황을 분석한 결과, 유방암 치료제 8품목, 비소세포폐암 치료제 5품목, 다발성골수종 치료제 4품목, 혈액암 치료제 4품목, 유전자표적항암제 3품목 총 20성분 30품목이 허가받은 것으로 집계됐다.
허가받은 항암제중 국내 제약사는 ▲에이스파마의 다발성 골수종 치료제 '메그발주50mg' ▲광동제약의 유방암 치료제 '에리니토정 5mg' ▲삼양바이오팜의 유방암 치료제 '에베로즈정' 2.5mg, 5mg, 10mg 3품목 ▲한미약품의 간암 치료제 '소라닙정200mg' ▲보령제약의 혈액암 치료제 '벤코드주' 10mg, 25mg ▲삼양바이오팜의 혈액암치료제 '벤다리드주' 25mg, 100mg 등 총 10품목으로 파악됐다.
한국화이자가 1월에 허가받은 '화이자보르테조밉주3.5mg‘은 '보르테조밉일수화물‘이 주성분으로 다발성 골수종과 외투세포림프종을 효능·효과로 허가받았다
에이스파마의 '메그발주50mg‘는 주성분이 '멜팔란염산염'으로 다발성 골수종을 효능·효과로 허가받았다.
한국화이자의 비소세포폐암 치료제 '비짐프로정15mg', '비짐프로정30mg', '비짐프로정45mg' 등 3품목은 2월 14일 허가받았다. '비짐프로정'의 주성분은 다코미티닙수화물으로 '상피세포성장인자수용체(EGFR) 엑손 19 결손 또는 엑손 21 L858R 치환 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 환자의 1차 치료'를 효능·효과로 한다.
광동제약의 유방암치료제 ‘에리니토정5mg(에베로무스)’는 3월 31일 허가받았다. '에리니토정5mg'은 칠레 제약사인 'Synthon chile ltda.'에서 수입한다. 광동제약은 지난해 3월 에베로무스 성분의 '에리니토정10mg'을 허가받은바 있다. 유방암 치료제 '에베로무스' 제제의 오리지널 의약품은 노바티스의 '아피니토'이다.
로슈의 'NTRK(신경성 티로신수용체키나제)' 표적 항암제인 ‘로즐리트렉캡슐(엔트리티닙)100mg’과 ‘로즐리트렉캡슐200mg’은 4월 21일 희귀의약품으로 허가받았다. ‘로즐리트렉캡슐’은 알려진 획득 내성 돌연변이 없이 NTRK(neurotrophic tyrosine receptor kinase)융합 유전자를 가진 성인과 만 12세 이상 소아의 고형암 치료에 사용한다. 또 성인의 ROS1 양성인 국소 진행성 또는 전이성 비소세포폐암에 사용할 수 있다.
바이엘코리아의 유전자 표적 항암치료제인 TRK 억제제 '비트락비' 3개 품목(비트락비액, 비트락비 캡슐 100mg, 25mg)은 5월 11일 허가받았다.
'비트락비'는 알려진 획득 내성 돌연변이가 없는 NTRK(neurotrophic receptor tyrosine kinase)유전자 융합을 보유한 성인 및 소아 환자 중 국소진행성, 전이성 또는 수술적 절제 시 중증 이환의 가능성이 높으며 기존 치료제(혹은 치료 요법) 이후 진행됐거나 현재 이용가능한 적합한 치료제가 없는 고형암 환자의 치료에 사용할 수 있다.
바이엘코리아의 '뉴베카정300mg'은 비전이 거세저항성 전립선암(nmCRPC) 환자를 위한 치료제로 5월 27일 허가받았다. '뉴베카정300mg'은 독특한 화학구조를 가진 안드로겐 수용체 저해제(ARi)로 안드로겐 수용체에 결합해 강한 길항작용을 통해 전립선암 세포의 성장을 억제한다.
한국얀센의 '다잘렉스피하주사(다라투무맙)은 한 가지 이상 항암요법에 실패한 환자에게 덱사메타손, 레날리도마이드(lenalidomide) 혹은 보테조밉(bortezomib)과 병합하여 사용할 수 있는 다발골수종 치료제이다.
삼양바이오팜은 유방암 표적항암제 ‘에베로즈 정(성분명 에베로리무스)’ 2.5mg, 5mg. 10mg 등 총 3가지 용량에 대한 품목 허가를 7월 9일 취득했다. '에베로즈 정'은 유방암 외에도 신경내분비암, 중추신경계암, 신장암 등에 적응증을 가지고 있는 노바티스의 '아피니토'의 제네릭이다.
한국화이자는 '탈라조파립토실산염(talazoparib tosylate) 성분의 유방암 치료제 신약인 '탈제나캡슐' 0.25mg, 1mg을 7월 30일 허가받았다.
로슈의 유방암 치료제 '허셉팁(트라스주맙)'의 바이오시밀러인 알보젠코리아의 '오기브리주150mg'와 삼성바이오에피스의 '삼페넷주440mg'은 각각 8월과 10월에 허가받았다.
한국로슈는 폴라투주맙베도틴(polatuzumab vedotin) 성분의 거대 B세포 림프종 치료제 신약 '폴라이비주'를 10월 27일 허가받았다. 폴라투주맙베도틴은 B세포 수용체의 구성 성분인 CD79b를 표적으로 하는 항체-약물 접합체이다.
한미약품은 간암 치료제인 '넥사바(바이엘)'의 퍼스트 제네릭인 '소라닙정 200mg'을 10월 29일 허가받았다. '소라닙정 200mg'은 특허도전에 성공해 출시 후 9개월간 후발의약품 시장 독점권도 획득했다.
보령제약은 에자이의 혈액암 치료제 '심벤다주'의 퍼스트 제네릭인 '벤코드주' 25mg(벤다무스틴염산염), 벤코드주100mg(벤다무스틴염산염)을 국내에 도입해 11월 11일 허가받았다.
파마사이언스코리아는 전립샘암 치료제인 '피엠에스비칼루타미드정50mg'를 11월 23일 허가받았다.
사노피-아벤티스코리아의 재발·불응성 다발골수종 치료제 '살클리사주'(이사툭시맙)은 12월 1일 허가받았다.
'살클리사주'는 이전에 레날리도마이드와 프로테아좀억제제를 포함한 두 가지 이상의 치료를 받은 다발골수종 환자에서 포말리도마이드 및 덱사메타손과의 병용요법으로 승인됐다.
'살클리사주'는 다발골수종 세포들에 나타나는 CD38 수용체의 특정 항원결정기(epitope)와 결합해 종양 세포 사멸을 유도하는 기전의 단클론항체 치료제다.
삼양바이오팜은 혈액암 치료제 ‘벤다리드주(벤다무스틴)’ 25mg과 100mg 등 두 가지 용량에 대한 품목 허가를 12월 22일 취득했다.
'벤다리드주'는 ‘한국에자이’의 ‘심벤다주’ 제네릭으로 ▲림프 조직에 생기는 악성 종양인 여포형 림프종에서 표적항암제 ‘리툭시맙’과의 병용요법 ▲혈액암 중 하나인 만성 림프구성 백혈병 ▲다발골수종 등에 적응증을 갖고 있다.
삼양바이오팜은 저온 제조 공법을 통해 안정성을 확보함으로써 그동안 수입에만 의존하던 벤다무스틴 제제의 국산화에 성공했다.
한국얀센의 '얼리다정(아팔루타마이드)'은 '호르몬 반응성 전이성 전립선암(mHSPC) 환자의 치료에 안드로겐 차단요법(ADT)과 병용'을 효능·효과로 12월 30일자 신약으로 허가받았다.
아팔루타마이드는 차세대 경구용 안드로겐 수용체 저해제의 일종으로, 2018년 2월 FDA로부터 '얼리다'(Erleada)라는 제품명으로 승인을 취득한 바 있다. 비전이성 거세저항성 전립선암 치료제가 FDA의 승인을 취득한 것은 '얼리다정'이 처음이다.