복지부-식약처, 시장 즉시진입 의료기술 제도 시행
식약처 임상평가 통과 시 신의료기술평가 없이 즉시 사용
혁신 의료기기가 식품의약품안전처의 강화된 임상평가를 거친 경우 별도의 신의료기술평가 없이 의료현장에 즉시 사용할 수 있는 제도가 도입된다.
보건복지부(장관 정은경)와 식품의약품안전처(처장 오유경)는 '시장 즉시진입 의료기술' 제도를 도입·시행한다고 26일 밝혔다. 해당 제도는 '신의료기술평가에 관한 규칙'과 '의료기기 허가·신고·심사 등에 관한 규정' 개정 절차가 마무리되는 오늘(26일)부터 시행된다.
신의료기술평가는 새로운 의료기술이 의료현장에 사용되기 전 안전성과 유효성을 검증하는 절차다. 그간 평가 유예 제도 등이 운영돼 왔으나 절차가 복잡하고 소요 기간이 길어 우수 의료기술의 조기 도입에 한계가 있다는 지적이 있었다.
이에 두 부처는 협업을 통해 의료기기 허가 단계에서 국제적 수준의 강화된 임상평가를 거친 의료기기를 사용하는 의료기술에 한해 신의료기술평가를 면제하고 즉시 시장 진입을 허용하는 제도를 마련했다.
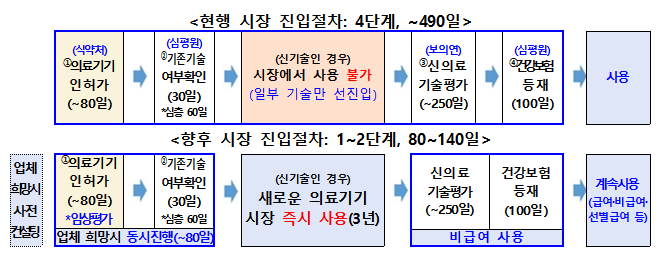
이번 개정으로 최장 490일이 소요되던 시장 진입 기간은 최단 80일까지 단축될 전망이다.
복지부는 규칙 개정을 통해 시장 즉시진입 의료기술의 대상을 규정하고, 건강보험심사평가원에 기존기술 여부를 확인받아 기존기술이 아닌 경우 복지부 장관 고시로 즉시 사용이 가능하도록 했다.
다만, 비급여 남용을 방지하고 환자 부담을 관리하기 위해, 필요 시 즉시진입 사용 기간 중에도 장관 직권으로 신의료기술평가를 실시하고 급여 여부를 결정할 수 있도록 했다.
식약처는 허가 단계에서 신의료기술평가 유예 적용이 가능한 의료기기 공고 근거를 마련하고 임상평가자료 제출 근거와 세부 기준을 신설했다. 임상시험 자료, 시판 후 조사와 실사용 자료, 임상 문헌 등 국제적 수준의 임상평가자료 제출을 요구해 안전성 검증을 강화한다는 방침이다.
아울러 식약처는 시장 즉시진입 대상 의료기기 품목으로 디지털의료기기, 체외진단의료기기, 의료용 로봇 등 총 199개 품목을 공고했다. 디지털의료기기 113개 품목, 체외진단시약 83개 품목, 로봇수술기·외골격장치 등 기타 품목이 포함된다.
곽순헌 복지부 보건의료정책관은 "의료기기 시장 진입 절차를 간소화해 산업을 활성화하고 우수 의료기기의 조기 현장 도입을 지원하겠다"며 "비급여 사용 현황을 모니터링해 제도가 안정적으로 정착되도록 하겠다"고 밝혔다.
이남희 식약처 의료기기안전국장은 "AI 등 혁신 의료기기의 시장 진출 애로를 해소하는 동시에, 강화된 임상평가를 통해 안전성 확보에도 만전을 기하겠다"고 말했다.

