미국 진입 목표로 임상 2상 및 FDA Pre IND 준비
케어젠(대표 정용지)은 자사가 개발 중인 안구건조증 치료제 후보물질 'CG-T1'에 대해 미국, 유럽연합(EU), 중국, 브라질, 러시아 등 약 31개국에 물질 특허를 출원했다고 16일 밝혔다.
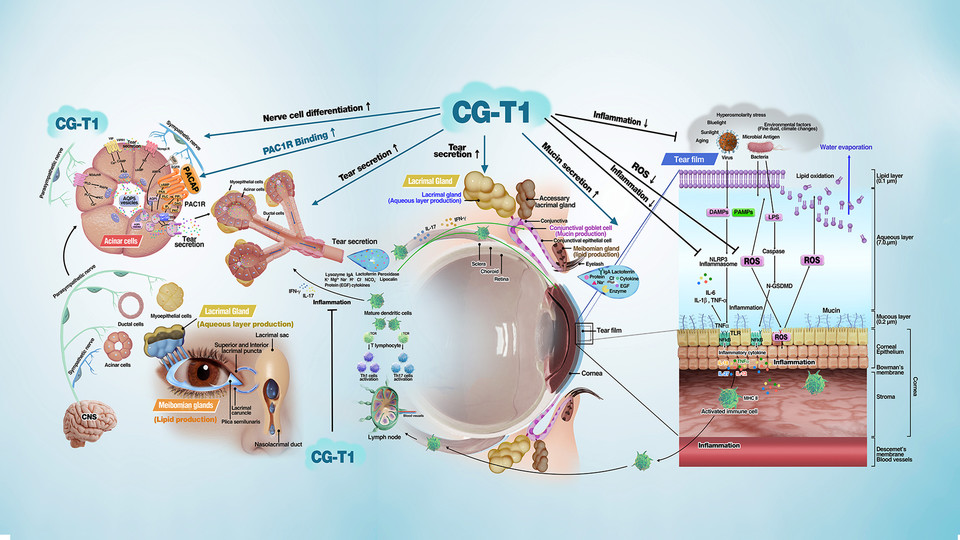
CG-T1은 눈물 분비 저하, 눈물막 불안정, 각막 및 결막 염증 등 안구건조증의 핵심 병태를 동시에 겨냥하는 펩타이드기반 점안제 후보물질로, PAC1 수용체(PAC1R)를 직접 타깃한다.
회사에 따르면 CG-T1은 현재 전임상 연구를 완료하고 데이터 분석 단계에 있다. 회사는 전임상 결과에서 안구건조증과 직접적으로 연관된 주요 지표 전반에서 유의미한 효능 신호가 확인됐다. 또한 기전 검증과 안전성 평가 데이터도 축적돼 임상 단계 진입을 위한 과학적 근거를 충분히 확보했다는 입장이다.
이를 바탕으로 미국 FDA 제출을 목표로 한 임상시험 프로토콜 설계와 함께 임상 2상으로 곧바로 진입하는 전략의 미국 FDA Pre IND 절차도 준비 중이라고 밝혔다.
정용지 대표는 "CG-T1은 눈물 분비와 눈물막 안정화, 안구 표면 보호라는 생리적 신호를 동시에 회복시키는 새로운 접근"이라며 "안구 표면 환경을 정상화함으로써 질환 진행 자체를 구조적으로 줄일 수 있는 잠재력을 가진 물질"이라고 말했다.
한편 회사는 내년 1분기 중 임상 2상에 본격적으로 진입해 안구건조증 환자 대상 안전성 및 유효성, 용량 반응을 중심으로 임상적 유의성 검증에 나설 계획이다.
관련기사
- 케어젠, 이란 BIOA와 코글루타이드 공급 계약 체결
- 케어젠, 필리핀 유통기업과 먹는 비만치료제 공급 계약
- 케어젠, 점안제 개발 섣부른 임상 결과 발표 "시장 혼란 키웠다"
- 케어젠, 브라질 'BCMED'와 5620만달러 건기식 3종 공급 계약
- 케어젠, 독일 의료기기 전시회 'MEDICA 2025' 참가
- 케어젠 '코글루타이드', FDA 기능성원료 등록 신청
- [실적] 케어젠, 3분기 매출은 감소했지만 영업이익은 증가
- 케어젠, 황반변성 점안제 임상 1상서 안전성·유효성 확인
- 케어젠, GLP-1 유사체 '코글루타이드' 美 FDA NDI 등재
- 케어젠, CG-P5, 습성 황반변성 임상 OCT 정밀 분석결과 공개
김동우 기자
glenn@hitnews.co.kr
뉴스, 그 이상의 이야기를 담겠습니다.

