국회, 약제성과평가 제도 체계화 계획 질의
심평원, 약제·질환별 레지스트리 구축 등 체계 정립할 시점

주요국에서 희귀·중증질환 약제의 성과평가를 위한 조직 및 인력을 확대하는 추세인 것으로 나타났다.
건강보험심사평가원은 국회 보건복지위원회 이주영 의원이 질의한 '고가 중증‧희귀질환 치료제 급증에 따른 약제성과평가 제도의 체계적 정립 필요성 및 이에 대한 계획'에 대해 전문성을 갖춘 전담 인력을 확충하고 효율적이고 신뢰성 높은 제도를 운영하겠다고 답변했다.
심평원 약제성과평가실에 따르면 영국과 네덜란드, 프랑스, 대만 등이 희귀 중증질환 약제의 조건부 임시급여 관리제도를 운영하고 있다.
영국은 비용-효과 가능성이 있으나 임상적 유용성이 불확실한 희귀‧중증(항암)질환 약제를 대상으로, 네덜란드는 EMA 등록 희귀의약품, 미 충족 의료 수요가 있는 약제, 프랑스는 중증, 희귀 또는 장애 유발 질환에 대한 혁신약제로 미 충족 의료 수요가 있는 약제, 대만은 비용-효과의 가능성이 있으나 임상적 유용성이 불확실한 희귀‧중증(항암)질환 약제가 대상이다.
이들은 등재 후 사후평가를 조건으로 임시 급여해 환자의 접근성을 보장하고 있다고 심평원은 설명했다.
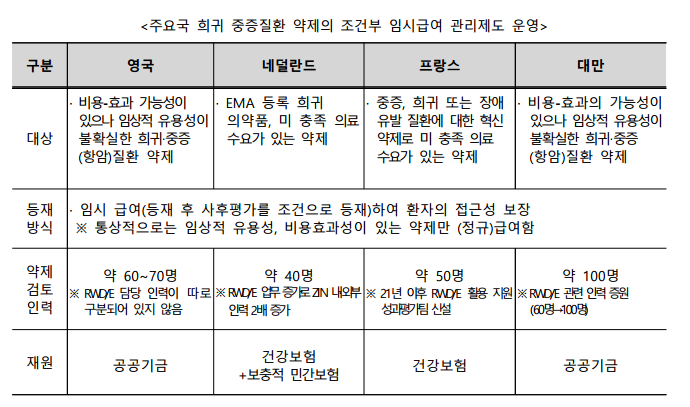
또한 약제검토 인력은 영국이 약 60~70명, 네덜란드는 약 40명, 프랑스는 약 50명, 대만은 약 100명에 이르는 것으로 파악됐다. 네덜란드는 RWD/E 업무 증가로 ZIN 내·외부 인력이 2배 증가했고, 프랑스는 2021년 이후 RWD/E 활용 지원 성과평가팀 신설했다. 대만은 RWD/E 관련 인력을 60명에서 100명으로 증원했다.
심평원 약제평가실은 "최근 허가‧등재되는 신약 중 임상근거가 불확실한 희귀‧중증질환 약제가 과반을 차지해 성과평가 필요 대상 약제가 급증하고 있다"며 "약제성과평가 제도를 체계적으로 정립 할 시점"이라고 밝혔다.
실제 최근 신약 중 위험분담 약제 비율은 2022년 35%(7개)에서 2024년 50%(16개)로 늘었다.
평가실은 "구체적으로 임상자료 등 외부 실제자료인 RWD 수집, 청구‧심사자료와 연계를 통한 약제별‧질환별 레지스트리 구축, 효율적 관리를 위한 IT 인프라의 운영이 요구"된다며 "현재 임시조직(TF)에서 정규조직으로 전환해 체계적인 관리가 필요하다"고 말했다.
이어 "정부와 협의해 전문성을 갖춘 전담인력과 조직을 확충하고, 효율적이고 신뢰성 높은 제도를 운영하는데 노력하겠다"고 덧붙였다.

