복지부, 신의료기술평가에 관한 규칙 개정안 입법예고
보건복지부(장관 조규홍)는 선진입 의료기술의 안전관리 강화·신의료기술의 재평가 근거 규정 마련 및 평가유예 기술의 기간 연장 등을 위한 내용의 '신의료기술평가에 관한 규칙' 일부개정안을 29일부터 오는 12월 9일까지 입법예고한다고 밝혔다.
새로운 의료기술의 임상 현장에서의 안전성과 유효성을 평가하는 신의료기술평가 제도는 평가 이전에도 안전성이 인정된 신의료기술에 한해 선진입 제도들을 통해 의료 현장에서 사용하며 임상근거를 만들 수 있다. 선진입 제도는 안전성이 인정된 신의료기술 중 신속히 사용할 필요가 있거나, 잠재성이 인정되거나, 비침습적 진단 검사 중 임상시험 자료가 있는 경우 정해진 사용 기간·의료 기관에서 사용하며 임상 근거를 만드는 제도로 '제한적 의료기술 평가', '평가유예 신의료기술', '혁신의료기술 평가' 등이 있다.
그동안 의료계와 시민단체 등에서는 안전성을 높여 달라고, 산업계는 사용 기간과 대상을 넓혀 달라고 요구해왔다. 복지부는 △바이오헬스 신시장 창출 전략 회의(’23.2.), △규제 혁신전략회의(’23.3.) 등에서 발굴한 혁신방안과 △선진입-후평가 제도개선 공청회(’23.8.)에서 논의된 내용을 반영해 선진입 기술의 안전성 강화와 기업의 시장진입 활성화를 동시에 달성하기 위한 규칙 개정안을 입법 예고했다.
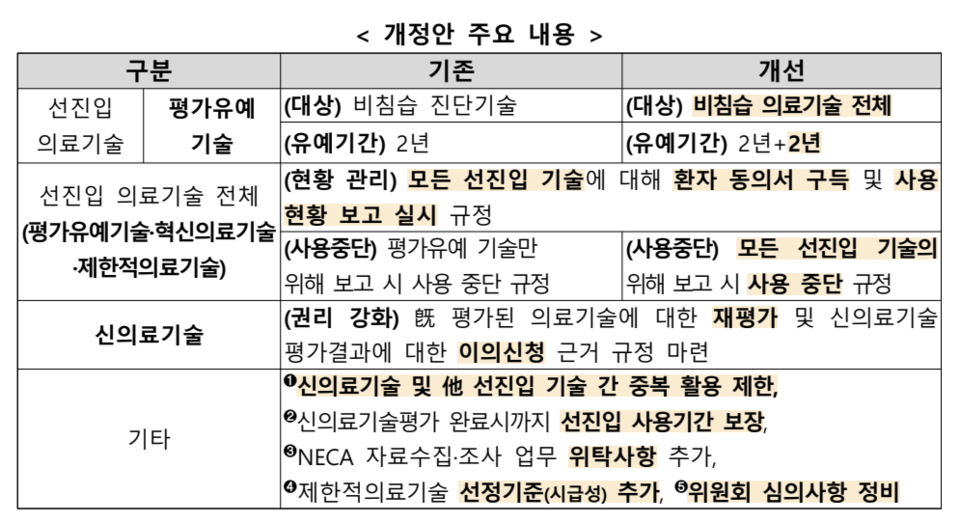
안전성을 확보하기 위해 환자 동의서 작성과 사용 현황 보고를 강화했으며, 평가위원회가 위해 수준이 높다고 보고한 선진입 기술은 퇴출되도록 했다. 시장 진입 확대를 위한 가장 큰 변화는 신의료기술평가 유예 제도의 대상과 기간을 넓힌 것이다. 기존 '비침습적 진단 기술'에서 '비침습적 의료기술' 전체로 확대했으며, 유예 기간을 '2+2년'으로 했다. 안전성 강화 및 유예 기간 기간 확대 모두 형평성을 고려해 규칙 개정 이전 사용 중인 기술에도 소급 적용했다.
복지부 김국일 보건의료정책관은 "지난 2022년 신의료기술평가에 관한 규칙 개정 이후 의료계·산업계·시민단체 등이 제기한 의견과 현장의 애로사항을 반영하여 이번 제도개선안을 마련했다"며 "선진입 의료기술의 안전성 관리를 강화하면서도 우수한 기술을 시장에서 신속하게 활용할 수 있게 될 것이라 기대한다"고 밝혔다.
의료기기산업협회 보험위원회 임재준 부위원장은 "선진입 의료기술 제도는 임상 근거를 만들기 위한 절차이지만 임상 디자인을 만드는데만 최소 6개월에서 1년이 소요 된다"며 "2년은 너무 짧아 지속적으로 개선을 요구해왔다"고 설명했다.
그는 "비침습적 의료기술로 확대하면서 디지털치료기기도 유예를 받을 수 있겠으나 작년 12월에 발표된 디지털치료기기 임시등재 지침에서 유예 제도는 대상이 아니기 때문에 처방료·효과 평가료를 받을 수 있는지 확인이 필요하다"는 의견을 밝혔다. 기업들에게는 "정부가 기업의 재량을 인정해준 만큼 근거 창출을 위해 보다 많은 노력을 기울여야한다"고 당부했다.
관련기사
- "신의료기술평가 이중규제 아냐...신약에도 도입해야"
- 첨단디지털의료기기, 낮은 임시 등재 가격에 통합심사 회피
- "혁신의료기기 선진입 필요하나 환자 안전·근거 신뢰도 중요"
- 신의료기술 통과율 23%… "허가 후 RWD로 평가 어떤가"
- 복지부·NECA, '신의료기술 선진입-후평가 제도개선' 공청회 30일 개최
- "의료기술, 시장 즉시진입 가능하다는데 유예와 다른점 뭔가"
- 시장 즉시진입 가능한 의료기술 제도로 CRO 역할 넓어진다
- 2024년 제4차 ‘신의료기술평가 길라잡이 서비스’ 모집
- 이모코그, 코그테라 독일 DiGA 인증 과정 공유
- DTx '슬립큐' 임시등재에도 비급여로 판매 계획
- 식약처, 이명 디지털치료기기 소리클리어 허가
- "소리클리어, 혁신의료기기 통합아닌 일반심사 택했다"

