종근당, JW신약 등 주블리아 후발약 허가 …9월 출시 예고
다이이찌산쿄, MSD 공동 개발 ADC 'I-DXd' …소세포폐암 대상 3상 승인
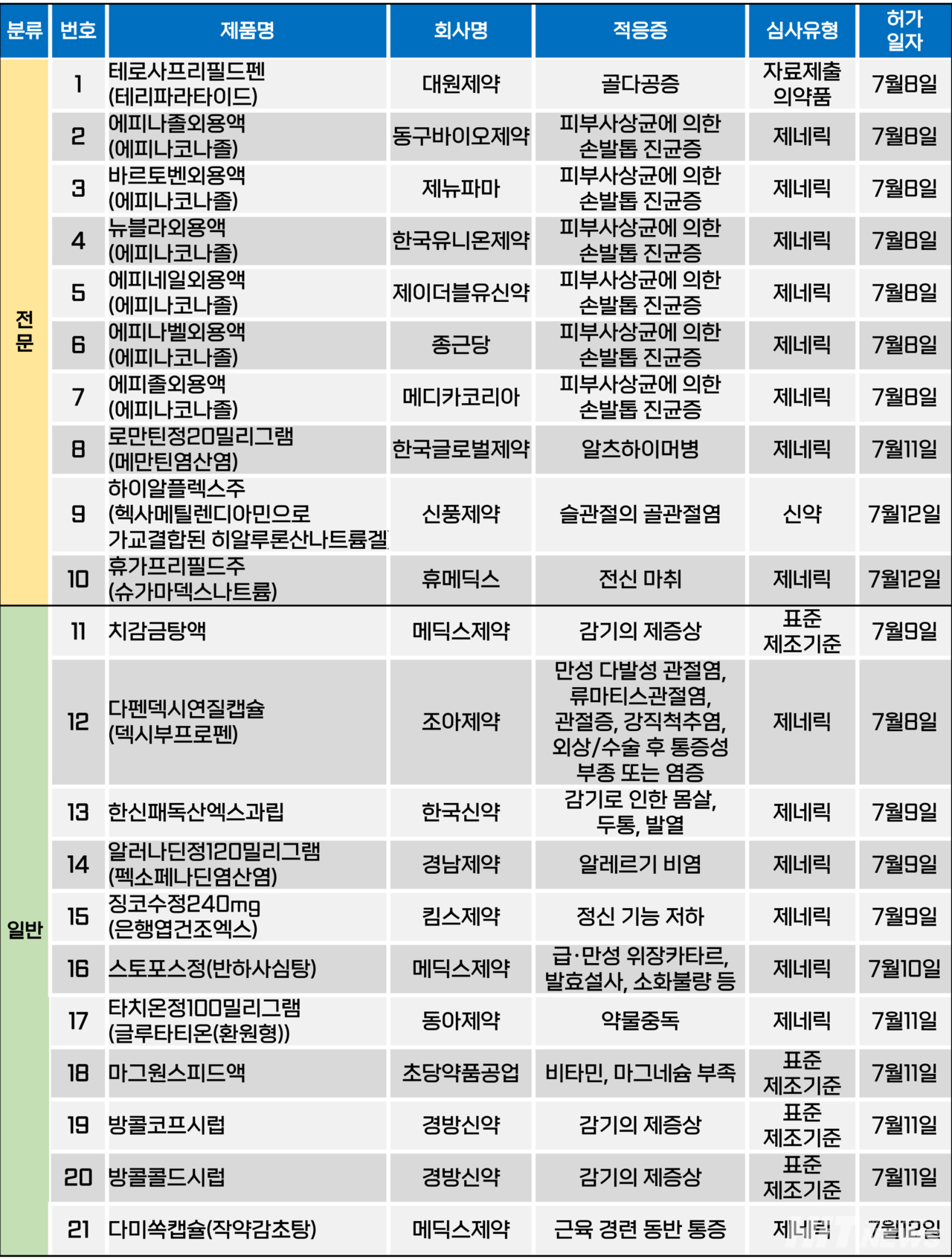
지난주(7월 8~12일) 총 21개 품목이 식품의약품안전처로부터 품목허가를 받았다. 전문의약품은 10개 품목, 일반의약품은 11개 품목이다. 이들은 골다공증, 손발톱 진균증, 알츠하이머병, 골관절염 등 다양한 적응증으로 허가됐다.
동아ST가 개발한 손·발톱무좀 치료제 '주블리아(성분 에피나코나졸)'의 후발약이 연이어 허가되고 있다.
식약처는 지난 8일 △에피나졸외용액(동구바이오제약) △바르토벤외용액(제뉴파마) △뉴블라외용액(한국유니온제약) △에피네일외용액(JW신약) △에피나벨외용액(종근당) △에피졸외용액(메디카코리아) 등 6개 품목이 허가됐다고 밝혔다. 해당 품목들은 모두 '피부사상균에 의한 손발톱 진균증'을 적응증으로 허가됐다.
에피나코나졸 성분 오리지널은 주블리아다. 동아ST는 2016년 주블리아의 원개발사인 일본 카겐제약과 국내 판권 계약을 맺었으며, 2017년 5월 16일 국내 허가 받았다. 이후 전문의약품임에도 환자 접근성이 중요한 무좀약 분야에서 유효성, 안전성 등에서 일반의약품 대비 유의미한 개선을 입증하며 경쟁력을 입증해왔다. 시장 조사기관 유비스트 기준, 작년 주블리아의 원외처방액 규모는 약 290억원이었다.
이후 2023년 2월 이후부터 △대웅제약 △동화약품 △동국제약 △제뉴원사이언스 △제뉴파마 △종근당 △JW신약 △메디카코리아 △명문제약 △오스코리아제약 △한국유니온제약 △동구바이오제약 △한국파마 △마더스제약 △비보존제약 △팜젠사이언스 등이 제품 특허를 회피하기 위한 소극적 권리범위확인심판을 청구했고, 이후 특허를 피했다는 '청구성립' 심결을 받았다.
이후 지난 2월 21일 대웅제약의 '주플리에외용액'을 시작으로, 4월 29일 휴온스 '에피러쉬외용액', 7월 5일 오스코리아제약 '에피니아외용액' 및 제뉴원사이언스 '케이졸외용액' 등 품목이 허가를 받았고, 이번 허가로 국내 에피나코나졸 성분 제제는 총 11개가 됐다.
각 후발 주자들이 오는 9월까지 자사 제품을 출시할 것으로 예상되면서 오는 4분기부터 기존 시장을 지키려는 오리지널과 이를 공략하기 위해 나선 제네릭들의 본격적인 경쟁이 시작될 것으로 보인다.
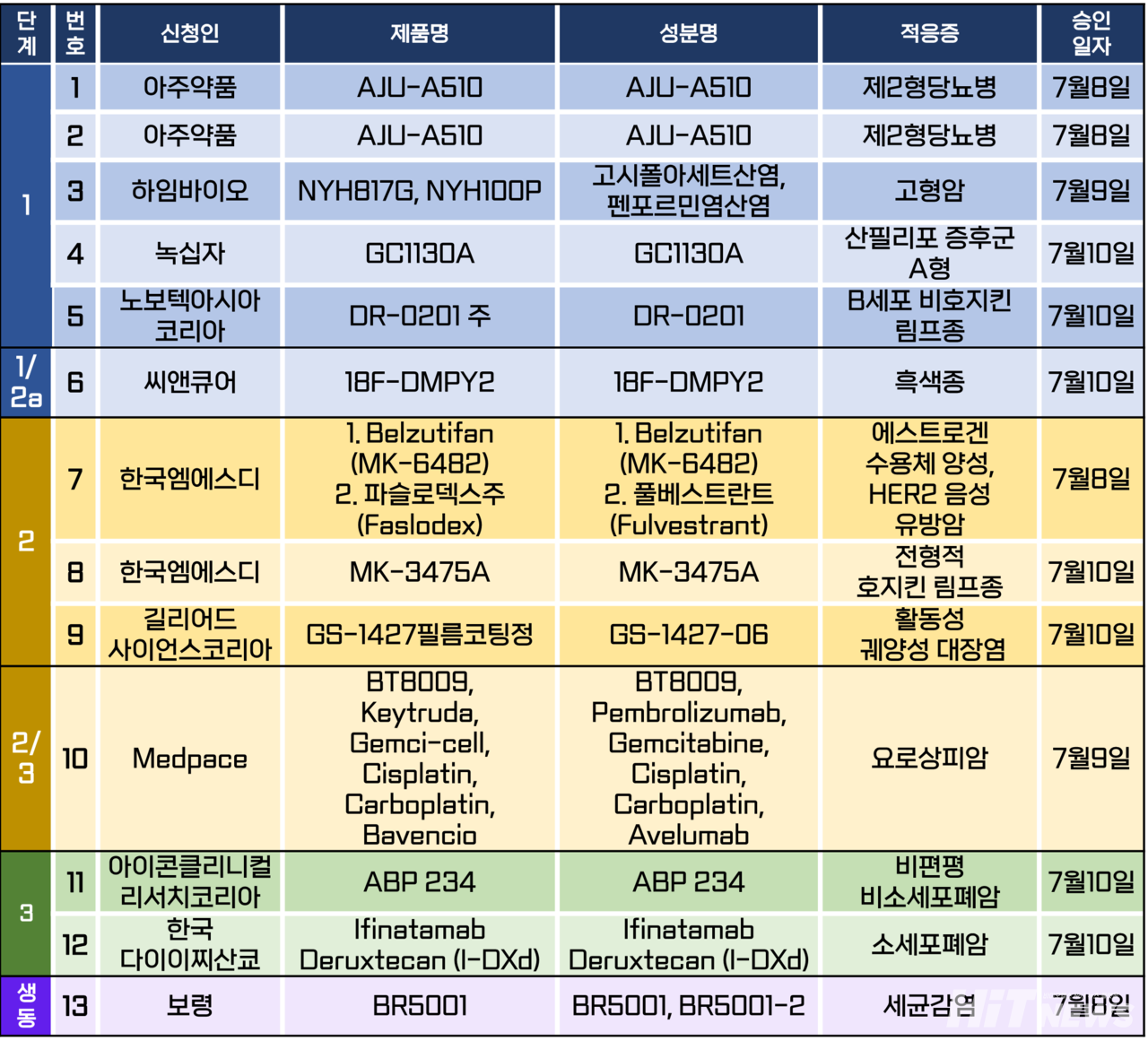
임상시험계획은 총 13건이 승인됐다. 세부적으로 △1상 5건 △1/2a상 1건 △2상 3건 △2/3상 1건 △3상 2건 △생물학적 동등성 1건 등이다. 이 임상시험들은 제2형당뇨병, 사닢ㄹ리포 증후군 A형, 활동성 궤양성 대장염 등 질환과 B세포 비호지킨 림프종, 호지킨 림프종, 흑색종, 유방암, 요로세포암, 비소세포폐암, 소세포폐암 등 암종을 대상으로 승인됐다.
다이이찌산쿄와 MSD가 개발하고 있는 항체약물접합체(Antibody Drug ConjugateㆍADC) 치료제 '이파나타맙 데룩스테칸(Ifinatamab DeruxtecanㆍI-DXd)'의 소세포폐암 대상 3상 임상시험계획이 지난 10일 승인됐다.
이번 3상 임상은 재발성 소세포폐암(SCLC)을 가진 환자에서 B7-H3 타깃 ADC인 I-DXd 대비 의사가 선택한 요법(TPC)의 안전성 및 유효성을 비교하기 위한 다기관, 무작위배정, 공개 연구(연구명 IDeate Lung02)다. B7-H3는 체내 면역세포 활성화에 관여하는 것으로 알려진 단백질이며, 이번 연구의 TPC는 토포테칸, 러비넥테딘, 암루비신 등이다.
연구진은 47명(글로벌 468명)의 환자 참여를 목표로 △삼성서울병원 △서울대병원 △서울아산병원 △분당서울대병원△국립암센터 △연세대 의대 세브란스병원 △칠곡경북대병원 △충북대병원 △가톨릭대 성빈센트병원 △아주대병원 등 의료기관에서 오는 2029년 2월까지 임상시험을 진행할 예정이다.
연구의 일차유효성평가변수는 △독립 중앙 맹검평가(Blinded Independent Central Review·BICR)에 의해 평가된 객관적반응률(ORR) 시험대상자의 수 △전체생존(OS) 등이다.
한편, 다이이찌산쿄와 MSD는 작년 10월 이파나타맙 데룩스테칸을 포함한 3종의 ADC에 대한 글로벌 개발ㆍ상업화 계약을 체결한 바 있다. 계약금(Upfront)은 40억달러, 전체 계약 규모는 220억달러였다.
이 계약으로 양사는 다이이찌산쿄의 △'파트리투맙 데룩스테칸(Patritumab DeruxtecanㆍHER3-DXd)' △'이피나타맙 데룩스테칸(Ifinatamab DeruxtecanㆍI-DXd) △'라루도타턱 데룩스테칸(Raludotatug DeruxtecanㆍR-DXd) 등 3종의 ADC를 공동 개발 및 상업화한다. MSD는 일본을 제외한 세계 지역에 대한 상업화 권리를 가지게 되고, 일본에 대한 상업화 권리는 다이이찌산쿄가 보유한다.

