작년 한국망막학회 설문, nAMD 1차 치료 아일리아 선호도 88%
환자 상태, 사용 경험, 안전성 등 의사 선호 차이 존재
국내 망막 분야 전문의들이 가장 선호하는 신생혈관성 연령 관련 황반변성(nAMD) 1차 치료 약제로 자리하고 있는 '아일리아(성분 에플리버셉트)'의 지위가 경쟁제품인 '바비스모(성분 파리시맙)' 출시 이후 어떤 변화가 있을지 관심을 모은다.
작년 한국망막학회가 총 125명의 회원을 대상으로 진행한 nAMD 치료 선호도 및 트렌드(PAT) 설문조사 결과, 약 88%의 전문의가 nAMD 1차 선호 약제로 아일리아를 꼽았다. 루센티스(성분 라니비주맙)가 10.4%, 비오뷰(성분 브롤루시주맙) 1.6%로 그 뒤를 이었다. 또, 아일리아를 사용하는 전문의 중 90% 이상이 16주까지 투여 간격을 조정할 수 있는 T&E(Treat-and-extend) 요법을 가장 많이 적용하고 있는 것으로 나타났다.
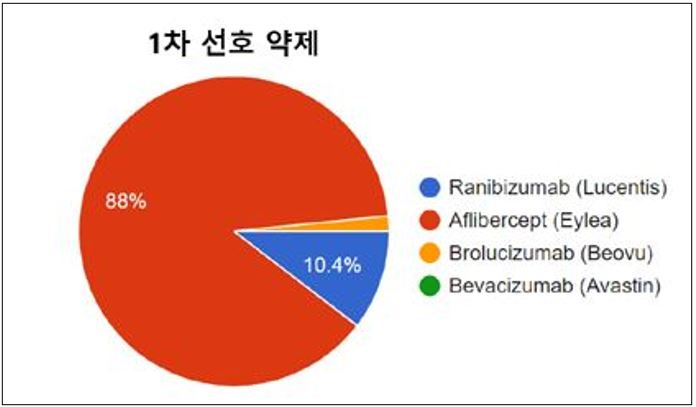
다만, 이 결과에 바비스모는 포함되지 않았다. 작년 10월 보험급여 등재된 이후부터 본격적인 처방이 이뤄지고 있기 때문이다. 이에 올해 조사될 설문에서 아일리아의 점유율에 변동이 있을 것이라는 전망이 나오고 있다.
바비스모는 항-혈관내피세포성장인자(Anti-Vascular Endothelial Growth Factorㆍ이하 anti-VEGF)만을 타깃하는 아일리아와 달리 안지오포이에틴-2(Ang-2)도 함께 타깃하는 이중특이항체로, 아일리아 2mg 제제와의 비교 3상 임상시험을 통해 비열등성을 입증했다.
한 국내 대형병원 안과 전문의는 "아일리아는 이미 국내에서 사용된 지 10년이 넘었고, 장기간의 안전성 데이터도 확보하고 있다. 그만큼 의료진들에게 친숙하고, 충분히 신뢰가 쌓여 있다는 것"이라며 "nAMD 1차 치료제 선택 선호도 변화가 일부 있을 것으로 예상되지만, 실제 임상 환경에서 충분한 안전성 데이터가 쌓일 때까지는 큰 추세 변화는 없을 것으로 판단한다"고 말했다.
이어 "다만, 아일리아를 비롯한 기존 치료제에 효과적으로 반응하지 않거나 반응이 없을 것으로 예상되는 환자들을 위한 추가적인 치료 옵션의 필요성에 대한 의료진의 수요가 존재해 왔다"며 "바비스모가 급여 등재되면서 그 부분이 채워진 점에 대해서는 긍정적으로 판단한다. 바비스모를 1차 치료에 사용하는 것을 선호하는 의사도 상당수 존재할 것"이라고 덧붙였다.
바비스모는 3상 임상에서 아일리아 대비 더 큰 황반중심두께(CST) 및 망막삼출물 감소를 보인 것으로 나타났는데, 이 부분에 주목해야 한다는 의료진도 존재했다.
대학병원 안과에서 근무 중인 이 전문의는 "DME 환자 대상 임상이긴 하지만, 바비스모가 아일리아 대비 유의미하게 황반중심두께와 망막삼출물 감소를 보인 것을 미뤄볼 때 nAMD에 있어서도 장점으로 작용할 수 있을 것"이라며 "황반변성 정도가 더 심한 nAMD 환자에게서 바비스모의 사용을 고려할 수 있을 것 같다"고 설명했다.
한편 최대 투여 기간이 16주로 동일한 아일리아 2mg 제제와 바비스모 6mg 제제의 점유율 경쟁이 진행중인 가운데, 바이엘코리아는 지난 4월 고용량 아일리아를 허가 받으며 격차 벌리기에 나섰다.
기존 제품의 고용량 버전인 아일리아 8mg 제제는 용량이 늘어난 만큼 T&E 요법을 통해 최대 투여 기간을 20주까지 늘릴 수 있도록 허가됐다. 기존 2mg 제제와 비교 임상으로 진행한 3상 임상에서 유효성에 대한 비열등성, 유사한 안전성을 확인했다.

지난 28일 진행된 '아일리아 고용량 허가 기념 간담회'에서 김재휘 한국망막학회 미래이사는 "아일리아 8mg 제제는 3상 임상을 통해 참여 환자 중 약 38.5%가 최대 20주까지 투여 간격을 연장할 수 있었음을 보였다"며 "안구 주사제의 특성상 투여에 대한 환자의 스트레스는 엄청난데, 투여기간을 기존 대비 4주가량 늘릴 수 있다는 것은 굉장히 큰 장점으로 작용할 것"이라고 말했다.
문귀현 바이엘코리아 의학부 이사는 "조만간 아일리아 투여 후 2년 추적 데이터가 공개될 예정이며, 3년 차부터는 임상명을 변경한 뒤 진행할 것"이라며 "최종적으로는 투여 간격을 24주까지 늘리도록 임상시험이 디자인된 만큼, 향후 좋은 연구 결과가 도출되기를 기대한다"고 전했다.
관련기사
- 황반변성 치료제 '아일리아' 고용량 허가… 투여간격 5개월까지 연장
- "아일리아, 습성황반변성 T&E 요법에 이상적… 맞춤치료 가능"
- 바이엘 지비주와 로슈 바비스모주, 평가금액 아래로 급여등재
- "안과영역 이중특이항체 '바비스모' 미충족수요 해소 기대"
- "이중항체 '바비스모', 중증 황반변성 환자서 활용 기대"
- [허가/임상] 황반변성 치료제 '아일리아' 시밀러 3상 승인
- 바이오시밀러 제일 먼저 낸 삼성바이오에피스 '약가 알박기'
- Samsung Bioepis Sets New Pricing Benchmark with Afilivu
- 망막질환 치료제 '아일리아' 고용량 내달부터 급여 적용
- 로슈, 바비스모 급여 1주년 국내외 의료진과 임상적 가치 논의
- 바비스모, 망막정맥폐쇄성 황반부종 시력손상에 사용
- [허가/임상] 황반변성 치료제 '바비스모', 6개월 간격 요법 3상 승인
- 아일리아 8mg, 최대 5→6개월로 투여 간격 확대 EU 허가 권고
- "바비스모, 이중억제 기전으로 신속ㆍ안전하게 '황반변성' 개선"

