국내 경쟁 치료제 중 투여 간격 6개월로 가장 길어
저용량으로 장기 약효 지속…"환자 편의성 증대 및 스트레스 감소 기대"
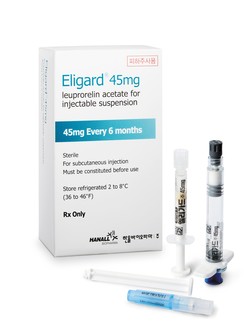
한올바이오파마(공동 대표 박수진·정승원)는 식품의약품안전처로부터 전립선암 치료제 '엘리가드주 45㎎'의 적응증으로 진성 성조숙증(Central Precocious Puberty·CPP)을 추가로 승인받았다고 11일 밝혔다.
이번 승인으로 엘리가드는 진성 성조숙증 진단을 받은 만 9세 미만 여아 및 만 10세 미만 남아의 치료에 사용될 수 있게 됐다. 엘리가드의 개발사 '톨마'는 지난 2020년 미국 식품의약국(FDA)으로부터 해당 적응증에 대한 추가 승인을 받은 바 있다.
성조숙증은 또래의 아이들보다 사춘기 발달이 비정상적으로 빠른 경우를 말한다. 여아의 경우 8세 이전의 유방 발달, 남아의 경우 9세 이전의 고환 크기 증가를 동반한다. 국내에서는 호르몬 검사를 통해 황체형성호르몬(Luteinizing Hormone·LH) 농도가 5IU/ℓ 이상인 경우 성조숙증으로 진단한다. 국내 성조숙증 환자는 2018년 10만명에서 매년 증가해 2022년 약 18만명으로 5년 사이 72% 늘었다.
엘리가드는 몸속에서 서서히 약물을 방출시키는 '중합젤(Ploymeric gel)' 기술이 적용돼 적은 용량(0.375㎖)으로 장기간 약효가 지속되는 것이 특징이다. 특히 국내 동일 성분·동일 적응증의 피하주사제 중에서는 유일하게 투여 간격이 6개월로 길다. 주사 치료를 무서워하거나 병원 방문을 꺼려 하는 아동들의 스트레스 감소에 도움이 될 것이라는 게 회사 측 설명이다.
박수진 한올바이오파마 대표는 "엘리가드는 2010년 국내 출시 이후 2021년 매출 100억을 달성하며 블록버스터 의약품으로 성장한 제품"이라며 "입증된 임상적 효능 및 안전성과 더불어 긍정적인 의학적 평가를 받아온 만큼 국내에서 성조숙증 환자들에게 새로운 치료 옵션으로 자리매김할 것으로 기대된다"고 말했다.
관련기사
- [허가/임상] SK케미칼 '수벡스' 허가, '펙수클루' 헬리코박터 제균 3상
- 한올바이오, 국내외 인재확보 프로그램 운영 눈길
- 한올바이오파마, 2분기 매출액 414억…전년비 58% 증가
- K보툴리눔 기업들은 언제쯤 보톡스를 따라 잡을 수 있을까
- 한올바이오 "자가면역질환 신약 후보 HL161, 中 품목허가 신청"
- 한올바이오 "자가면역질환 치료제 'HL161ANS', 1상 초기 결과 발표"
- 한올바이오파마, 美 파트너 항체신약 임상 1상 데이터 공개에 상한가
- 한올·대웅제약·뉴론 "파킨슨병 치료제, 임상 1상서 첫 환자 투약"
- 한올바이오파마 "3분기 매출액 330억 달성"

