[ASCO 2023] MSD, 키트루다 보조요법 대조군 대비 EFS 위험 42% 감소
"OS, 통계적으로 유의미한 중간값 도달 못해…지속 시험해 나갈 것"
"하위그룹 분석서 PD-L1 발현 정도 관계 없이 유의미한 EFS 개선 보여"
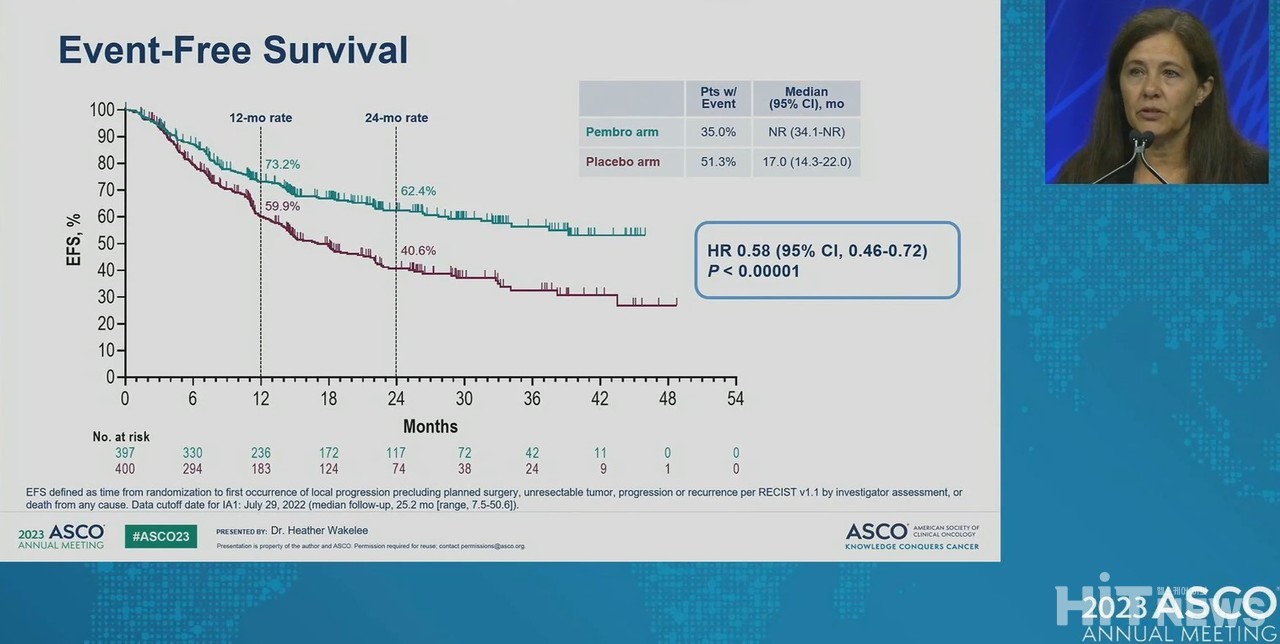
미국 머크(MSD)의 면역항암제 '키트루다(성분 펨브롤리주맙)'를 절제 가능한 2기, 3A기 또는 3B기 비소세포폐암(NSCLC) 환자의 수술 전·후 보조요법으로 사용한 결과, 대조군인 항암화학요법(수술 전 보조요법) 및 위약(수술 후 보조요법) 병용요법에 비해 재발, 진행 또는 사망 위험이 42% 낮아졌다는 연구 결과가 발표됐다.
지난 3일(현지 시각) 진행된 미국임상종양학회(ASCO) 2023 연례학술회의에서 헤더 웨이클리(Heather Wakelee) 미국 스탠포드대 의과대학 흉부종양학과 교수(세계폐암학회(IASLC) 회장)는 현재 MSD가 진행 중인 'KEYNOTE-671'의 임상3상 결과를 발표했다.
KEYNOTE-671 연구는 절제 가능한 2기, 3A기 또는 3B기 NSCLC 환자의 수술 전·후 보조요법으로서 키트루다의 유효성을 평가하기 위한 3상 임상시험이다. 이번 ASCO에서는 1차 유효성 평가변수인 추적관찰 기간 25.2개월(중앙값) 시점의 무사건 생존율(Event-Free SurvivalㆍEFS)과 전체 생존 기간(Overall SurvivalㆍOS) 데이터가 공개됐다.
웨이클리 교수가 공개한 자료에 따르면, 절제 수술 전·후로 키트루다를 단독요법으로 투여한 2기, 3A기 또는 3B기 NSCLC 환자 중 65%에서 진행·질병·사망 등 사건이 발생하지 않았지만, EFS 중앙값에는 도달하지 못했다(95% CI, 34.1개월~도달하지 못함). 대조군인 항암화학요법(수술 전 보조요법) 및 위약(수술 후 보조요법) 투여 환자군에서는 48.7% 환자에서 사건이 발생하지 않았으며, EFS 중앙값은 17.0개월(95% CI, 14.3~22.0개월)로 나타났다. 대조군 대비 EFS 위험비(HR)는 0.58%(95% CI, 0.46~0.72, p<0.00001)로 분석됐는데, 42%만큼 질병의 재발, 진행 또는 사망 위험이 낮아졌다는 뜻이다.
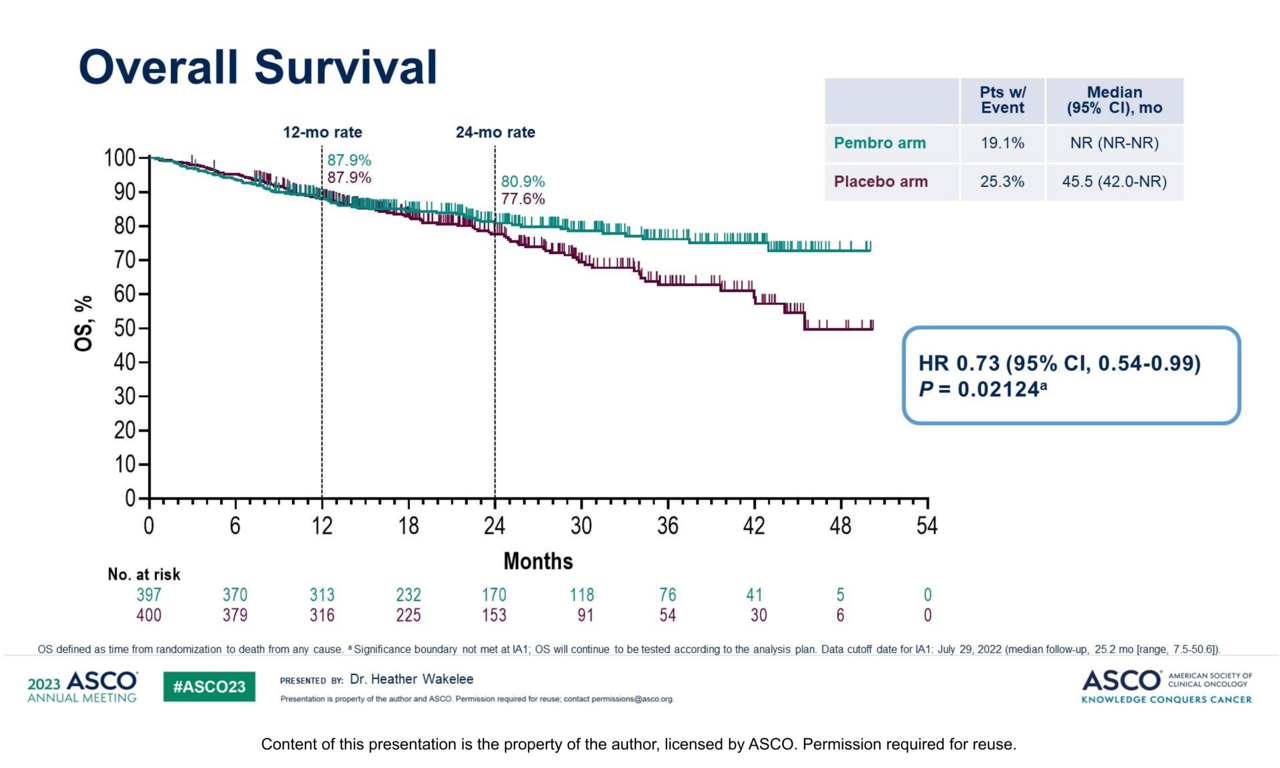
현재까지의 대조군 대비 OS 위험비는 0.73(95% CI, 0.54-0.99, p=0.02124)으로 나타났지만, 통계적으로 유의미한 중간 분석 시점에 도달하지 못한 것으로 확인됐다. 헤더 교수는 "이번 발표에서는 키트루다 투여군의 중간 분석시점 OS에 도달할 수 없었다"며 "남은 연구기간 통계적 분석 계획에 따라 지속적으로 시험해나갈 것"이라고 설명했다.
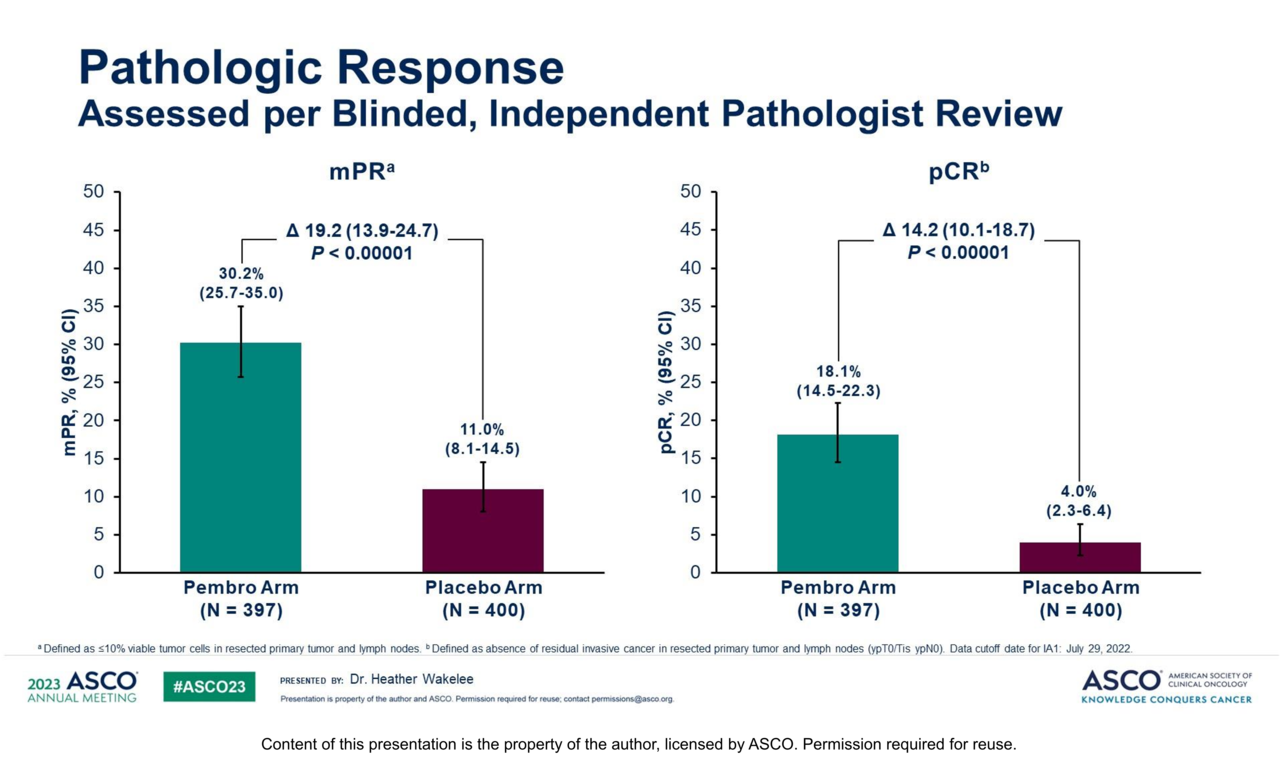
한편 연구진은 주요 2차 유효성 평가변수인 병리학적 완전관해(pCR) 및 주요 병리학적 반응(mPR)에 대해서는 통계적으로 유의미한 결과를 얻었다. mPR은 수술 전·후 종양 세포가 10% 이하로 남은 상태를 말한다.
pCR 도달률은 키트루다 투여군에서 18.1%(95% CI, 14.5~22.3), 대조군에서 4.0%(2.3~6.4)로, 14.2%포인트(95% CI, 10.1-18.7, p<0.00001)의 차이를 보였다. 또 mPR은 키트루다 투여군에서 30.2%(95% CI, 25.7~35.0), 대조군에서 11%(95% CI, 8.1~14.5)로, 19.2%포인트(95% CI, 13.9~24.7, p<0.00001) 차이가 나타났다.
하위그룹 분석에서는 키트루다 보조요법 환자군에서 PD-L1 발현 정도와 관계 없이 유의미한 EFS 위험 개선을 보였다. 세부적으로 PD-L1 발현율 △1% 미만(HR=0.77, 95% CI, 0.55~1.07) △1~49%(HR=0.51, 95% CI, 0.34~0.75) △50% 이상(HR=0.42, 95% CI, 0.28~0.65) 등으로 나타났다.
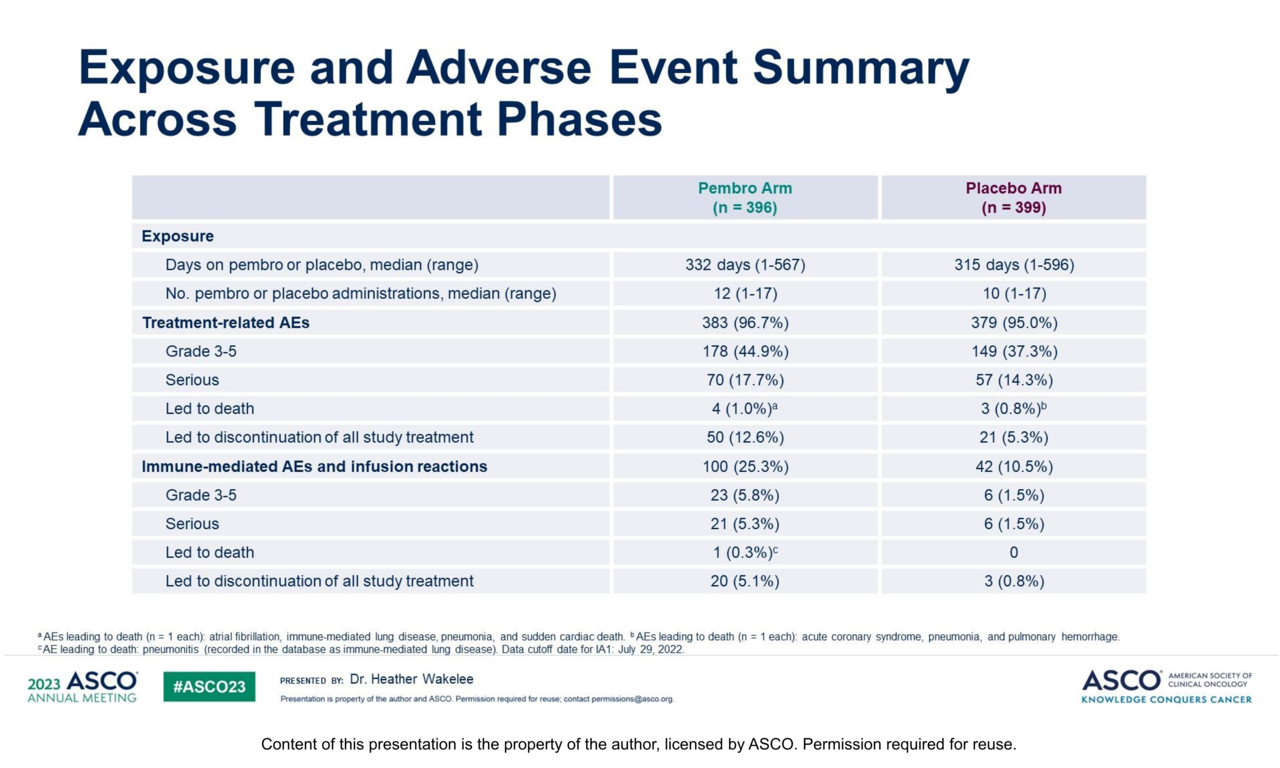
안전성 프로파일은 기존 연구를 통해 밝혀진 데이터와 유사했다. 치료 관련 이상반응(TRAE) 비율은 키트루다 투여군(396명)이 96.7%(383명), 대조군(399명)이 95%(379명)였으며, 3~5등급의 TRAE 비율은 각각 44.9%, 37.3%였다. TRAE로 인한 모든 치료 중단 비율은 키트루다 투여군에서 12.6%, 대조군에서 5.3%였으며, TRAE로 인한 사망비율은 각 1.0%(4명), 0.8%(3명)였다.
면역매개 이상반응(Immune-mediated AE)과 주입반응(Infusion reactions) 발생 비율은키트루다 투여군이 25.3%(100명), 대조군이 10.5%(42명)였다. 3~5등급의 면역매개 이상반응 및 주입반응 비율은 투여군 5.8%, 대조군 1.5%였다.
기존 키트루다 투여군에게서 가장 흔히 발생하는 이상반응으로 나타났던 갑상선기능저하증(Hypothyroidism)은 11.1%로 나타났으며, 면역매개 이상반응과 주입반응으로 인한 사망비율은 키트루다 투여군이 0.3%(1명), 대조군이 0%였다. 이 반응으로 모든 치료를 중단한 비율은 각 5.1%(20명), 0.8%(3명)였다.

