셀트리온제약 청주공장 펜, 프리필드시린지 등 피하주사 완제 생산
AZ, 'DS-1062a' 1~3기 삼중음성 유방암 대상 추가 적응증 임상 승인
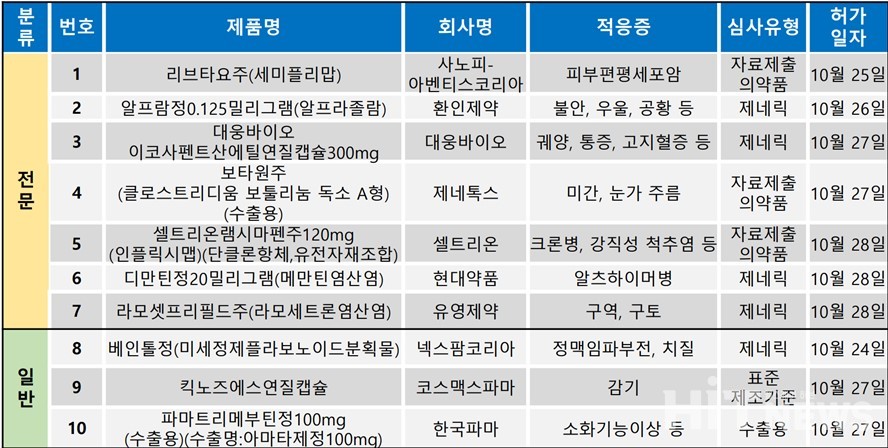
지난 주(10월 24일~10월 30일)에는 총 10개 품목이 식품의약품안전처로부터 품목허가를 받았다. 이 중 전문의약품은 7건, 일반의약품은 3건이었다.
이번 허가 전문의약품들은 피부편평세포암, 크론병, 강직성 척추염, 알츠하이머병, 제2형당뇨병 등 적응증이 주를 이뤘다.
셀트리온은 지난 28일 램시마SC(피하주사) 시리즈 중 펜타입 '셀트리온램시마펜주120mg'의 국내 품목허가를 획득했다. 램시마SC는 기존 정맥주사 제형의 램시마주의 투여 경로를 피하주사 형태로 변경한 제형으로, 프리필드 타입과 펜 타입이 있다.
회사는 지난 2020년 10월 12일 동일 제제(램시마펜주120mg)에 대한 수입품목허가를 획득해 미국과 독일로부터 수입해 왔다. 이 피하투여 제제들은 2019년 11월 유럽 EMA로부터 판매 승인됐다.
최초 국내 허가 당시 류마티스 관절염 적응증으로 허가됐으나, 점차 궤양성 대장염, 강직성 척추염, 성인 크론병 등으로 그 범위를 확대해 갔다.
램시마SC의 국내 제조품목허가는 이번이 처음이 아니다. 지난 3월 7일 회사는 '셀트리온램시마프리필드주시린지주120mg'를 허가받은 바 있다.
회사는 허가 당시 "그 동안 국내에서 품질을 유지하며 램시마SC 완제의약품을 생산할 수 있는 제조소가 없어 해외에서 수입해야만 했다"면서 "셀트리온제약이 생산시설을 완비함에 따라 램시마 SC 완제의약품을 국내에서 생산할 수 있게 됐다"고 밝혔다.
이어 "해외 위탁 생산에 비해 국내 생산을 통해 제조 시간을 절감할 수 있을 것"이라고 덧붙였다.
또한 지난 24일 셀트리온제약은 PDA(국제 세계비경구의약품협회) 전문가들을 초청해 청주공장 PFS(Pre-filled Syringes) 생산시설 투어를 진행하며, 펜(Auto Injector) 1종, 프리필드시린지 2종 등 총 3가지 유형의 피하제형 완제의약품 생산이 가능하다고 밝힌 바 있다.
이 외 희귀의약품의 허가 소식도 있다.
사노피-아벤티스코리아는 지난 25일 미국 리제네론과 함께 개발한 피부편평세포암 치료제 '리브타요(LIBTAYO)'의 희귀의약품 품목허가를 획득했다.
리브타요는 '근치적 수술이나 근치적 방사선 요법의 대상이 아닌 국소 진행성 또는 전이성 피부편평세포암'으로 효능·효과를 허가받았다.
이 의약품은 T세포의 면역관문 수용체인 PD-1(세포 예정사 1, programmed cell death 1)을 표적으로 하는 단클론항체로, 암세포가 PD-1을 이용해 T세포를 회피하는 기전을 차단해 면역세포가 암세포를 공격·제거할 수 있도록 돕는 작용 기전을 가진다.
PD-1은 CD28 계열에 속하는 억제성 면역관문 수용체로, 활성화된 T세포, B세포, NK세포, 골수 계통 세포에서 발현되며, 면역조절에서 중추적인 역할을 수행한다.
현재 리브타요는 미국 FDA(2018년)와 유럽 EMA(2019년)로부터 피부편평세포암 적응증을 획득했다. 이 외에도 양 기관은 기저세포암, 비소세포폐암 적응증에 대한 사용을 승인한 바 있으며, 자궁경부암 적응증은 EMA로부터 승인받았다.
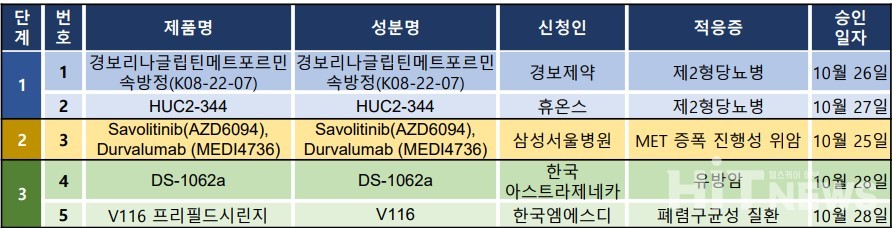
지난주 임상시험계획은 총 5건이 승인 완료됐다. 세부적으로 △임상1상 2건 △2상 1건 △3상 2건 등이다.
이 임상시험들은 유방암, MET 증폭 진행성 위암, 제2형당뇨병, 폐렴구균성 질환 등 다양한 적응증에 대해 승인됐다.
다이이찌산쿄와 아스트라제네카가 공동 개발 중인 TROP2 표적 항체 약물접합체(ADC) 'DS-1062a(성분명 : 다토포타맙 데룩스테칸)'의 삼중 음성 유방암 환자 대상 임상 3상 시험(TROPION Breast03)이 승인됐다.
아스트라제네카는 이번 임상시험계획 적응증을 '선행보조 전신요법 치료 후 절제수술 시 유방 및/또는 액와 림프절에 잔류 침습질환이 존재하던 1~3기 삼중음성 유방암'으로 승인받아 진행한다.
양사는 앞서 3월 '수술 불가능한 국소진행성 또는 전이된 삼중음성 유방암의 1차 선택 치료로서 PD 1/PD L1 저해제 치료 대상이 아닌 환자'를 대상으로도 승인받아 임상 3상을 진행 중이다.
또한 DS-1062a를 유방암 외에도 △비소세포폐암 △자궁내막암 △위암 △거세저항성 전립선암 △난소암 △결장직장암 등 고형암 대상으로 개발 중이다.
양사는 지난 8월 6일 개최된 세계폐암학회(WCLC) 2022에서 키트루다와 다토포타맙 데룩스테칸 병용요법에 대한 최신 임상결과를 발표했다.
크리스티안 마세시 아스트라제네카 최고 의료 책임자는 "진행성 비소세포폐암 환자에게 새롭고 효과적인 치료 옵션을 제공하는 것을 목표로 항체 약물 접합체 연구를 계속하고 있다"고 말했다.
발표된 임상 결과(TROPION-lung02, 08)에 따르면, 회사는 주요 변이 유전자가 없고 이전 치료를 받지 않은 진행성 또는 전이성 비소세포폐암 환자를 대상으로 진행했으며, 키트루다·다포토타맙 병용요법을 투여 받은 환자에서 1차 요법으로 62% 객관적반응율(ORR)을 확인했다.
현재 이 제제는 '표적화가능한 게놈 변화 없는 국소 진행성 또는 전이성 비소세포폐암 환자의 1차 선택 치료' 적응증에 대한 병용투여 임상 3상을 식약처로부터 지난 9월 7일 승인받아 개발 중이다.

