식약처 '2022년 상반기 의약품 허가업무 온라인 설명회'

오는 4월15일부터 전문의약품 생물학적동등성시험(이하 생동시험) 범위 확대에 따라 자료 제출이 요구되는 경구용액제와 시럽제에 대해 이화학적동등성시험(이하 이동)자료 제출이 가능해 진다.
이동시험은 주로 제품 투여 경로나 작용 기전에 따라 생동 시험이 어려운 제형에 대해 진행되는 의약품동등성 시험의 한 종류다.
식품의약품안전처는 22일 '올해 상반기 의약품 허가업무 온라인 설명회'를 개최해 달라지는 허가제도와 연계해 의약품 허가·신고·등록 시 고려해야 할 사항들을 안내했다.
허가총괄담당관 문현주 연구관은 2020년 개정돼 올해 4월 15월부터 개정 시행되는 총리령 '의약품등의 안전에 관한 규칙'에서 전문의약품의 생동시험 제출 범위 확대 내용을 소개했다.
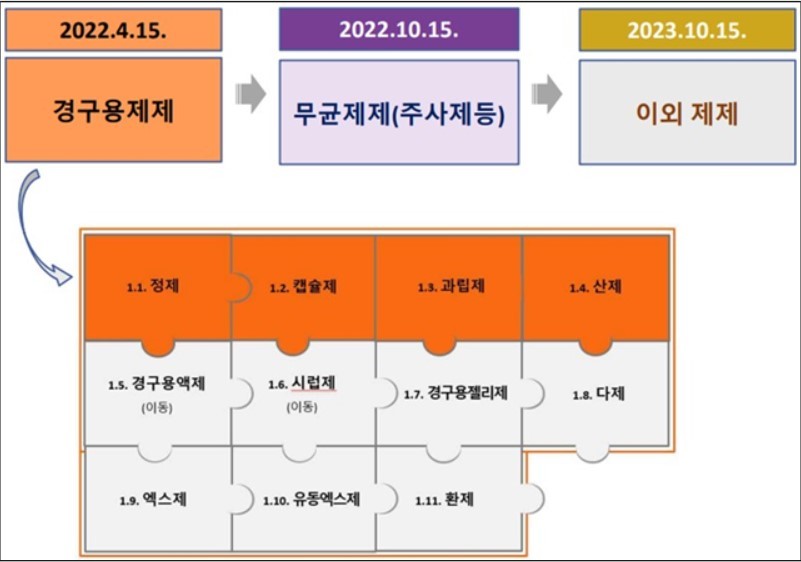
개정된 총리령에 따라 ▷오는 4월 15일부터 경구용제제 ▷오는 10월 15일부터 무균제제(주사제 등) ▷내년 10월 15일부터 이외 제제들에 대한 생동시험 또는 비교임상시험 자료 제출이 의무화된다.
문현주 연구관에 따르면, 현재 생동시험의 자료제출이 의무화된 전문의약품 제형은 정제, 캡슐제, 과립제, 산제 등 4종이다.
이 외 경구용제제인 △경구용액제 △시럽제 △경구용젤리제 △다제 △엑스제 △유동엑스제 △환제 등은 4월 15일부터 생동시험 자료제출이 의무화된다.
다만, 경구용액제와 시럽제는 이동 자료제출이 인정된다. 경구용액제와 시럽제는 식약처 고시인 '의약품 품목허가·신고·심사 규정' 제27조에 이동자료를 제출해도 된다고 명시돼 있기 때문이다.
이번 답변은 그동안 의약품 제조업체 허가 담당자들이 이 두 규정상의 불일치로 다수의 민원을 식약처에 제시해왔었기 때문인 것으로 추측된다.

이 외에도, 문 연구관은 올해 11월 12일에 시행되는 식약처 고시 규정으로 △외국의약품집 관련 자료 면제 규정 삭제 △별표19. CTD로 작성된 품목의 제조방법 변경 시 제출자료 범위 제시 △복합 전문의약품 제품명에 3개 이하 성분 기재 △CTD로 허가 신청 시 제조방법란 기재 △일회용 점안제 포장단위 5mm로 제한 등이 예정돼 있다고 소개했다.

