Kim's Weekly 9월 4주차 의약품 품목허가 임상승인 현황
용량·제형 확대로 시장 방어 나선 제약계
한국얀센 다발골수종 CAR-T 치료제 국내 임상 3상 진입

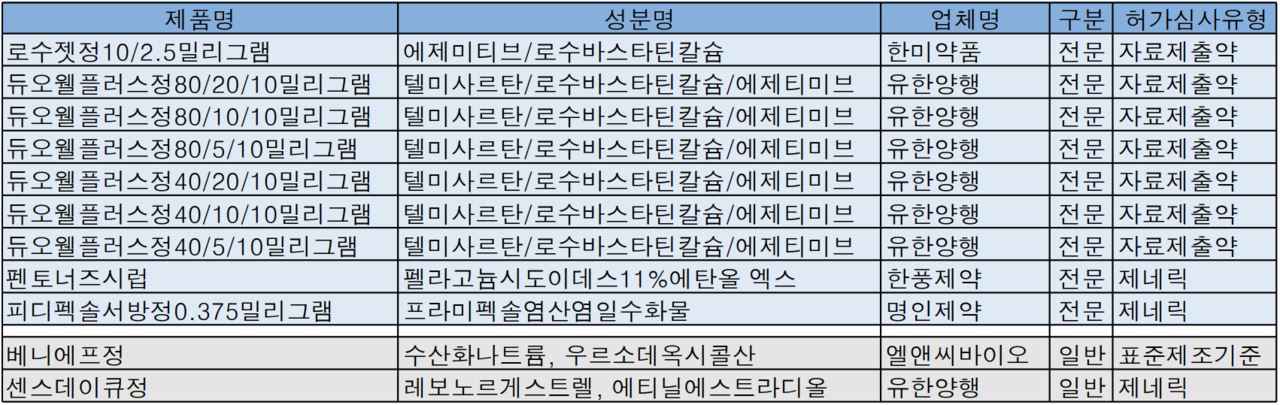
유한양행이 고혈압·고지혈증 3제 복합제 '듀오웰플러스정(텔미사르탄/로수바스타틴칼슘/에제미티브)' 품목허가를 받았다.
한미약품은 고지혈증치료제 로수젯정의 새로운 용량 '로수젯정10/2.5밀리그램(에제미티브/로수바스타틴칼슘)' 품목허가를 획득하며 상반기 534억원 매출을 올린 효자품목의 라인업을 확장했다.
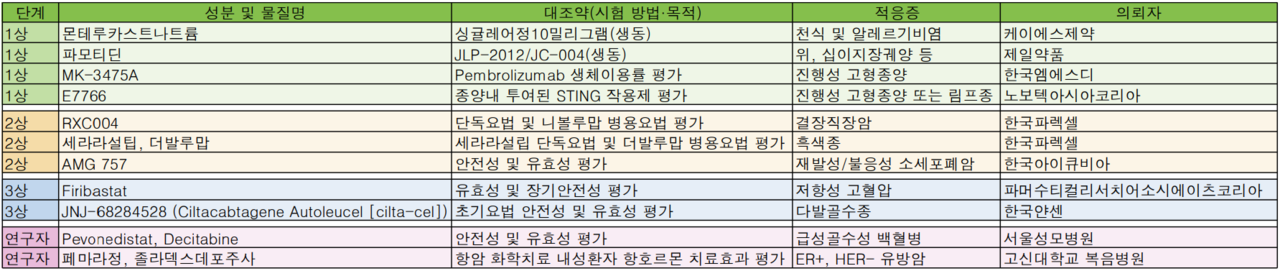
식품의약품안전처는 9월 4주차(2021. 09. 20~2021. 09. 26) 듀오웰플러스정 6개 제형을 포함한 11(전문약: 9개, 일반약: 2개) 품목허가와 11개 임상시험(1상: 4개, 2상: 3개, 3상: 2개, 연구자: 2개)계획을 각각 승인했다.
용량·제형 확대로 시장 방어 나선 제약계
듀오웰플러스정은 기존 텔미사르탄, 로수바스타틴칼슘 복합제에 에제미티브를 추가한 3제 복합제로, 텔미사르탄/로수바스타틴칼슘/에제미티브 6가지 용량(80/20/10, 80/10/10, 80/5/10, 40/20/10, 40/10/10, 40/5/10mg)에 대한 품목허가를 획득했다.
듀오웰플러스정은 텔미사르탄/로수바스타틴칼슘/암로디핀베실산염 3제 복합제 '듀오웰에이정'에 이은 3제 복합제로 작년 듀오웰정 PMS만료 이후 쏟아진 2제 복합제 품목허가 공세에 대한 대응전략으로 파악됐다.
시장 방어 움직임은 용량확대로도 확인되고 있다. 한미약품은 에제미티브/로수바스타틴칼슘 10/2.5mg 용량을 추가함으로써 고지혈증 초기환자로 타깃을 넓혔다.
이밖에도 지난주 유한양행은 피임약 '센시데이큐정'을, 엘앤씨바이오는 변비치료제 '베니에프정'에 대한 품목허가(일반의약품)를 각각 획득했다.
한국얀센 다발골수종 CAR-T 치료제 국내 임상 3상 진입
한국얀센은 CAR-T 치료제 임상시험 3상에 나선다. 대상환자는 새롭게 진단되고 초기 요법으로 조혈모세포 이식이 예정되지 않은 다발골수종 환자로 보르테조밉, 레날리도마이드 및 덱사메타손 (VRd) 이후 BCMA를 표적으로 하는 키메릭 항원 수용체 T 세포(CAR-T) 요법인 실타캅타젠 오토류셀 대 보르테조밉, 레날리도마이드 및 덱사메타손(VRd) 이후 레날리도마이드 및 덱사메타손(Rd) 요법을 비교평가한다. 글로벌임상시험으로 우리나라에서는 서울아산병원, 세브란스병원, 화순전남대병원, 삼성서울병원 등이 참여한다.
임상시험수탁기관 파머수티컬리서치어소시에이츠코리아는 Firibastat에 대한 임상시험 3상을 승인받았다. Firibastat는 퀀텀 지노믹스의 치료하기어려운/저항성 고혈압 치료후보물질로 국내환자 75명(글로벌 전체 750명)을 대상으로 최대 48주동안 장기안전성 및 효과성 평가에 나설 예정이다.
이밖에 케이에스제약은 천식 및 알레르기비염 치료제인 한국MSD 싱귤레어정10밀리그램(몬테루카스트나트륨)과 '케이레어정10mg'에 대한 생물학적 동등성 평가를 진행한다.