검토보고서 통해 임상시험자료 사용 동의횟수 제한 신중해야
식품의약품안전처가 제네릭의약품 관련 생물학적동등성 자료 1+3 적용을 찬성한 것과 달리 자료제출의약품에 대해서는 신중한 접근이 필요하다는 의견을 내놨다.
국회 보건복지위원회 홍형선 수석전문위원의 검토보고서에서 식약처는 임상시험자료를 사용할 수 있는 품목(자료제출의약품)수를 총 4개로 제한하는 것은 의약품 개발을 저해할 우려가 있다고 밝혔다.
생동성자료 횟수 제한 약사법 개정안 찬성 견해를 밝힌 것과 상반된 입장이다.
공동생동 1+3 규제법안은 작년 9월 서영석 의원이 대표발의했다.
개정안은 이미 생동성을 입증한 품목을 제조하는 제조소에 동일한 제조방법으로 위탁제조하고 그 품목의 생동성자료를 이용해(동의서 제출) 허가 신청하는 경우 허가 신청이 가능한 품목을 3개 이내로 제한(안 제31조제12항)하는 내용이다.
당시 검토보고서를 통해 식약처는 위탁제조에 따른 유통 문란과 제품 개발 능력 약화 문제를 해소하고, 제약산업의 경쟁력을 강화할 필요가 있다는 점에서 개정안 입법취지에 공감한다고 밝혔다.
또한 해당 개정안 추진으로 제네릭 난립 억제를 통해 ▲약품의 품질 제고에 영향을 끼쳐 국민의 안전한 의약품 사용 환경을 만드는데 기여하고 ▲제네릭 신뢰 회복을 통한 사용 활성화로 건보재정 절감에 기여하며 ▲제네릭 품질에 대한 품목 허가권자의 책임성 부여를 통해 제약기업 역량강화 및 수출 경쟁력 확보하고 ▲자체 연구개발 능력 향상을 통한 의약품 산업 구조 개선을 기대할 수 있다고 설명했다.
서정숙 의원도 작년 11월 동일한 임상시험자료 사용 동의 횟수 제한 약사법 개정안을 발의했다.
바이오제약산업의 유통 문란과 신약 개발 능력 약화 문제를 해소하기 위해 의약품 허가 시 동일한 임상시험자료 사용 동의 횟수를 3회로 제한(안 제31조제11항)하자는 내용이다.
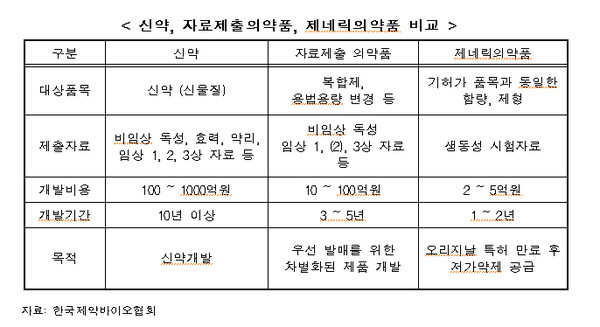
이에 대해 관련부처인 식약처는 신약 또는 식약처장이 정하는 의약품 등 임상시험 자료를 제출해야 하는 의약품의 경우 다양한 종류의 제품이 개발되고 있고, 개발하는 품목 특성에 따라 수행하는 임상시험의 규모 및 비용 등이 상이하므로 해당 임상시험 자료를 사용할 수 있는 품목수를 일률적으로 총 4개로 제한하는 것은 해당 의약품의 개발을 저해할 우려가 있다고 말했다.
임상시험의 경우 막대한 비용이 소요된다는 점에서 한 업체가 모든 비용을 부담하기 어려울 경우 여러 업체가 공동투자할 수 있는 기회를 제공할 필요가 있는 점을 고려할 때 해당 개정안에 대해 신중한 검토가 필요한 것으로 판단된다고 덧붙였다.
한편 생동시험 1+3 제한관련 개정안은 오는 25일 법안심사소위원회에 상정되지만, 자료제출의약품 관련 법안은 상정목록에 포함되지 않았다.

