ITT 및 HER2 초저발현 군에서도 유사한 mPFS 개선 효과 보여
HER 저발현 환자서 ORR, 엔허투군 57.3% vs TPC군 31.2%

다이이찌산쿄와 아스트라제네카가 공동 개발한 항체약물접합체 의약품(ADC) '엔허투(성분 트라스투주맙 데룩스테칸)'가 HER2(인간 표피 성장인자 수용체2) 저발현 환자의 1차 치료에서 무진행 생존기간 중앙값(mPFS) 13.2개월을 입증했다.
주세페 쿠리글리아노(Guiseppe Curigliano) 밀라노 대학교 의학종양학과 교수(이탈리아 유럽종양학연구소 부서장)는 2일(현지 시간) 미국 시카고에서 진행된 미국종양학회(ASCO) 연례 학술대회에서 'Destiny-Breast06' 3상 임상 시험의 중간 결과를 발표했다.
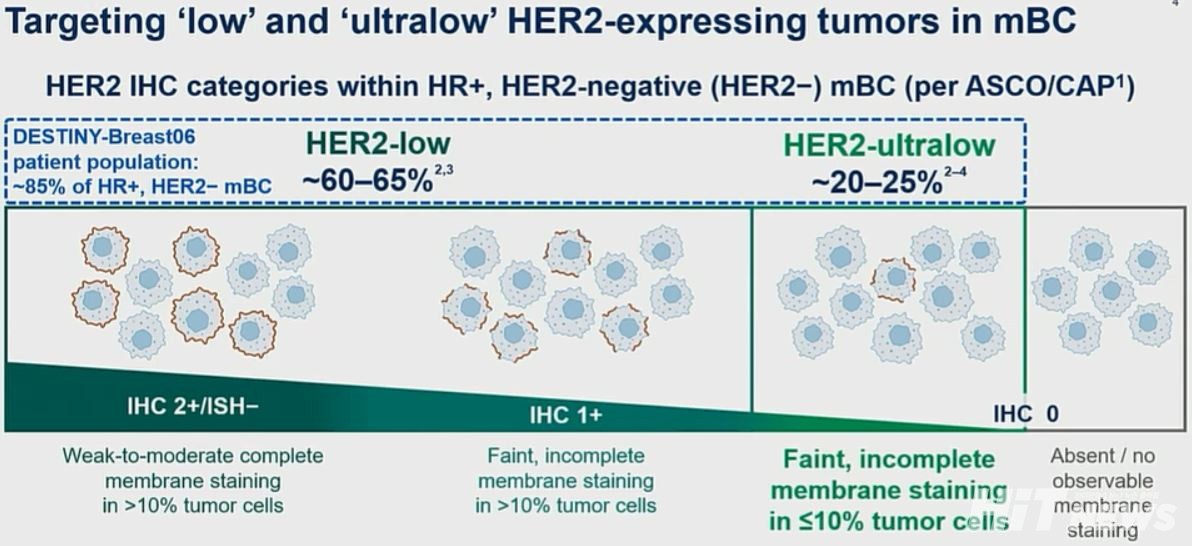
Destiny-Breast06 임상은 항암화학요법을 받은 적 없고 ①전이 단계에서 2차 이상 내분비요법 치료를 받았거나 ②보조요법으로 내분비요법을 시행해 24개월 이전에 질병이 진행한 경우 전이 단계에서 내분비요법을 1차 시행한 호르몬수용체 양성, HER2 저발현(IHC 1+ 또는 IHC 2+/ISH-))/초저발현(IHC 0 초과 1 미만) 환자를 대상으로 '엔허투'와 '의사의 선택 화학요법(TPC)'의 1차 치료 효과를 비교하는 연구다.
올해 3월 18일 기준, 866명의 환자(HER2 저발현=713명, HER2 초저발현=153명)가 무작위로 배정됐으며, 이 중 90.4%는 이전 CDK4/6 억제제로 치료받은 경험이 있었다. TPC 그룹 환자들은 카페시타빈(59.8%), 나브파클리탁셀(24.4%) 또는 파클리탁셀(15.8%)이 투여됐다.
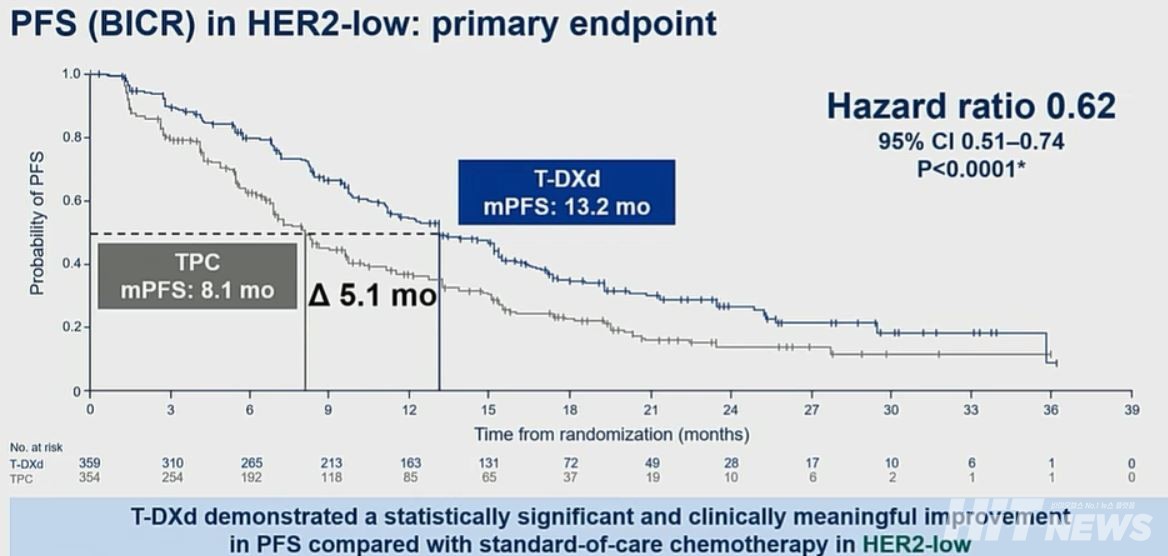
중간 분석 결과, 일차유효성평가변수인 독립적 중앙 맹검평가(BICR)에 의한 HER2 저발현 유방암 환자의 mPFS는 엔허투군이 13.2개월로, TPC그룹군 8.1개월보다 5.1개월 높았다. 이는 항암화학요법 대비 엔허투가 질병 진행 및 사망 위험을 38% 낮춘 결과다(HR : 0.62, 95% CI : 0.51-0.74, p<0.0001).
이 경향은 전체 환자군(ITT군, HER2 저발현+초저발현 환자) 및 HER2 저발현군 분석에서도 동일한 경향을 보였다. 주요 이차유효성평가변수인 전체 환자군에서의 mPFS는 엔허투군에서 13.2개월, TPC군에서 8.1개월이었으며(HR 0.63, 95% CI : 0.53-0.75, p<0.0001), HER2 저발현군에서는 각 13.2개월, 8.3개월이었다(HR 0.78, 95% CI : 0.50-1.21).
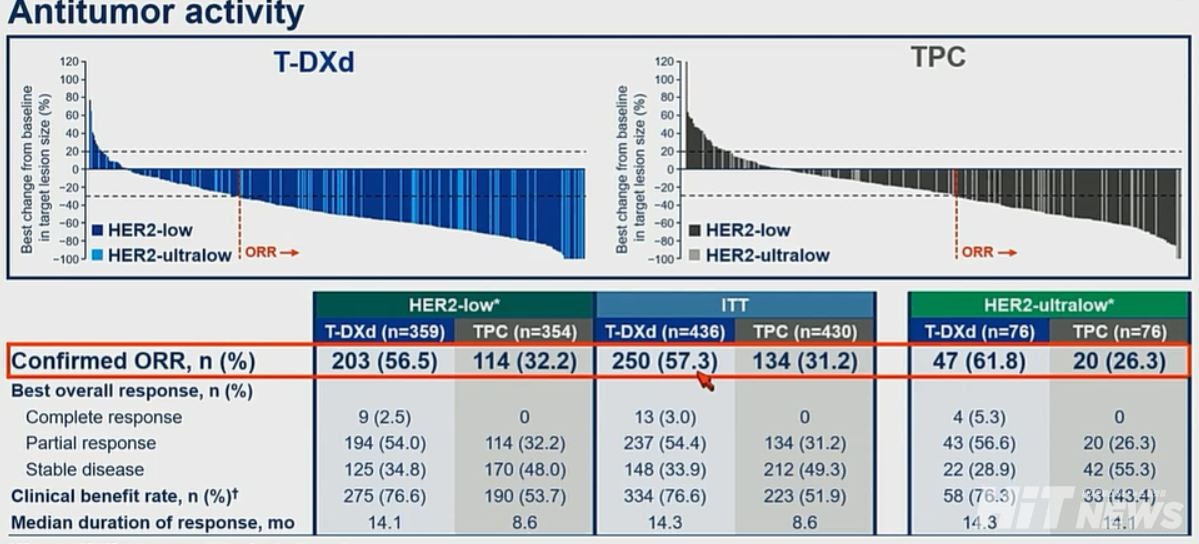
이차유효성평가변수인 HER2 저발현 환자에서의 객관적 반응률은 엔허투군이 56.5%(203명), TPC군이 32.2%(114명)이었다. 완전 관해율(CR)은 각 2.5%(9명), 0%이었고, 부분 관해율은 각 54.0%(194명), 32.2%(114명)이었다.
전체 환자군에서의 ORR은 엔허투군이 57.3%(250명), TPC군이 31.2%로 HER2 저발현 환자의 결과와 유사하게 도출됐다. 뿐만 아니라, HER2 초저발현 환자군에서는 각 61.8%(47명), 26.3%(20명)로 차이가 더 극명하게 벌어졌다.
전체생존율(OS)은 아직 데이터가 충분히 성숙하지 않아(Immature) 통계적 유의성을 확보하지 못했다. 12개월 시점 OS는 HER2 저발현 환자에서 엔허투군이 87.6%, CPT군이 81.7%였다. 이는 사망 위험을 약 17% 낮춘 수치다(HR 0.83, 95% CI : 0.66-1.05, p=0.1181).
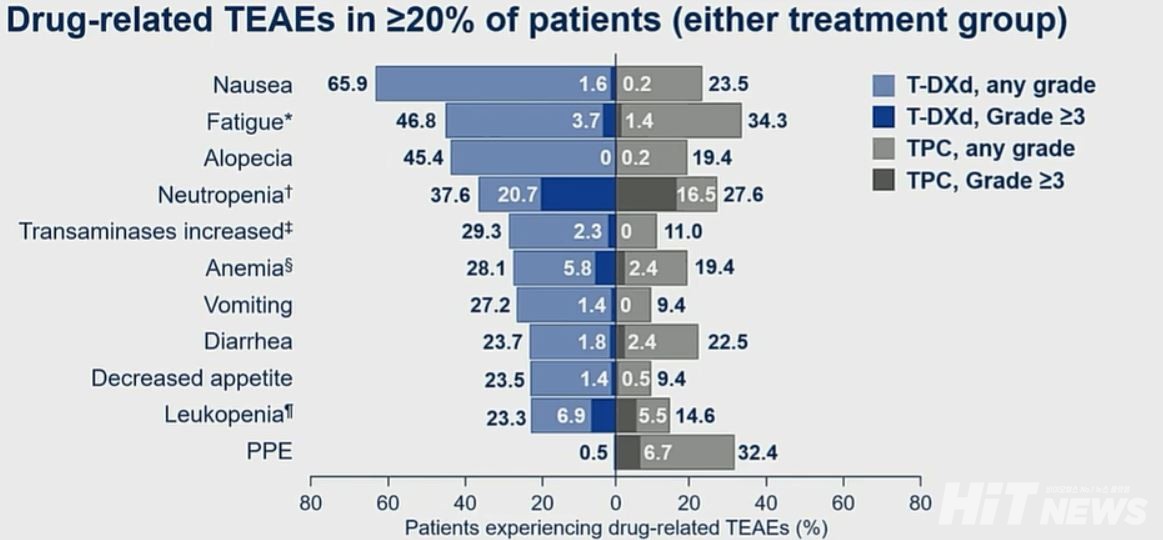
이번 연구에서 엔허투의 안전성 프로파일은 기존 유방암에서 보고됐던 이상반응과 일치한 것으로 나타났다. 엔허투군에서 가장 흔하게 발생한 3등급 이상의 치료 관련 이상반응(TEAE)는 호중구감소증(20.7%), 백혈구감소증(6.9%), 빈혈(5.8%) 순이었다. 약물 투여량 감소를 야기한 가장 빈번한 TEAE는 구역(Nausea)였다. 간질성 폐질환(ILD)와 폐렴은 엔허투군 중 11.3% 환자에서 발생했지만, 대부분 1~2등급의 중증도 수준이었다.
주세페 쿠리글리아노 교수는 "Destiny-Breast06 연구를 통해 엔허투가 1차 이상 내분비요법 치료를 받은 호르몬 양성, HER2 저발현/초저발현 전이성 유방암 환자의 새로운 치료 옵션이 될 수 있음을 입증했다"고 말하며 발표를 마쳤다.
한편, 다이이찌산쿄와 아스트라제네카는 지난달 20일 국내에서 엔허투를 HER2 저발현 유방암 2차 이상 치료 영역으로 확대한 바 있다. 해당 적응증 확대는 'DESTINY-Breast04' 3상 임상 연구를 근거로 이뤄졌다.
식품의약품안전처는 엔허투를 이전에 전이성 환경에서 전신 요법을 받았거나 보조 화학요법(adjuvant chemotherapy)을 받는 도중 또는 완료 후 6개월 이내에 재발한 절제 불가능한 또는 전이성 HER2 저발현(IHC 1+ 또는 IHC 2+/ISH-) 유방암 환자의 치료에 사용할 수 있도록 허가했다.

