아비테론듀오, '아비테론+프레드니솔론' 성분 전립선암 치료제
질티베키맙, 전신 염증 동반 심부전 이어 '급성 심근경색' 3a상 승인
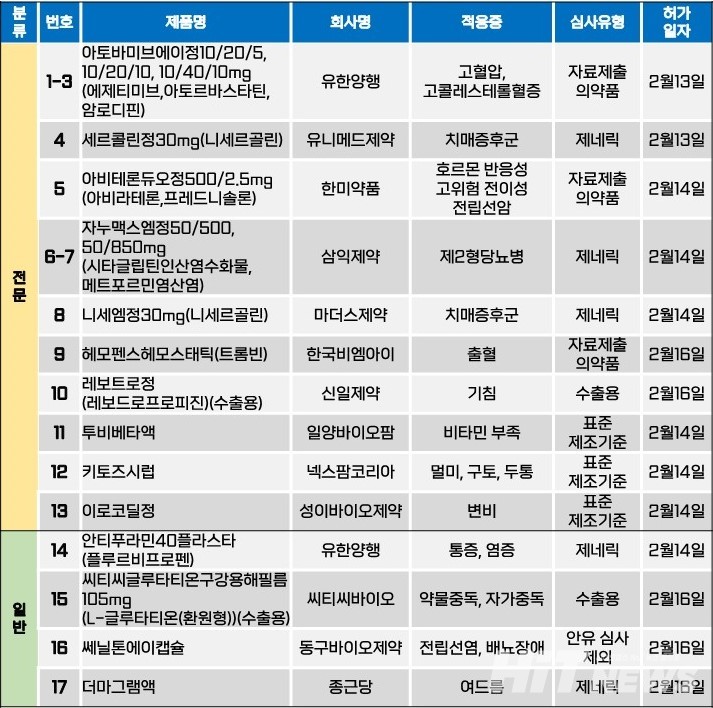
지난주(2월 12~16일) 총 17개 품목이 식품의약품안전처로부터 품목허가를 받았다. 전문의약품은 13개 품목, 일반의약품은 4개 품목이었다. 이 의약품들은 고혈압, 고콜레스테롤혈증, 제2형 당뇨병, 치매 증후군, 호르몬 반응성 고위험 전이성 전립선암 등 다양한 적응증으로 허가됐다.
한미약품이 전이성 전립선암 치료제 '아비테론정'의 복합제 버전인 '아비테론듀오(성분 아비라테론+프레드니솔론)'를 지난 14일 허가받았다. 아비테론은 한국얀센의 오리지널 의약품 '자이티가정'의 퍼스트 제네릭으로, 작년 6월 14일 허가된 후 같은해 10월 4일 출시된 바 있다.
아비테론은 고환과 부신, 전립선암세포 등 3개의 안드로겐(남성호르몬) 생성 경로를 모두 차단하는 안드로겐 생합성 저해제다. 안드로겐 합성 효소인 'CYP17'을 비가역적으로 억제해 암의 진행을 지연시키는 작용기전을 가진다.
출시 당시 회사는 오리지널 제품인 자이티가 대비 저렴한 약가를 강점으로 보험 재정 및 환자 부담에 도움을 줄 수 있다고 강조한 바 있다. 통상 아비테론 제제는 부신피질호르몬 제제인 '프레드니솔론' 성분 제제와 함께 처방되는데, 이번에 허가된 아비테론듀오 500/2.5㎎(아비테론/프레드니솔론)은 이 2개 성분을 복합제로 묶어 환자의 복약 편의성을 강화했다.
그동안 한미약품은 병용 처방되는 경우가 많은 성분들을 한 데 묶는 복합제 전략을 취해왔다. 회사는 4제 고혈압ㆍ고지혈증 복합제 시장에서도 1년 새 58%가량 시장 점유율을 확대하는 등 복합제 시장에서 눈에 띄는 성과를 보이고 있다. 회사의 전략이 향후 항암 복합제 분야에서도 통할 수 있을지 귀추가 주목된다.
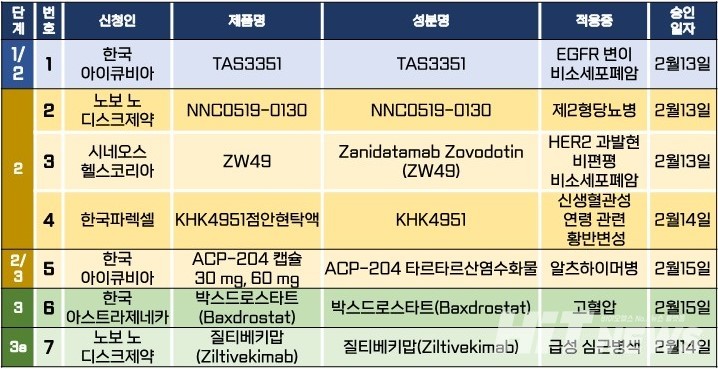
지난주 임상시험계획은 총 7건이 승인됐다. 세부적으로 △1/2상 1건 △2상 3건 △2/3상 1건 △3상 1건 △3a상 1건 등이다. 이 임상시험들은 제2형 당뇨병, 고혈압, 급성 심근경색, 신생혈관성 연령 관련 황반변성, 알츠하이머병 등 질환과 EGFR 변이 또는 HER2 과발현 비소세포폐암 등 암종을 대상으로 승인됐다.
노보노디스크가 개발 중인 심혈관계질환 치료제 '질티베키맙(Ziltivekimab)'이 지난 13일 급성 심근경색 환자를 대상으로 3a상 임상시험계획이 승인됐다. 이 치료제는 2020년 6월 노보노디스크가 미국 코비디아테라퓨틱스(Corvidia Therapeutics)를 인수하며 심혈관계 환자를 대상으로 개발해 온 인터루킨-6(IL-6) 단일클론항체다. IL-6은 면역반응과 염증반응에 중요한 역할을 하는 사이토카인의 한 종류다.
이번 임상시험(연구명 ARTEMIS)은 급성 심근경색 환자에서 심혈관 결과에 대한 질티베키맙 대 위약의 효과를 확인하기 위한 무작위, 이중 눈가림 3a상 연구다. 연구진은 225명(글로벌 1만명)을 대상으로 오는 6월부터 임상을 시작해 2026년 9월 완료하는 것을 목표로 한다. 임상은 △서울아산병원 △연세대 세브란스병원 △연세대 원주세브란스기독병원 △충남대병원 △분당서울대병원 △길병원 △고려대 의대부속병원 △전남대병원 등 의료기관에서 진행될 예정이다.
이번 임상의 1차 유효성 평가변수(Primary endpoint)를 'CV(심혈관) 사망, 비치명적 MI(심근경색), 비치명적 뇌졸중 등 3개 요소의 MACE(주요 심장사건) 평가변수가 나타나는 최초 발생까지의 시간'으로 설정했다. 2차 유효성 평가변수(Secondary endpoint)는 △CV 사망, 비치명적 MI 또는 비치명적 뇌졸중 건수 △모든 원인의 사망, 비치명적 MI, 비치명적 뇌졸중 등으로 구성된 MACE 평가변수의 최초 발생까지의 시간 △모든 원인의 사망, 비치명적 MI 또는 비치명적 뇌졸중 건수 등이다.
한편, 회사는 지속적으로 염증과 관련된 심혈관질환 환자들을 대상으로 한 임상을 확대해 진행해 오고 있는 중이다. 지난 2021년 9월 △죽상경화성 심혈관질환 △만성 신장병 및 전신 염증 환자를 대상으로 심혈관 관련 질티베키맙 대비 위약 효과를 비교하는 3a상 임상시험계획을 승인받았다. 또 작년 2월 20일에는 박출률이 약간 감소하거나 보존된 전신 염증을 동반한 심부전 환자에서 이환 및 사망에 대한 위약 대비 효과를 비교하기 위한 3상 임상시험계획을 승인받은 바 있다.

