지놈앤컴퍼니, 위암·담도암 타깃의 GEN-001 임상 박차
고바이오랩, 궤양성 대장염·건선 타깃의 파이프라인 개발
CJ바사, 지난 1월 FDA서 CJRB-101의 1/2상 IND 승인
지난달 세계 최초의 경구용 마이크로바이옴 치료제인 '보우스트(Vowst)'가 탄생한 가운데, 국내 신약 개발 기업들이 다양한 적응증을 타깃으로 하는 마이크로바이옴 치료제 개발에 나서고 있다. 국내에서는 △지놈앤컴퍼니 △고바이오랩 △CJ바이오사이언스 △에이치이엠파마 △이뮤노바이옴 등이 마이크로바이옴 치료제 개발에 도전하고 있다.
지놈앤컴퍼니(대표 배지수·박한수·서영진)는 마이크로바이옴 면역항암 치료제 GEN-001의 위암 대상 임상 2상(바벤시오 병용 투여) 중간 결과를 올해 상반기에 발표할 예정이다. 지난 3월 회사 관계자는 "독일 머크(Merck), 화이자(Pfizer)와 합의된 내용에 한해 상반기에 중간 결과 내용을 밝힐 계획"이라며 "위암 대상 2상 중간결과 세부 데이터는 2023년 하반기 해외 학회를 통해 발표할 것"이라고 말했다.
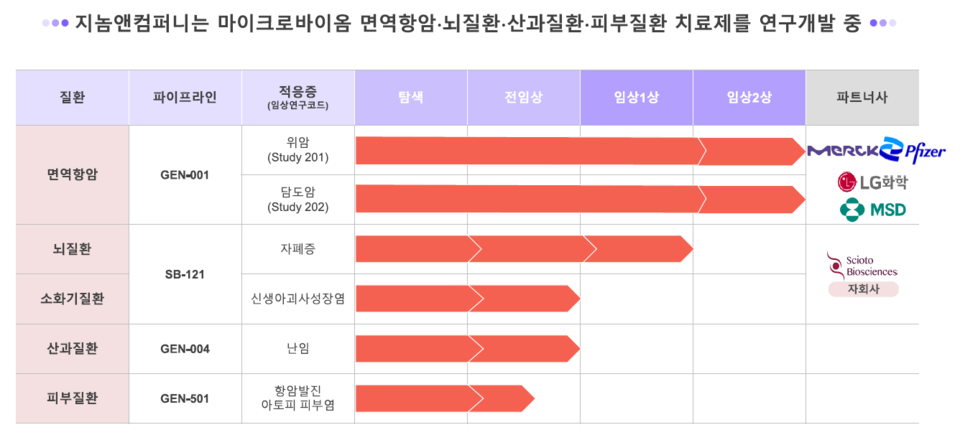
회사는 GEN-001의 담도암 대상 임상 2상(키트루다 병용 투여) 진행에 나서고 있는 가운데 임상개발 전략 수정에 나섰다. 회사는 지난달 28일 공시를 통해 GEN-001의 담도암 환자 대상 국내 2상 임상시험계획(IND) 변경승인을 신청했다고 밝혔다.
회사 관계자는 "펨브롤리주맙과 GEN-001의 병용 투여 시에 대한 GEN-001의 안전성 및 유효성뿐만 아니라 펨브롤리주맙과 mFORFOX(성분명 플루오로우라실·류코보린·옥살리플라틴), GEN-001을 병용 투여하는 경우에 대한 GEN-001의 안전성 및 유효성을 함께 탐색할 것"이라고 강조했다.
또한 자회사 '사이오토 바이오사이언스(Scioto Biosciences)'는 뇌질환 마이크로바이옴 치료제 SB-121(개발코드명)을 개발하고 있다. SB-121은 자폐 스펙트럼 장애(ASD, Autism Spectrum Disorder)를 적응증으로 하는 치료제다.
고바이오랩(대표 고광표)은 지난달 식품의약품안전처로부터 궤양성 대장염 치료제 파이프라인 'KBLP-007(후보물질 KBL697)'의 2상 임상시험계획(IND)을 승인받았다.
회사 관계자는 "KBL697은 뛰어난 안전성 및 내약성이 검증된 고기능성 생균치료제 개발 후보로 이를 활용해 건선을 타깃하는 KBLP-001과 궤양성 대장염을 타깃하는 파이프라인 KBLP-007을 개발하고 있다"고 설명했다. 현재 KBLP-007은 미국 식품의약국(FDA)으로부터 임상 2a상을 승인받아 호주에서 환자 모집을 진행하고 있다.
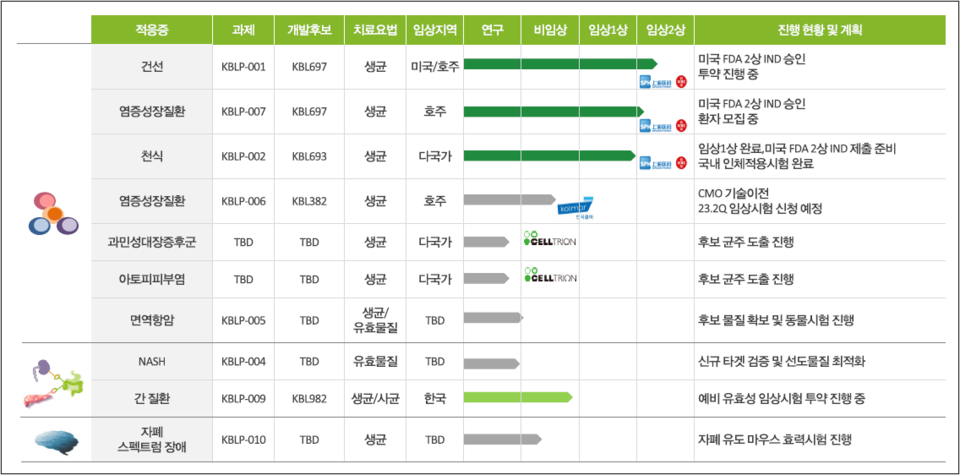
CJ바이오사이언스(대표 천종식)는 지난 1월 FDA서 마이크로바이옴 면역항암치료제 CJRB-101의 1/2상 임상시험계획서(IND)가 승인됐다고 밝혔다. CJRB-101은 CJ바이오사이언스가 확보한 면역항암 타깃 신약 후보물질(파이프라인)로, CJ제일제당이 구축해온 균주 라이브러리를 기반으로 다양한 면역학적 검토를 통해 개발됐다.
또한 회사는 지난 3월 마이크로바이옴 기업 4D파마(4D Pharma)가 보유 중인 유망 신약 후보물질과 플랫폼 기술을 인수하는 계약을 체결했다. 신규 도입되는 신약 후보물질(Drug candidate)은 총 9건으로 고형암·소화기질환·뇌질환·면역질환 등을 대상으로 한다.
에이치이엠파마(대표 지요셉)는 지난 3월 저위전방절제증후군(Low Anterior Resection Syndrome) 치료제 후보 미생물인 HEM1036에 대해 호주 인체연구윤리위원회(HREC) 승인 후 호주 식품의약품안전청(TGA)에 임상 2상시험계획(IND)을 통보했다. 회사는 같은 달 우울증 치료제 신약 후보물질 HEM20-01에 대한 임상시험계획(IND)을 FDA에 제출했다.
이뮤노바이옴(대표 임신혁)은 지난 2월 염증성 장질환 및 난치성 자가면역질환 신약 후보물질 'IMB002'가 임상 1상에 진입했다고 밝혔다. 회사는 이번 임상 1상에서 건강한 성인을 대상으로 IMB002 투여 후 장내 미생물 조성 변화 및 안전성 검증을 목표로 하고 있다.
보우스트, FDA서 승인 받았지만…"숙제로 남은 적응증 확장"
지난달 FDA서 허가받은 세레스테라퓨틱스(Seres Therapeutics)의 경구용 클로스트리디움 디피실 감염증(CDI·Clostridium Difficile Infection) 치료제인 보우스트(Vowst)는 CDI 재발 예방을 위한 치료제로 승인됐다.
첫 경구용 마이크로바이옴 치료제 보우스트는 마이크로바이옴 업계에 긍정적인 이벤트임이 분명하지만, 염증성 장질환 치료제이기 때문에 다른 적응증 타깃의 마이크로바이옴 치료 후보물질의 임상개발 성공 가능성과 뚜렷한 상관관계는 없다.
한 바이오업계 관계자는 "재발성 CDI 예방을 위한 마이크로바이옴 치료제와 항암 또는 건선 치료를 목적으로 하는 마이크로바이옴 치료제는 작용기전이 다르기 때문에 연관 관계를 도출하는 것이 어렵다"며 "각각의 적응증은 개별의 임상시험으로 증명해야 한다고 생각한다"고 전했다.
관련기사
- 첫 경구용 마이크로바이옴 치료제 탄생…업계 "산업 성장 기대"
- 고바이오랩, '궤양성 대장염' 치료제 국내 임상2상 승인
- CJ바사, AACR서 CJRB-101 항암효과와 작용기전 발표
- 지놈앤컴퍼니, 장뇌축 기반 뇌질환 치료제 개발 나서는데
- "마이크로바이옴 R&D 문제 개선? 의료 분야 투자해야"
- 제자와 스승이 창업한 HEM파마, 연내 코스닥 상장 추진
- "FDA 첫 마이크로바이옴 신약 승인...K바이오, 면역항암제 개발 중"
- CJ바이오사이언스, 최대주주 CJ제일제당 유증 참여 여부 촉각
- 에이치이엠파마, 美 FDA서 우울증 신약 후보물질 임상 2상 승인받아
- 마이크로바이옴 신약기업협의회 발족…"27개 기업 똘똘 뭉쳐"
- 이뮤노바이옴, 염증성 장질환 치료제 국내 임상 1상 승인

