현행 DTC규제의 틀과 보건복지부의 항목 인증제 정의와 현황
신기현 변호사가 풀어주는 디지털 헬스케어와 법률
디지털 헬스케어 등장으로 헬스케어 관련 제도들의 재정비가 예상되는 가운데 히트뉴스는 헬스케어 전문 법률전문가 신기현 변호사와 함께 현재 이뤄지고 있는 디지털 헬스케어 도입 시도와 법적 쟁점을 알아보고 합리적 개선을 위한 제안을 소개한다.
① 비대면 진료 ② 의약품 배송 ③ DTC ④ 웰니스 ⑤ Guess What...?
DTC(Direct to customer)란 소비자들이 의료기관을 거치지 않고 유전자검사기관에 직접 의뢰해 받는 유전자 검사 서비스를 일컫는다. 생명윤리법에서는 이를 '소비자 대상 직접 시행 유전자검사'라고 정의하고 있다.
국외에서는 DTC 검사가 이미 널리 시행되고 있어 2019년 기준으로 약 7조7천억원 정도의 해외 시장이 형성돼 있다고 하나, 국내 시장은 아직 10억원 규모에 미치지 못하고 있는 것으로 파악된다.
이러한 시장 규모의 차이는 DTC에 대해 각국이 바라보는 시각과 그에 따른 규제 강도의 차이에서 비롯된 것으로 짐작된다. 본 기고에서는 DTC에 대해 어떤 규제가 존재하고, 어떠한 개정 논의가 있어 왔는지를 살펴보고자 한다.
현행 DTC 규제의 틀
DTC에 관한 규제는 생명윤리법에 있다. 생명윤리법 제50조 제3항은, 의료기관이 아닌 유전자검사기관은 원칙적으로 유전자검사를 할 수 없고, 다만 질병의 예방과 관련된 유전자검사로 보건복지부장관이 필요하다고 인정하는 경우(즉, 보건복지부가 고시하는 경우)에만 유전자검사를 할 수 있도록 했다.
위와 같은 법률에 따라 보건복지부는 '의료기관이 아닌 유전자검사기관이 직접 실시할 수 있는 유전자검사 항목에 관한 규정(고시)'을 마련하고 있다.
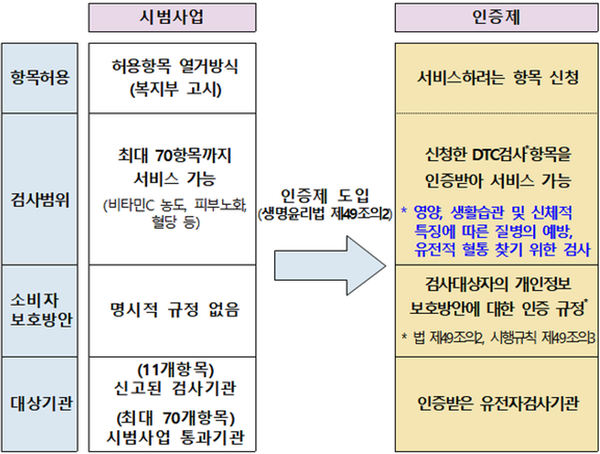
보건복지부 고시의 개정: 허용 항목 제한 열거방식 → 항목 인증제
위 보건복지부 고시는 2022년 2월 22일에 개정됐는데, 개정 이전에는 별표에 열거된 70개의 항목(혈당, 혈압, 비타민D 농도 등)에 대해서만 DTC가 제한적 허용돼 검사의 실용성에 대해 아쉬움을 표하는 시각이 많았다.
보건복지부는 당시 개정을 통해, 꼭 열거된 항목이 아니더라도 검사역량에 대하여 인증을 받은 기관은 인증 받은 범위 내에서 소비자 대상 직접 시행 유전자검사를 실시할 수 있도록 했다. 즉, 인증 받은 기관은 DTC 검사 항목을 신청하고, 이를 인증 받아 서비스를 할 수 있게 된 것이다.
결론적으로 유전자검사기관이 검사역량을 갖추었다면, 검사 항목을 자유롭게 신청해 인증을 받은 후 서비스가 가능해져, 이론적으로는 검사 가능한 서비스 항목이 대폭 확대될 수 있게 됐다.
인증제 운영 현황
'인증'이라는 행정 절차가 개입되는 만큼, 제도 개선의 성패는 그 운영에 달려 있다고 해도 과언이 아닐 것이다. 위 고시 개정은 2022년 2월에 이뤄졌으나, 아직 DTC 인증을 수행하는 기관 및 검사의 정확도를 평가하는 기관의 자격 요건에 관한 법령(고시 포함)이 완비되지 않아, 현재는 인증제가 실질적으로 운영되지 못하고 있는 것으로 보인다.
정부 차원의 의지를 담은 규제 개선이 이루어진 만큼, 이를 뒷받침하는 법령 정비도 신속히 이루어지기를 기대해 본다. 다소 늦은 감도 있지만, 이와 같은 개선이 국내 DTC 산업 성장의 중요한 밑그림이 될 수 있기를 바란다.

신기현 변호사/법무법인 윈스 파트너변호사
법무부, 특허청 등 법무관 활동한 바 있으며 현재는 법무법인 윈스에서 벤처·스타트업의 기업법무, 헬스케어, 지식재산권(IP/저작권), 형사소송, 의료소송 등 업무를 수행하고 있다.
현재 특허청 규제개혁위원회 위원, 법무부 창조경제혁신센터 법률지원단, 한국무역협회 스타트업브랜치 상담위원으로 활약하고 있다.

