네비보롤 검토자료 9월 30일·시험결과 11월 30일,
클래리트로마이신 시험결과 12월 1일까지 제출

지난해 10월 캐나다 연방보건부(Health Canada)가 심전도 상 QT간격(심실기) 연장 및 TdP(다형성심실 빈맥)가 존재하는 환자, 전해질 장애를 가진 환자에게 금기시 해 이슈가 됐던 항생제 '클래리트로마이신' 제제가 이번엔 니트로사민류(NDMA) 불순물함유 가능성으로 취급 완제 제약사들의 긴장을 사고 있다. 엎친 데 덮친 격으로 고혈압 치료에 사용되는 '네비보롤' 제제도 함께 NDMA 불순물 이슈 도마에 올랐다.
식품의약품안전처는 최근 '클래리트로마이신' 성분 의약품에서 NDMA 불순물이 검출됐다는 안전성 정보를 입수함에 따라, 사전적 예방조치 차원에서 관련 완제의약품(정제에 한함) 업체에 불순물 시험검사를 요구하는 공문을 송부했다.
시험 대상은 시중 유통 가능한 완제품 중 대표성 있는 제조번호 제품이며, 제출 기한은 오는 12월 1일까지다.
식약처는 지난해 10월 캐나다 연방보건부가 클래리트로마이신 제제 안정성 정보 변경함에 따라, 지난 2월 17일 국내 클래리트로마이신 제제 취급 업체들을 대상으로 안전성·유효성 입증자료 등 근거자료 제출과 허가 변경 필요 여부에 대한 의견을 요청한 바 있다.
'네비보롤' 제제 또한 불순물 이슈로 시험 결과 제출이 요구됐다.
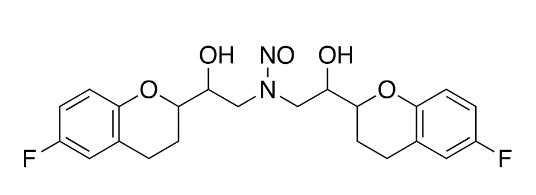
식약처 의약품관리과 관계자는 "최근 네비보롤 성분 함유 완제의약품에서 불순물(N-Nitroso-Nebivolol)이 검출됐다는 안전성 정보를 입수했다"며 "사전예방적 조치를 위해 이 성분 함유 완제의약품 제조(수입) 품목에 대한 검토 자료와 시중 유통 가능한 완제품 중 대표성 있는 제조번호에 대한 시험검사 결과를 제출할 것"이라고 요청했다.
여기서 검토 자료란 △발생가능성 평가 △공정검토 자료 △자체 1일 섭취허용량 및 설정 근거 등을 말하고, 시험 검사 결과는 매년 사용기한 임박한 3개 제조 단위 이상 제품 혹은 매년 3개 이하로 생산한 경우 전 제조번호 제품을 대상으로 한다. 각 제출기한은 오는 9월 30일과 11월 30일이다.
식약처 의약품관리자 관계자는 두 공문 모두 "제출기한 이전이라도 해당 불순물이 검출된 경우 즉시 식약처에 보고하는 등 필요한 조치를 취해주시기를 바란다"고 전했다.
다만, 식약처 측은 이번에 조치된 각 제제 불순물이 국내·외 중 어느 국가·업체에서 발견됐는지 공개하지 않았다.
한편, 클래리트로마이신은 기관지염, 폐렴, 인두염과 같은 상·하기도감염증 및 마이코박테리아 감염증 등에 사용되는 항생제다.국내 클래리트로마이신 성분 제제는 수입품목을 포함해 총 259 품목이다. 취급 제조·수입 업체는 총 120곳이다. 유비스트에 따르면, 지난해 이 성분 원외처방조제액은 약 424억 원에 해당했다. 한미약품 '클래리'가 49억 원 규모로 가장 큰 매출을 올린 것으로 나타났다.
네비보롤은 교감신경 베타1(β1) 수용체를 선택적으로 차단하고, 일산화질소(NO)를 강화시켜 혈관을 확장해 혈압을 낮추는 약물이다.
국내 네비보롤 성분 제제는 총 19 품목이며, 지난해 이 성분 원외처방조제액은 약 164억 원으로 집계됐다. 한국메나리니 '네비레트'가 76억 원으로 가장 큰 매출을 올렸다.

