황기자의 주간 의약품 품목허가/임상승인 모아보기(3월7일~3월11일)
국내 최초 RET 돌연변이 암 표적 신약 한국릴리 '레테브모캡슐' 허가
셀트리온 '램시마프리필드시린지' 국내 자체 생산·유통 돌입
미FDA 조건부 승인 듀센형근이영양증 치료제 국내 임상 3상 돌입

품목허가, RET 돌연변이 암 타겟 신약 등장
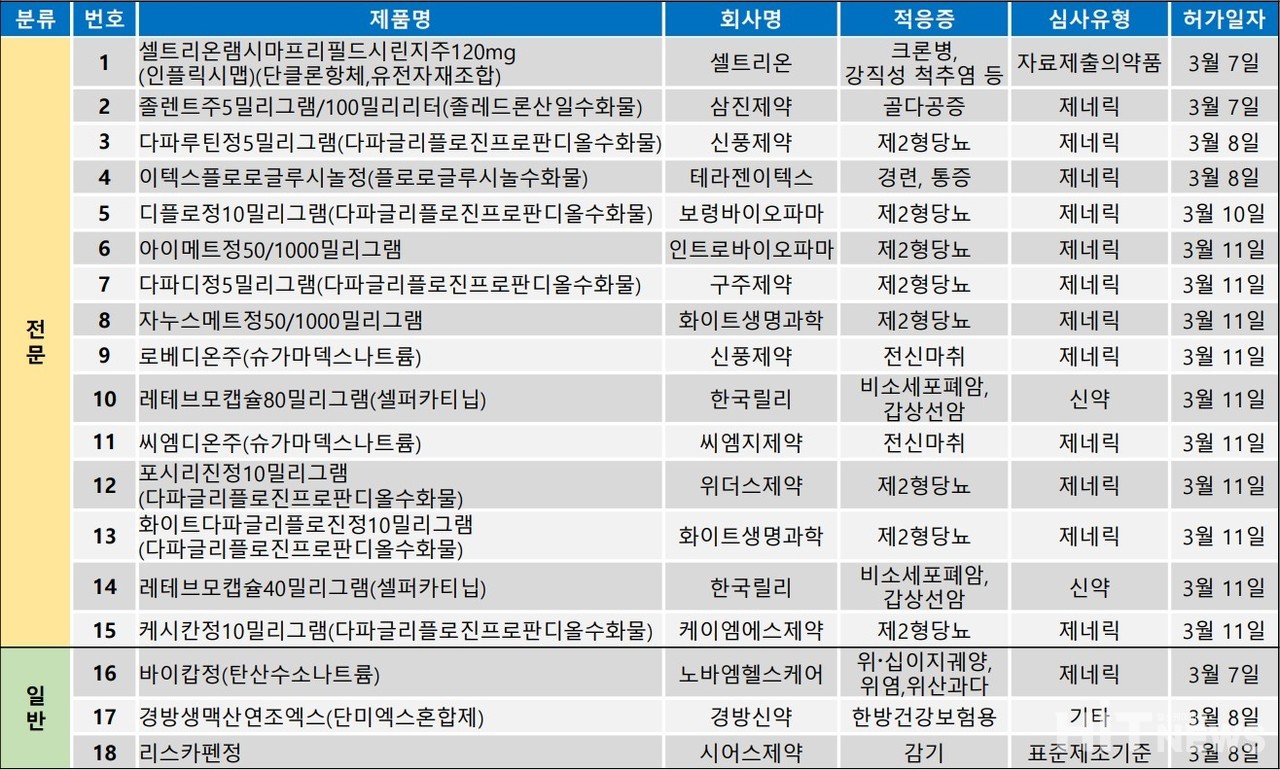
지난 주(3월 7일~3월 11일)에는 국내 최초로 RET 돌연변이 암 환자를 위한 신약인 한국릴리 '레테브모캡슐', 국내 자체 생산을 선언한 크론병 치료제인 셀트리온 '램시마프리필드시린지주' 등의 식품의약품안전처 품목허가 소식이 전해졌다.
전체 품목허가 수는 총 18건이며, 이 중 전문의약품은 15건, 일반의약품은 3건이었다. 이번 허가된 제2형당뇨약은 8건으로, 전문약 허가의 50% 이상을 점유하며 여전히 강세를 보였다.
이번 품목허가 현황에는 한국 릴리의 RET 돌연변이 암 표적 신약인 ‘레테브모캡슐’이 등장했다.
허가 품목은 2가지 용량(40mg, 80mg)으로, 점·융합 돌연변이 등 RET 유전자 변이를 표적해 억제제하는 표적치료제로는 국내에서 처음 허가(First-in-Class)됐다.
식약처는 레테브모를 △전이성 RET 융합-양성 비소세포폐암 성인 환자 △전신요법을 요하는 진행성 또는 전이성 RET-변이 갑상선 수질암이 있는 성인 및 만 12세 이상 소아 환자 △방사선 요오드에 불응하고, 이전 소라페닙 및/또는 렌바티닙의 치료 경험이 있으며 전신요법을 요하는 진행성 또는 전이성 RET 융합-양성 갑상선암 성인 환자 등에 사용할 수 있도록 허가했다.
이 약은 식약처 신속 심사 과정을 통해 허가된 것으로 확인되며, 지난 2020년 미국 FDA 신속 심사(Accelerated Approval), 우선 심사(Priority Review) 혁신의약품 및 희귀의약품 지정(Breakthrough Therapy&Orphan Drug Designation) 등이 적용돼 미국에서 동일 환자군을 대상으로 승인된 바 있다.
셀트리온 '램시마프리필드시린지(인플릭시맵)'의 허가도 주목된다.
이번에 허가된 램시마는 IV(정맥주사) 타입이 아닌, SC(피하주사) 타입으로 크론병, 류마티스성 관절염, 강직성 척추염 등에 사용되는 제제다.
회사는 이미 2020년 '램시마프리필드시린지'에 대한 허가를 받은 바 있다. 다만 당시에는 독일에서 제조된 의약품을 수입해 국내 유통했던 방식이었다면, 이번 허가에서는 자회사인 셀트리온제약 오창 공장에서 제조 및 국내 유통까지 전담할 것으로 나타났다.
회사 관계자에 따르면, 해당 시설은 연간 약 2900만 실린지 생산력(Capacity)을 보유한 상태인 것으로 확인됐다.
임상승인, 미FDA 조건부 승인된 듀센형근이영양증 치료제 국내 임상 3상 돌입
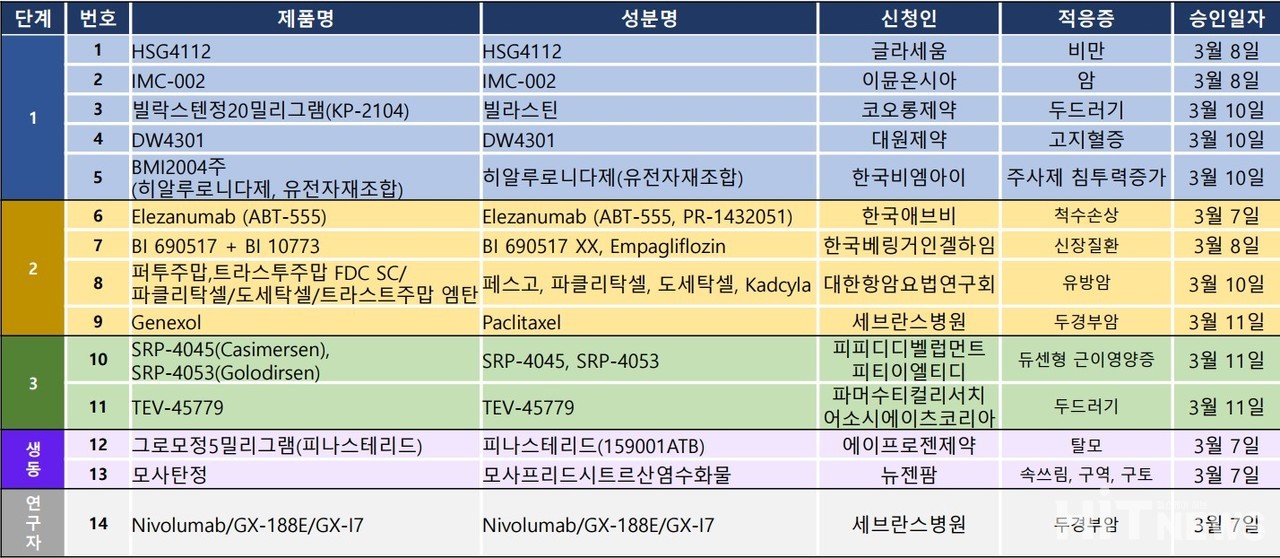
지난주 임상시험계획은 총 14건이 승인완료됐다. 세부적으로 임상 1상 5건, 2상 4건, 3상 2건, 생물학적동등성 2건, 연구자임상 1건 등으로 확인됐다.
임상 적응증은 유방암, 두경부암, 듀센형 근이영양증, 두드러기, 비만 등 다양한 종류로 나타났다.
바이오기업 글라세움이 비만 치료제로 사용되는 'HSG4112' 성분에 대한 임상시험 1상이 승인됐다. 회사는 이미 2020년 해당 성분에 대한 임상1상을 완료했으며, 현재 2상을 진행 중에 있다.
이번 임상시험계획에 따르면, 임상시험은 기존 1상이 '남성' 혹은 '비만인' 조건도 적용됐던 것과 달리, 건강한 성인만을 대상으로 '식이 영향에 대한 평가'와 '약력/약동학적 특성 평가' 등을 목적으로 진행되는 것으로 나타났다.
글로벌 임상시험수탁기관인 '피피디디벨럽먼트피티이엘티디'는 'SRP-4045', 'SRP-4053' 성분에 대한 임상시험 3상에 돌입한다.
이 성분들은 미국 RNA 표적치료제 전문 제약사 사렙타 테라퓨틱스(Sarepta Therapeutics)의 듀센형 근이영양증 환자 치료 성분으로, 이번 임상시험은 SRP-4045와 SRP 4053 복합 투여에 대한 평가를 목적으로 한다.
이 성분은 해당 적응증 환자의 특정 유전자인 엑손(Exon) 45를 스키핑(Skipping)시킨다. 스키핑 작용은 문제가 되는 유전자가 발현되지 않도록 유전자 번역을 건너뛰게 해주는 역할을 한다.
SRP-4045는 '카시머센(Casimersen, AMONDYS 45)'이라는 명칭으로 지난해 미국 FDA에게 조건부 허가로 시판 승인됐다. 이에 따라 회사는 2024년까지 FDA에게 글로벌 3상 연구를 완료해 추가적인 임상 데이터를 제출하도록 요구된 바 있다.

