식약처, 부산제조소 최장 7일 내 현장조사 마치고 결정
"사실일 경우, 업계 신뢰 해악… 제도·품질 되돌아 볼때"
약업계가 의약품 주원료 용량과 제조방법 임의조작 의혹을 받는 바이넥스 사태를 주시하며 "의혹이 사실이라면 있을 수 없는 일"이라며 공분하고 있다.
'별지'두고 제조 바이넥스, 위탁품목 32개도 회수
바이넥스 사태는 8일 YTN의 보도로 시작됐다. 바이넥스가 해열제와 우울증약, 당뇨 약 등의 용량을 조작해 제조, 판매했다고 보도한 것이다.
식약처는 당일 오후 바이넥스가 허가 또는 신고된 사항과 다르게 제조한 6품목(아모린정·셀렉틴캡슐·닥스펜정·로프신정250mg·셀렉틴캡슐10mg·카딜정1mg)에 대해 잠정 제조·판매 중지 및 회수 조치를 내리고, 부산 제조소 조사에 착수했다.
보도에서 지적된 핵심 혐의는 바이넥스가 식약처에서 허가받은 제조법 옆 '별지 제조방법'을 따로 뒀다는 점이다. 한마디로 제조 조작 의혹 제기다. 당뇨병치료제인 아모린정은 주성분인 글리메피리드 함량이 1/10 수준으로 기준치 이하고 우울증치료제 셀렉틴캡슐에 대해서는 용량을 초과 배합했다고 문제를 제기했다.

특히 식약처 정기감시 때, 문서와 관련 사실을 은폐하는 등 오랜기간 회사 차원의 조작 시도가 있었다고도 나왔다. 사실이라면 허가사항과 다르게 임의대로 품목을 제조한 게 된다. 사실상 포장만 다른 위탁제네릭도 문제가 된다.
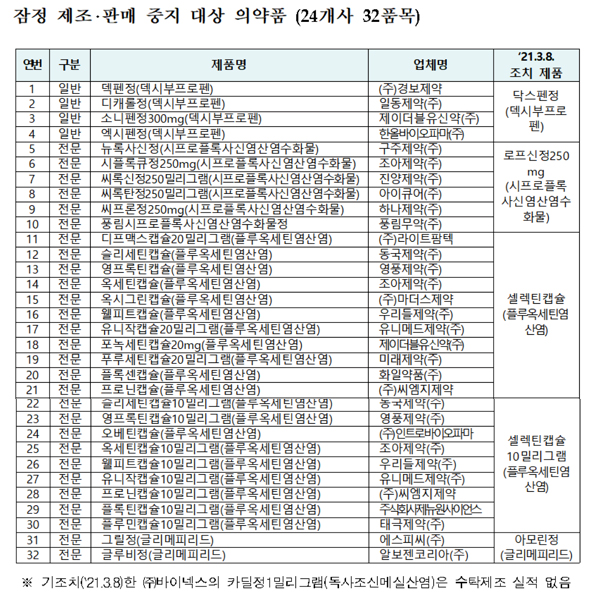
식약처는 6개 바이넥스 품목에 더해 수탁제조하는 24개사 32품목에 대해서도 9일자로 잠정 제조·판매중지 및 회수 조치했다.
식약처 관계자는 "바이넥스가 자진 회수하는 6품목과 위탁 제네릭 등 부산 제조소 제품에 대해 GMP 기준에 따른 제조법과 용량 조작 위반여부를 조사하고 있다"며 "필요시 업체의 다른 GMP 제조소도 조사할 수 있다"고 말했다.
때문에 위탁사들은 촉각을 곤두세우는 모습이다. 더욱이 보도를 통해 바이넥스가 10개 제품을 자진신고했다고 밝혀 문제 품목이 더 늘어나는 것 아니냐는 관측도 나온다.
제조업무정지부터 품목 허가취소까지 가능
식약처는 회사가 허가와 GMP(품질관리) 규정 등을 위반한 사실이 특정 또는 모든 품목에 해당하는지, 부산 제조소만의 문제인지 등을 조사한 뒤 행정처분할 것으로 보인다. 사안에 따라서는 검찰 고발도 따를 것으로 예상된다.
위반 사실과 고의성 등을 검토해 의약품 등의 안전에 관한 규칙에 따라 ▲해당 제품 제조업무정지 1~6개월 ▲전 제조업무정지 1~3개월 ▲해당 품목허가 취소 ▲업체에 대한 제조업 허가 취소 등의 행정처분이 가능하다.
이와 관련 업계는 주성분 원료 용량을 조작하는 등 임의제조하는 일은 '있어서는 안되는 일'로 규정하며 업계 신뢰에 좋지 않은 영향을 미칠 것이라고 우려했다.
A제약사 개발담당 임원은 "설비시설이 낡아 품질편차를 줄이기 위해서라면, 그 시설은 버려야 할 시설이며 정기점검할 때 거짓말했다는 것"이라고 했다.
제약사 대표를 역임한 바 있는 B업체 대표는 "GMP 규정을 위배하는 것이므로 용인될 수 없다. 방법을 변경해 운영할 수 있지만 그러기 위해서는 관련 문서를 변경해 당국의 승인을 받고 사안에 따라 밸리데이션 시험을 해야한다"고 설명했다.
바이넥스 사례에 아연실색...위탁제네릭 문제 곱씹어봐야
업계는 바이넥스 의혹을 부적절한 특정 업체 사례로 규정하면서도 제조 맡긴 업체들도 책임있음을 언급했다.
C제약사 개발담당 관계자는 "주원료 함량과 제조방법을 조작하는 것은 업계에서는 있을 수 없는 일이다. 바이넥스 사례를 모든 제약사의 문제로 확대해석해야 하는 것은 경계해야 한다"면서도 "위탁제네릭 문제는 살펴봐야 한다"고 전했다.
D제약사 대표는 "(사실로 밝혀질 경우) 바이넥스의 사례는 옛날 일부 제약사들의 부적절한 행태라 볼 수 있다. 복용환자들 부작용을 걱정할 수 밖에 없다"며 "이는 위탁제네릭사들도 책임져야 할 것"이라고 했다.
식약처 허가사항에 따르면, 바이넥스는 411품목의 허가를 갖고 있는데 자사 웹 사이트를 통해 127품목이 시판되는 것으로 소개된다. 타 제약사 194품목을 위탁생산하고 있다.
이와 관련 대한약사회는 "무제한 위탁생동‧공동개발 제도가 불러온 예고된 참사"라며 "식약처가 이번 사태가 의약품 전반에 대한 불신으로 번지지 않도록 아주 빠르게 국내 제조소 GMP를 전면 재검토하고 품목 허가권자의 의무를 강화하는 것을 포함해 위탁생동‧공동개발 품목 허가제도를 재설계해야 한다"고 요구했다.

