뇌 전이 환자 대상 3b/4상 임상 'DESTINY-Breast12' 연구
안정적 뇌 전이 환자 62.9%, 활동성 뇌 전이 환자 59.6%로 유사

[바르셀로나(스페인)=황재선 기자] 아스트라제네카와 다이이찌산쿄가 공동 개발한 항체약물접합체(ADC) '엔허투(성분 트라스투주맙 데룩스테칸)'가 HER2 양성 뇌전이 유방암 환자에서의 무진행생존(PFS) 및 전체생존(OS)에서의 이점을 입증했다.
14일(현지시간) ESMO 연례학술대회에서는 HER2 양성 전이성 유방암 환자 중 뇌 전이 환자를 대상으로 한 3b/4상 'Destiny-Breast12' 데이터가 공개됐다. 이 연구는 뇌 전이가 있거나 없는 HER2 양성 전이성 유방암 환자 500명을 대상으로 엔허투의 유효성 및 안전성을 평가한 최초의 다국가, 다기관, 오픈라벨, 임상 3b/4상 연구다.

이날 발표를 맡은 미국 보스턴 'Dana-Farber' 종양 연구소의 유방암 부서장이자 'DESTINY-Breast12' 연구책임자(PI) 낸시 린(Nancy Lin) 박사는 "현재 엔허투는 HER2 양성 환자와 뇌 전이 환자에 효과적이라는 임상적 증거가 확보된 상황"이라며 "이번 연구는 그 중 뇌 전이 여부에 상관없이 엔허투가 유사한 유효성 및 안전성을 확인하고자한 것"이라고 설명했다.
낸시 린 박사에 따르면, 이번 DESTINY-Breast12 연구는 코호트 1에 뇌 전이가 없는 HER2 양성 전이성 유방암 환자 241명을, 코호트 2에 △즉각적인 국소 치료가 필요하지 않으면서 치료되지 않은 뇌전이 환자 △이전에 치료를 받은 진행 중인 또는 안정적인 뇌 전이 환자를 모두 포함하면서 활동성이 있는 뇌 전이 환자 등 263명을 배정했다.
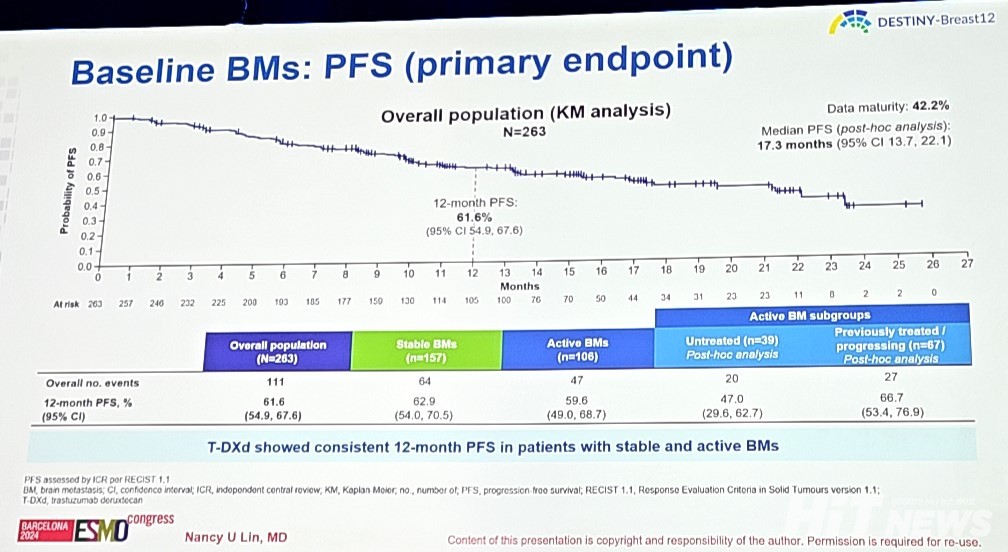
뇌 전이가 확인된 코호트 2 환자군은 일차유효성평가변수(Primary Endpoint) '12개월 시점 PFS'이 61.6%(95% CI : 54.9-67.6)로 분석됐다. 그 중 안정적인 뇌 전이 환자는 62.9%(95% CI : 54.0-70.5), 활동성 뇌 전이 환자는 59.6%(95% CI : 49.0-68.7)로 유사한 결과를 보였다.
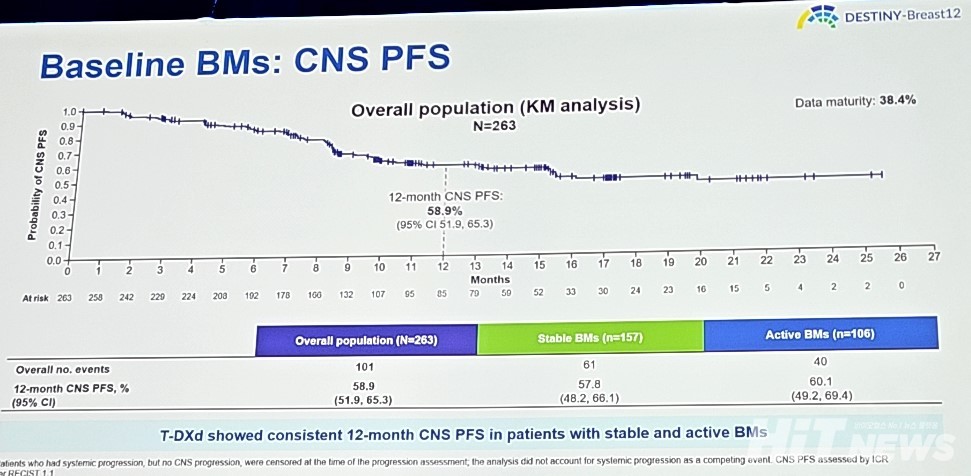
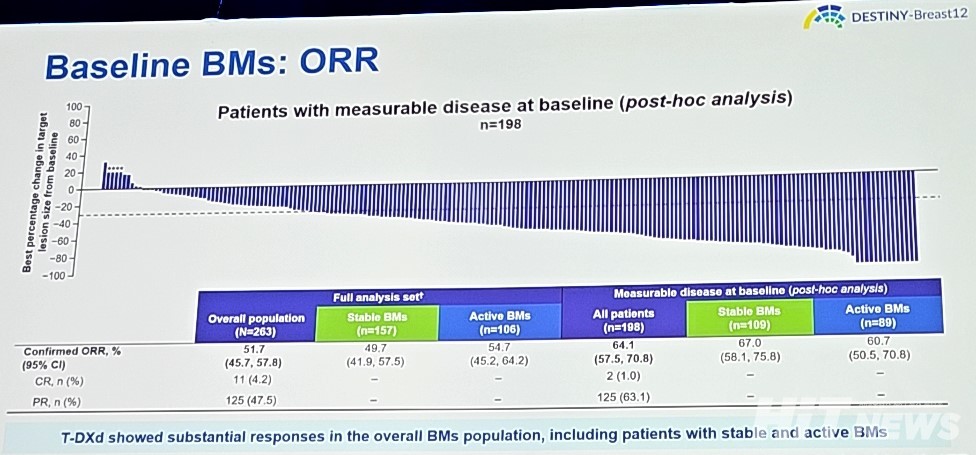
주요 이차유효성평가변수(Key Secondary Endpoint)인 '12개월 시점 중추신경계 무진행생존비율(CNS PFS)'은 58.9%(95% CI : 51.9-65.3)로, 안정적인 뇌 전이 환자 57.8%(95% CI 48.2-66.1)에서나 활동성이 있는 뇌 전이 환자(60.1%, 95% CI 49.2-69.4)에서 모두 비슷한 결과가 보고됐다. 객관적 반응률(ORR)은 51.7%(95% CI : 45.7-57.8)이었다.
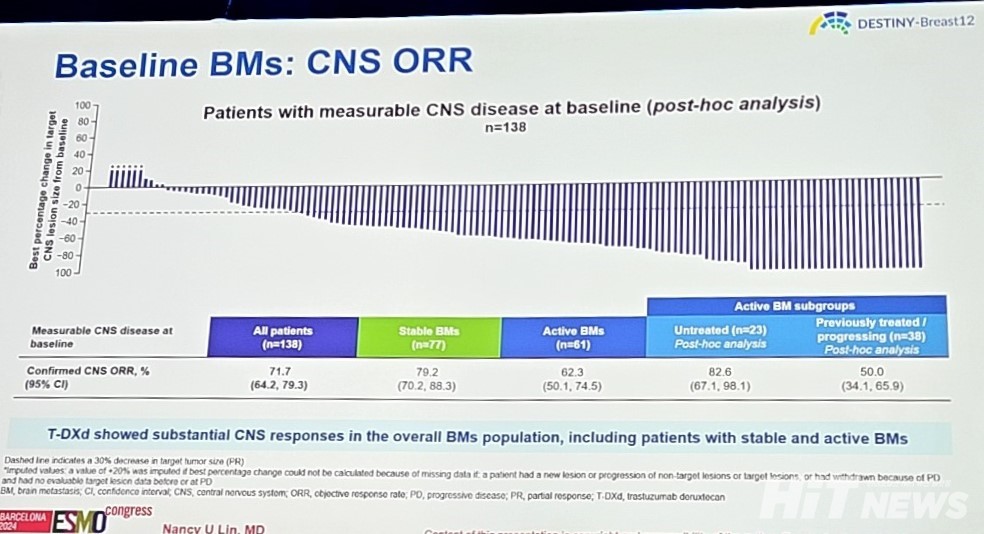
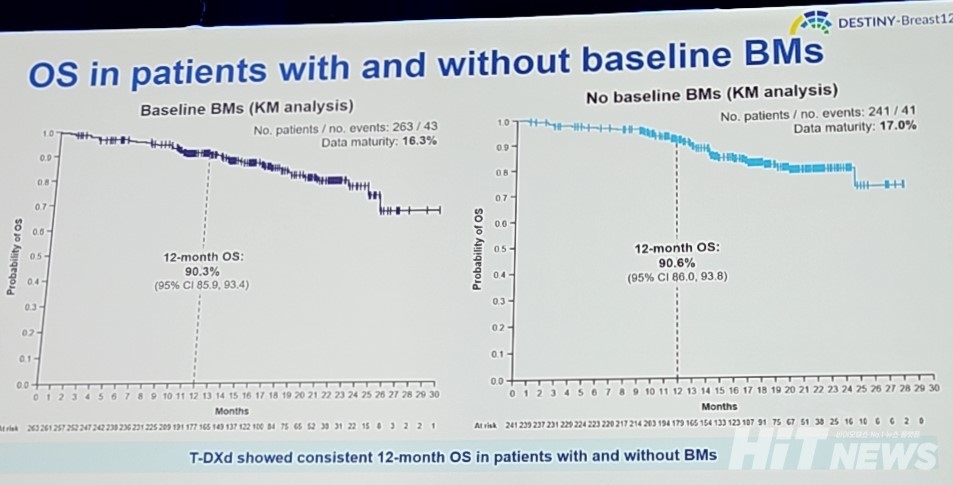
뇌 전이가 없는 코호트 1 환자군에서의 일차유효성평가변수인 ORR은 62.7%(95% CI : 56.5-68.8)로 확인됐으며, 이 중 완전 관해율(CR)은 9.5%, 부분 관해율(PR)은 53.1%였다. 또, 두 코호트 모두에서 12개월 시점의 OS는 각 90.3%(95% CI : 85.9-93.4)와 90.6%(95% CI : 86.0-93.8)로, 데이터가 아직 미성숙한 상태지만 유사하게 나타났다.
해당 연구에서 엔허투의 안전성 프로파일은 코호트 1과 코호트 2 모두 관리 가능한(Managable) 수준이었으며, 약제의 새로운 안전성 관련 보고는 없었다. 전체 이상반응 중 가장 빈번한 증상은 메스꺼움(Nausea), 피로(Fatigue) 등이었고, 3등급 이상 이상반응 중에서는 백혈구감소증(Neutropenia)이었다.
낸시 박사는 "이번 연구 결과로 엔허투는 안정한 또는 활동성 뇌전이를 가진 HER2 양성 전이성 유방암 환자에게 도움이 될 수 있다는 것을 입증했다"며 "다만, 아직 간질성 폐질환(ILD) 및 폐렴(Pneumonitis)의 안전성 문제는 중요한 숙제로 남아있다"고 말했다.
한편 그동안 HER2 양성 유방암 환자를 위한 치료 옵션은 다양하게 제시돼 왔지만, 뇌 전이 환자에서의 임상적 혜택을 제시한 약제는 제한된 상황이었다.
엔허투는 기존 허가 임상인 'DESTINY-Breast03' 연구의 뇌 전이군 82명 하위분석에서 유의미한 치료 혜택을 냈다고 발표된 바 있다. 다만, 해당 연구에는 활동성이 있는 뇌 전이 환자가 포함돼 있지 않았다.
DESTINY-Breast03 연구 뇌 전이군 하위분석 결과, 뇌 전이 환자에서 무진행생존기간 중앙값(mPFS)은 엔허투 투약군 15.0개월(95% CI : 12.5-22.2), 케싸일라(성분 트라스투주맙 엠탄신) 투약군 3.0개월(95% CI : 2.8-5.8)로, 엔허투군에서 약 5배 높게 나타났다(HR=0.25, 95% CI : 0.13-0.45). 두개 내 객관적반응률(IC-ORR)은 엔허투 투약군 65.7%, 케싸일라 투약군 34.3%로 나타났으며, ORR은 각 67.4%, 20.5%로 확인됐다.
이 외에도 엔허투는 작년 12월 샌안토니오 유방암 학술대회(SABCS 2023)에서 발표된 단일국가 임상인 'ROSET-BM' 연구와 단일기관 임상인 'TUXEDO-1' 연구에서도 뇌 전이가 있는 HER2 양성 전이성 유방암 환자에서 치료 혜택을 확인한 바 있다.
각각 20.4개월, 26.5개월 중앙 추적 관찰 기간에도 OS 데이터가 중앙값에 도달하지 못한 것으로 나타났다. 특히 TUXEDO-1 연구에서는 1차 분석 당시 활성화된 뇌 전이가 있는 HER2 양성 전이성 유방암 환자에서 IC-ORR 73.3%를 나타냈으며, 최종 분석 결과에서는 mPFS 21개월을 보였다.

