동구바이오제약·마더스제약 등 후발약 허가
한국MSD 'MK-2870' 자궁경부암 대상 3상 승인
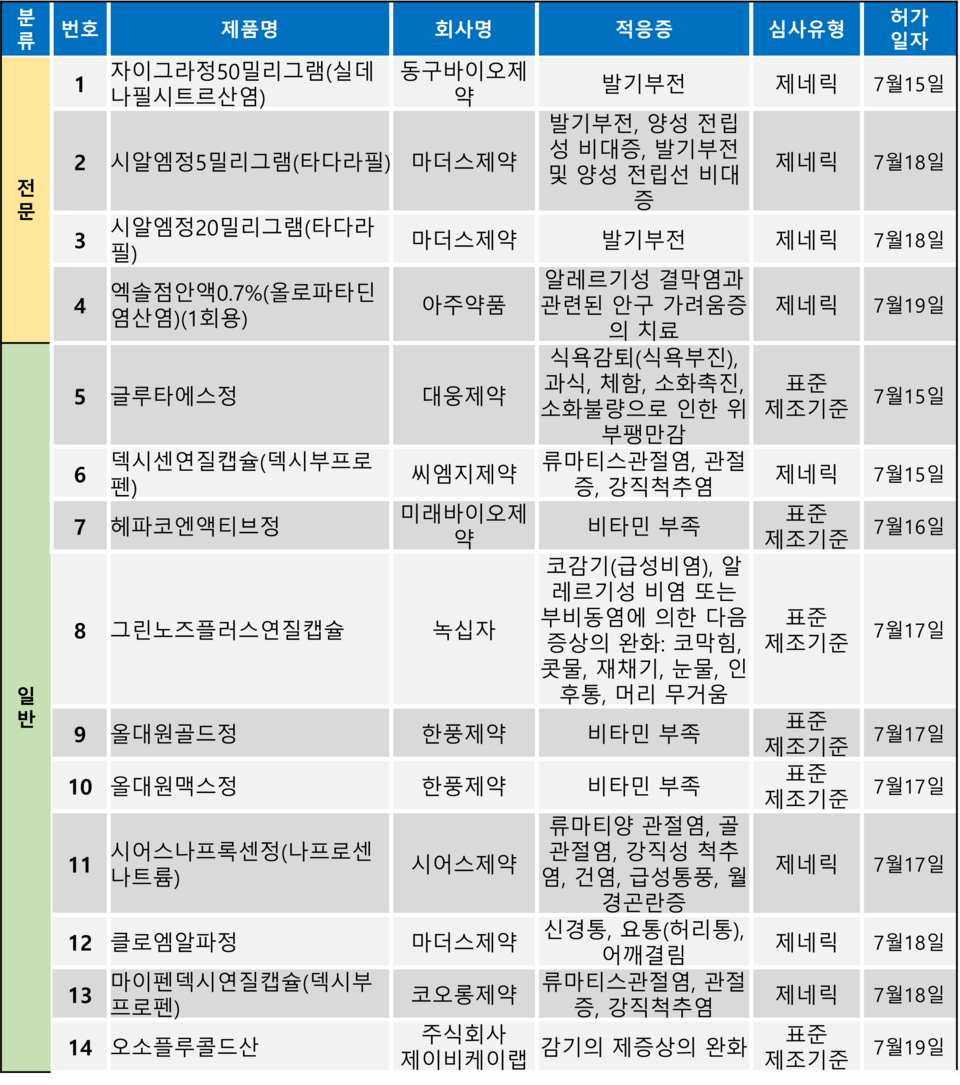
지난주(7월 15일~19일) 총 14개 품목이 식품의약품안전처에서 품목 허가를 받았다. 전문의약품은 4개 품목, 일반의약품은 10개 품목이다. 이들은 발기부전, 류마티스 관절염, 강직척추염, 신경통 등 다양한 적응증으로 허가됐다.
릴리의 '시알리스(성분 타다라필)' 후발약 2건과 화이자의 '비아그라(성분 실데나필시트르산염)' 후발약 1건 등 발기부전 치료제가 연이어 허가됐다.
식약처는 △자이그라정50밀리그램(동구바이오제약) △시알엠정5밀리그램(마더스제약) △시알엠정20밀리그램(마더스제약) 등 3개 품목이 허가됐다고 밝혔다. 해당 품목들은 모두 '발기부전'을 적응증으로 허가됐다.
실데나필시트르산염 성분 오리지널은 비아그라다. 화이자가 1998년 개발한 비아그라는 1999년 8월 국내 시판 허가를 획득했다. 이후 2012년 5월 물질 특허가 만료됨에 따라 제약사들이 약 30종의 제네릭을 출시했다.
타다라필 성분 오리지널은 시알리스다. 시알리스는 2003년 7월 수입 허가를 받아 한국릴리와 대웅제약이 공동판매하는 약이다. 2015년 9월 물질특허 만료로, 18곳에 달하는 제약사가 생동성 시험을 진행했고, △한미약품 △삼진제약 △서울제약 △씨티씨바이오 등이 시판 허가를 획득했다.
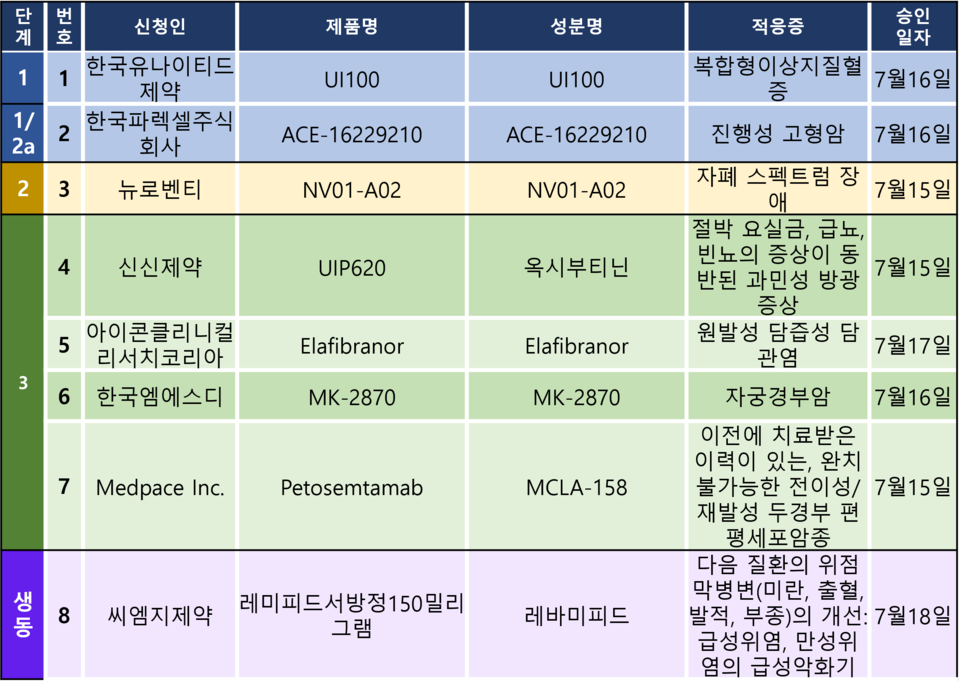
임상시험계획은 총 8건이 승인됐다. 세부적으로 △1상 1건 △1/2a상 1건 △2상 1건 △3상 4건 △생물학적 동등성 1건 등이다. 이 임상시험들은 복합형 이상지질혈증, 진행성 고형암, 자폐 스펙트럼 장애, 요실금, 자궁경부암 등을 대상으로 승인됐다.
한국 MSD가 개발하고 있는 'MK-2870'의 자궁경부암 대상 3상 임상시험계획이 지난 16일 승인됐다.
이번 3상 임상은 재발성 또는 전이성 자궁경부암을 앓고 있는 참가자에 대한 2차 선택 치료로서의 MK-2870 단독요법의 유효성과 안전성을 의사가 선택한 치료와 비교하는 무작위배정, 활성약 대조, 라벨 공개, 다기관 임상시험이다.
연구진은 △서울대학교병원 △삼성서울병원 △서울아산병원 △연세대 의대 세브란스병원 등 의료기관에서 오는 2029년 7월까지 임상시험을 진행할 예정이다.
연구의 일차유효성평가변수는 BICR을 통한 평가에서 나타난 MK-2870군에 등록된 환자에서의 RECIST 1.1에 따른 객관적 반응(완전 반응이나 부분 반응)의 비율 및 전체생존 기간(OS) 등이다.

