애드타미브플러스정, '아토르바+에제+암로디핀' 새로운 성분 조합
한국MSD, 한미약품서 기술이전해온 NASH 치료제 임상 2b상 승인
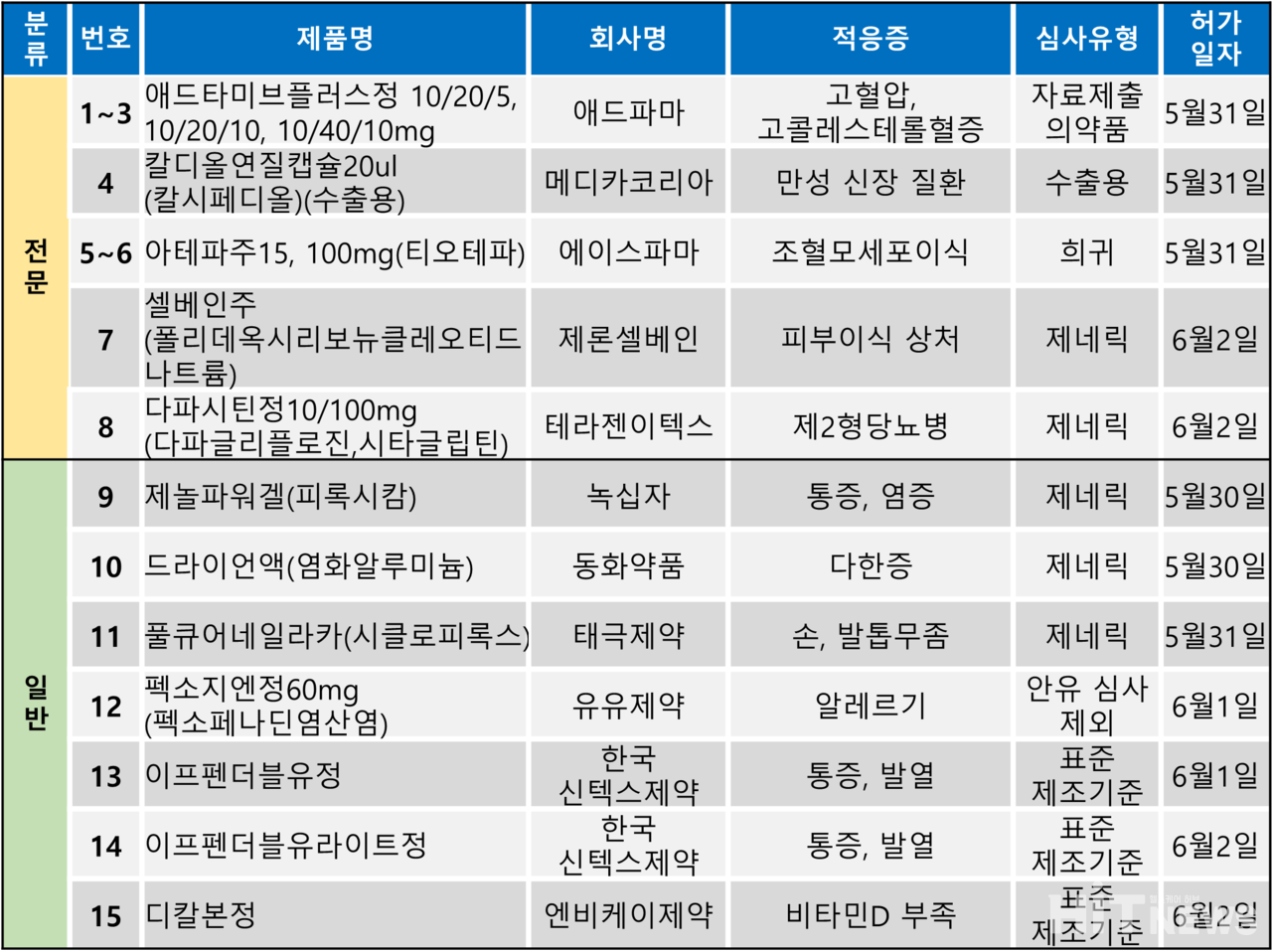
지난주(5월 29~6월 2일)에는 총 15개 품목이 식품의약품안전처로부터 품목 허가를 받았다. 전문의약품은 8개 품목, 일반의약품은 7개 품목이었다. 허가 품목들은 △제2형 당뇨병 △고혈압 △신장 투석으로 인한 만성 신장 질환 △피부 이식 등으로 발생한 상처 등 다양한 적응증으로 허가됐다.
유한양행 자(子)회사 애드파마가 지난달 31일 '아토르바스타틴+에제티미브+암로디핀'으로 구성된 새로운 조합의 고혈압·고지혈증 치료제 '애드타미브플러스정'을 허가받았다. 식약처는 암로디핀과 에제티미브+아토르바스타틴 복합제를 동시에 투여해야 하는 환자에 한정해서 사용할 수 있도록 허가했다. 허가 용량(에제티미브·아토르바스타틴·암로디핀)은 10/20/5, 10/20/10, 10/40/10㎎ 등 3개며, 수탁 제조는 유한양행이 맡는다.
애드타미브플러스정은 고지혈증 치료제로 사용되는 아토르바스타틴과 에제티미브에 고혈압 치료 성분 암로디핀으로 구성된 3제 복합제다. 기존에 허가된 3제 고혈압·고지혈증 복합제들은 △스타틴(콜레스테롤 합성 저해제)+사르탄(ARB·안지오텐신Ⅱ 수용체 차단제)+암로디핀(CCB·칼슘채널차단제) △스타틴+사르탄+에제티미브(콜레스테롤 흡수 저해제) 등으로 구성돼 왔다.
현재까지 허가된 3제 고혈압·고지혈증 복합제 조합별 대표 품목으로는 △보령 '듀카로(로수바스타틴+피마사르탄+암로디핀)' △한미약품 '아모잘탄큐(로수바스타틴+로사르탄+암로디핀)' △일동제약 '텔로스톱플러스(로수바스타틴+텔미사르탄+암로디핀)' △HK이노엔 '엑스원알(로수바스타틴+발사르탄+암로디핀)' △녹십자 '로제텔(로수바스타틴+로사르탄+에제티미브)' △유한양행 '듀오웰플러스(로수바스타틴+텔미사르탄+에제티미브)' △종근당 '칸타벨에이(아토르바스타틴+칸데사르탄+암로디핀)' 등이 있다.
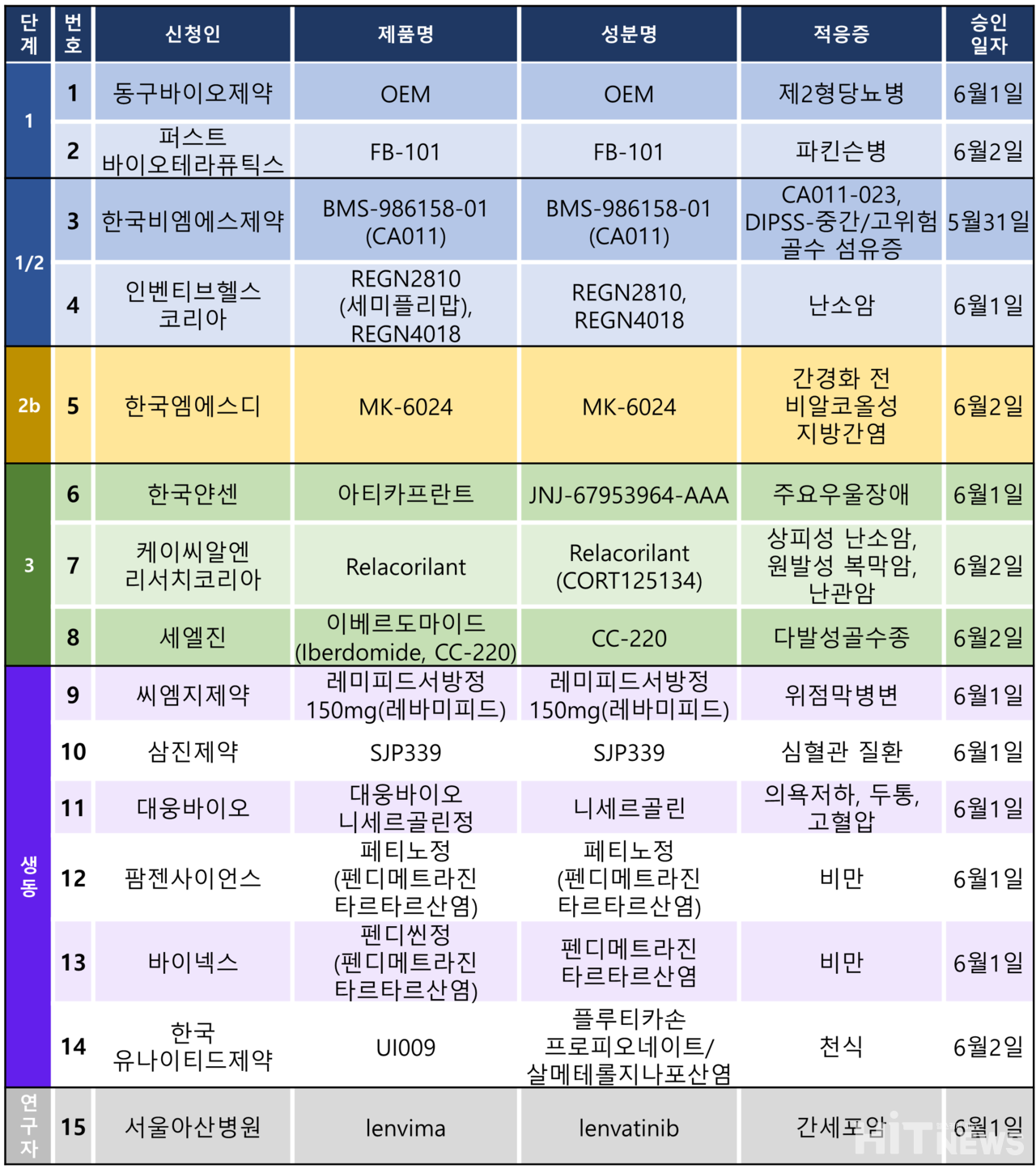
지난주 임상시험계획은 총 15건이 승인됐다. 세부적으로 △임상 1상 2건 △임상 1/2상 2건 △임상 2b상 1건 △임상 3상 3건 △생물학적동등성시험 6건 △연구자임상 1건 등이다.
이 임상시험들은 제2형 당뇨병, 파킨슨병, 비알코올성 지방간염(NASH), 우울 장애, 골수 섬유종 등 질환과 난소암, 복막암, 난관암, 다발성 골수종 등 암종을 대상으로 승인됐다.
한국엠에스디(한국MSD)가 개발하고 있는 NASH 치료 후보물질 'MK-6024(성분 에피노페그듀타이드)'의 2b상 임상시험계획이 지난 2일 승인됐다. 회사는 2021년 7월 임상 2a상을 승인받고 연구를 진행해 왔다.
이번 임상 2b상은 간경화 전 NASH를 앓고 있는 성인을 대상으로 에피노페그듀타이드의 유효성과 안전성을 평가하기 위한 무작위배정, 이중눈가림, 위약 대조, 다기관 임상 연구다. 삼성서울병원, 연세대 의대 세브란스병원, 인하대 의대 부속병원, 서울 보라매병원 등 5개 의료기관에서 진행된다.
MSD는 지난 2020년 8월 한미약품 LAPS GLP/Glucagon 수용체 이중 작용제(dual agonist) 'HM12525A'을 MK-6024라는 프로젝트명으로 기술이전 해왔다. HM12525A는 GLP-1과 글루카곤을 동시에 활성화하는 이중 작용제에 한미약품의 바이오의약품 약효 지속 플랫폼 '랩스커버리' 기술이 적용된 물질이다.
당시 계약으로 MSD는 한국을 제외한 국가에서의 개발 및 상업화 권리를 확보했다. 확정된 계약금은 1000만달러였으며, 한미약품은 추후 개발 단계에 따른 마일스톤으로 최대 8억6000만달러를, 상업화 이후에는 두 자리 퍼센트의 로열티를 수령하도록 계약했다.

