식약처, 사르탄류 NDMA·NDEA 잠정관리기준 설정 및 시험법 교육

식품의약품안전처(처장 류영진) 식품의약품안전평가원은 발사르탄 등 사르탄류 고혈압약의 불순물 관리를 위해 'N-니트로소디에틸아민(NDEA)' 잠정관리기준을 설정, 시험법을 공개하고 시험검사기관 및 업체 등에 시험법 교육을 실시한다고 21일 밝혔다.
안전평가원은 지난 8월과 10월, 발사르탄 및 발사르탄과 구조가 유사한 사르탄류에 대한 NDMA 잠정기준 설정 및 시험법을 공개한 바 있다.
발사르탄과 구조가 유사한 사르탄류로 로사르탄, 올메사르탄, 이르베사르탄, 칸데사르탄, 피마사르탄이 있다.
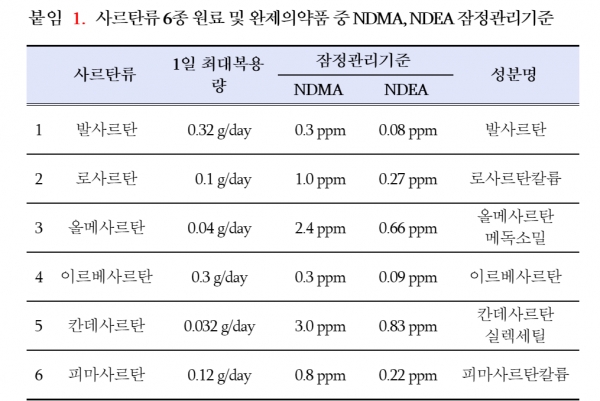
식약처는 발사르탄의 1일 최대 복용량은 0.32g을 기준으로, NDMA는 0.3 ppm, NDEA는 0.08ppm을 기준으로 잡았다.로사르탄은 1일 최대 0.1g 기준 NDMA로 1.0 ppm, NDEA는 0.27 ppm이며 올메사르탄은 0.04g 기준 NDMA 2.4 ppm, NDEA 0.66 ppm 이하로 관리해야 한다.
이르베사르탄은 0.3g 기준, NDMA 0.3 ppm, NDEA 0.09 ppm이어야 한다. 칸데사르탄은 0.032g 기준 NDMA 3.0 ppm, NDEA 0.83 ppm, 피마사르탄은 0.12g 기준 NDMA 0.8ppm NDEA 0.22ppm이 된다.
식약처는 "쥐에서 종양발생률이 50%인 용량을 일컫는 독성정보(TD50(rat)*)에 근거한 사람(50kg)에서 NDMA 및 NDEA의 1일 섭취허용량은 각각 0.0959µg/day 및 0.0265µg/day이다"고 밝혔다.
이는 체중 50kg인 사람이 매일 사르탄류 의약품 1일 최대 복용량을 평생(70년) 복용할 때, 자연발생적인 발암가능성에 더해 10만분의 1의 확률로 암이 더 발생할 수 있는 NDMA 또는 NDEA 섭취 허용량을 의미한다고 설명했다.
식약처는 잠정관리기준이 국가별로 다를 수 있으나 사르탄류 제제별 1일 최대복용량을 고려해 산출했다고 했다. 설정한 NDEA 기준은 국제의약품규제조화위원회(ICH)가 권고하는 가이드라인(ICH M7)과 외국 규제당국과의 논의를 거쳐 설정했으며, 중앙약사심의위원회의 자문을 통해 확정했다.
중앙약심은 "유럽의약품안전청(EMA)과 일본후생노동성(MHLW) 등 해외 규제기관에서도 NDMA와 NDEA에 대해 1일 섭취허용량을 동일하게 설정하고 있는 점 등을 감안할 때 잠정관리기준 설정은 타당하다"고 자문했다.
식약처는 이에 앞서 업체 및 시험분석기관에서 사르탄 계열 의약품에서 NDMA와 NDEA을 동시에 분석할 수 있는 시험법을 개발해 홈페이지에 공개했다.
이 시험법은 사르탄류 6종의 원료 및 완제의약품을 대상으로 질량분석기(LC-MS/MS)를 이용한 방법으로, 식약처는 21일 오후 2시에 한국제약바이오협회 2층 K회의실에서 시험검사기관과 업체 등을 대상으로 분석법 교육을 실시할 계획이다.

