펙수클루 동시출격 전략 위한 대비까지
레스타시스 개량신약 2상에…레보드로프로피진 생동성 강세
12월 두 번째 주 허가받은 의약품은 총 27건으로 전문의약품 19건, 일반의약품 8건이다.
전문의약품 중 가장 먼저 보이는 품목은 대웅바이오의 베나보정과 한올바이오파마의 이글렉스정(성분명 이나보글리플로진)이다. 성분에서 알 수 있듯이 해당 품목은 얼마 전 국내 허가를 받은 대웅제약의 나트륨-포도당 공동 수송체-2(SGLT-2) 억제제 계열의 약제인 국산 신약 36호 엔블로의 쌍둥이 제품이다.
대웅의 쌍둥이약 출격 작전은 앞서 나왔던 역류성식도염 치료제 '펙수클루'에서도 확인할 수 있다. 회사는 펙수클루 출시 후 대웅바이오, 한올바이오파마 심지어 스핀아웃인 대웅제약의 자회사 아이엔테라퓨틱스까지 회사별 특징에 맞춰 쌍둥이약을 출시했다.
당시 대웅제약이 가장 큰 종합병원급 수준의 의료기관을 맡고 타 회사가 각각 병원급, 로컬급(지역 개원가) 등을 맡으며 전담마크 작전을 펼쳤다. 해당 제품의 출시 역시 어느 정도는 이같은 가능성을 내포하고 있는 셈이다. 문제는 최근 펙수클루가 보험약가 이야기가 슬슬 오가고 있다는 점이다.
나머지 제품이 대웅의 서류를 토대로 제출한 형태의 자료제출의약품이기 때문이다. 대웅제약과 다른 회사의 관계를 '타사'로 볼 경우 제품의 약가 인하 가능성이 높아지기 때문이다.
이를 막기 위해 대웅제약 측은 허가 과정에서 이들의 제품을 '신약' 분류로 허가받았는데 엔블로와 베나보, 이글렉스 등은 다른 방향으로 문제를 풀어갈 수 있을지 주목된다.
이런 가운데 허가가 이어지고 있는 신구 경구용 항응고제(NOAC) 계열의 한국다이이찌산쿄 릭시아나(에독사반) 제네릭도 이어지고 있다.
12월 2주차에도 한국휴텍스제약과 한독이 각각 엔시아나와 메가사반을 허가받으면서 향후 시장 출시를 위한 준비를 서두르고 있다. 제뉴파마 역시 제뉴파마에독사반정을 허가받았다. 현재 릭시아나에는 2026년 11월 10일 만료되는 디아민 유도체 특허(물질 관련)와 2028년 8월 21일 만료되는 의약 조성물 특허가 각각 있다.
이 중 2028년 조성물 특허는 국내사가 회피에 성공한 상황. 이후 2026년 앞서 나온 물질특허가 끝나는 시점에 제품을 갖춰놓으려는 선행적 움직임이기도 하다.
이 밖에 또다른 SGLT-2 억제제인 포시가(다파글리플로진)와 메트포르민 복합제인 직듀오서방정 등의 제네릭 역시 허가를 받았다.
일반의약품 중에는 6일 허가받은 한풍제약의 '비맥스에버플러스정'이 눈에 띈다. 한풍제약은 GC녹십자의 활성비타민제인 비맥스 제품군의 제조를 맡고 있는 회사다. 비맥스에버플러스는 지난 2020년 출시된 비맥스에버의 업그레이드판이다.
지난 2020년 10월 한풍제약은 기존 비타민제제에 한방 성분인 당귀, 작약, 황기, 녹용 등을 포함한 비맥스에버를 출시했다. 다만 시장 반응은 그다지 좋지 못했다. 주력 상품이 아니라는 아쉬움은 있지만 의약품 시장조사기관 아이큐비아 기준 올해 3분기까지의 매출은 20억 원 남짓에 불과하다. 전년 22억 원보다도 감소한 셈이다.
이런 가운데 로얄젤리 등을 넣은 새로운 제품을 추가로 출시하면서 시장에 진입하려 할 가능성이 높다는 점에 흥미를 가지고 지켜볼 만하다.
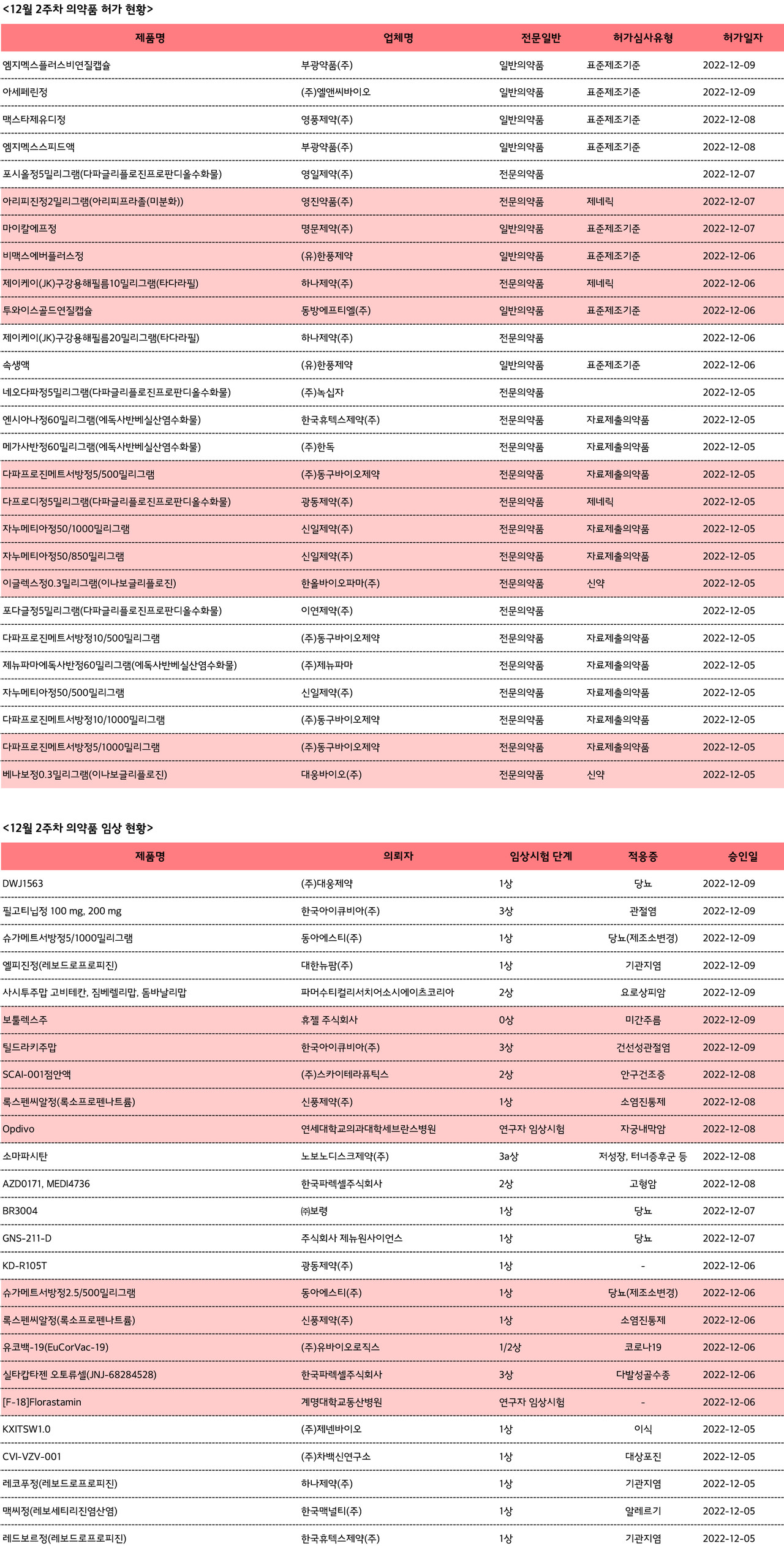
같은 기간 임상은 총 25건 진행됐다. 이 중 18건은 제약사의 임상이었고 임상수탁업체(CRO)의 대행건수는 5건, 나머지 2건은 의료기관에서 각각 승인을 받았다.
여기에서도 눈에 보이는 임상은 대웅제약의 DWJ1563이다. 엔블로가 출시된 지 얼마 되지 않았지만 회사는 엔블로와 함께 제미글로(제미글립틴)의 복합제 임상을 진행중이다. 이를 통해 약물 농도 등을 판단한다는 계획이다.
오랜만에 안구건조증 치료제 임상 승인도 나왔다. 스카이테라퓨틱스는 SCAI-001의 2상을 지난 8일 승인받았다. 해당 치료제는 기존 사이클로스포린 0.05% 제제에 생체이용률 향상 기술 '모아시스'를 적용한 개량신약으로 적은 용량으로 부형제를 줄이면서도 치료효과를 보일 수 있다는 데서 기대를 모으고 있다.
임상수탁업체의 임상 중에는 지난 2018년 3월 미국에 등장한 건선치료제 일루미아(미국 제품명, 틸드라키주맙)의 3상이 있다. 한국아이큐비아가 진행하는 이번 임상에서 회사는 건선성 관절염의 장기 안전성 및 효과성을 확인하기 위한 연장시험을 진행한다.
휴젤은 여러 이슈 속에도 자사의 보툴리눔톡신 보툴렉스의 미간주름 임상의 투여용량 및 미간 주름 효과 확인을 위한 임상을 진행할 예정이다.
이 밖에 파마수티컬리서치에서 진행하는 길리어드의 사시투주맙 고비테칸, 짐베렐리맙, 돔바닐리맙의 요로상피암 임상도 있다. 이번 2상에서는 절제 불능성 국소 진행성/전이성 요로상피암에서 객관절반응률 및 무진행생존을 확인하는 절차가 진행된다.
여기에 생물학적 동등성시험 중에는 레보드로프로피진 대상 건이 총 3건을 차지했다. 대한뉴팜과 한국휴텍스제약, 하나제약이 각각 코오롱제약의 드로피진을 대상으로 생물학적 동등성을 확인할 계획이다.
또 보령이 디펩티딜 펩티다제-4(DPP-4) 억제제 계열 당뇨치료제인 트라젠타(리나글립틴)과 메트포르민을 복합한 '트라젠타 듀오'의 후발 제제 개발을 시작한다.
관련기사
- [허가/임상] 눈에 띄는 포시가 제네릭들과 신약 엔블로
- [허가/임상] 발베사정, 희귀의약품으로 허가
- [허가/임상] 내년 특허만료 '다파+메트포르민' 후발약 허가
- [허가/임상] 알듀카정 등 듀카브 제네릭 등장… 생동 강세 여전
- [허가/임상] 4월출시 막차 탄 '포시가' 후발, 11년 기다린 '보술리프'
- 첫 도전 5년 만에 깨진 '700억원대 릭시아나' 물질 특허
- Lixiana’s NCE Patent Worth $70 Million Broken after First Challenge in 5 Years
- 한풍제약, 중국 '천사력제약' 방문…'심적환' 제조기업과 교류 목적

