포스테오·테로사 동일 성분이지만 바이오의약품으로 달라
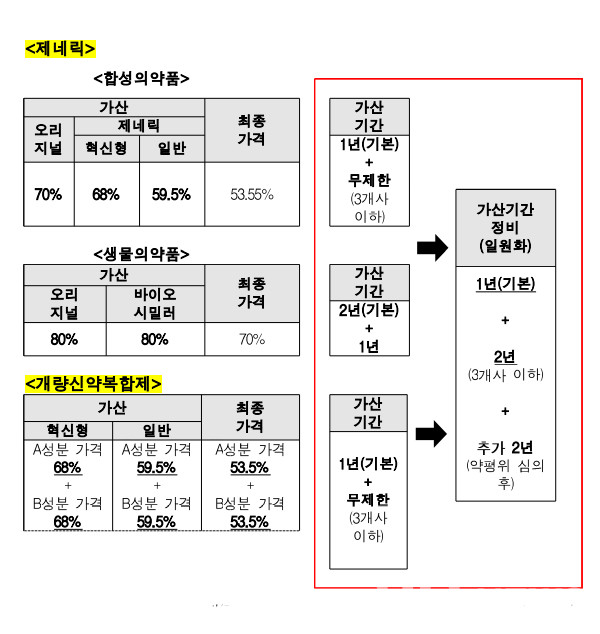
약평위 통해 추가 2년 연장 결정
동아ST의 '테리본'이 3년 가산기간 종료를 앞두고 있어 재평가를 통해 가산기간 연장이 가능할지 관심을 모은다.
동일한 성분의 바이오의약품은 있지만 합성의약품은 테리본이 유일해 가산유지 가능성도 있는 것으로 예상된다.
3일 관련업계에 따르면 건강보험심사평가원은 2023년 가산기간 3년 종료 예정인 약제에 대한 재평가를 올해 시행한다. 올해 대상품목은 24개로 평가 대상 약제는 가산종료 예정 월이 속한 분기 시작시점을 기준으로 약 9개월 전에 안내된다.
테리본의 가산종료일은 2023년 1월 31일까지로, 가산재평가가 진행 중이다.
지난해 개편된 가산제도에 따르면 기본 가산기간은 1년이고, 3개사 이하일 경우 2년이 추가된다. 약제급여평가위원회 심의에 따라 추가 2년 적용이 가능하다.
테리본은 3년 가산기간이 적용됐기 때문에 가산 종료여부를 살펴봐야 한다.
현재 테리본은 '테리파라타이드' 성분의 골다공증치료제로, 같은 성분 약에는 릴리의 '포스테오'와 대원제약의 '테로사' 등이 있다.
포스테오와 테로사는 바이오의약품인 반면 테리본은 염을 붙인 합성의약품으로, 동일 제품을 가진 회사 수를 분리해서 볼 수 있다.
다만, 포스테오의 바이오시밀러인 테로사가 급여등재될 지난 2020년 당시 테리본의 약가도 같이 조정된 바 있다.
가산 재평가는 △가산유지 신청사유 △대체약제 여부 △진료상 필수 여부 △추가 소요비용 △동일제제 등재현황 등의 자료를 검토해 가산 유지여부를 결정된다.
최근 사후평가소위원회에서 테리본의 경우 테리파라타이드 성분 유일한 합성의약품으로 검토됨에 따라 가산 유지 가능성도 커지고 있다.
재평가를 통해 가산기간이 늘어날 경우 테리본의 가산은 최대 2년까지 연장 가능할 것으로 전망된다.