식약처, '중대한 이상사례 검토‧처리 지침서'·'장기추적조사 지정 해제 절차' 마련

첨단바이오의약품 장기추적조사를 체계적으로 운영하기 위한 '중대한 이상사례 검토‧처리 지침서' 및 '장기추적조사 지정 해제 절차'가 31일 발간됐다.
첨단바이오의약품 장기추적조사는 줄기세포 또는 유전물질을 포함하는 첨단바이오의약품을 투여받은 환자의 안전을 위해 투여 후 장기간에 걸쳐 이상사례 발생 여부를 추적‧조사하는 것을 말한다. 조사 기간은 △줄기세포치료제(5년) △유전자치료제(15년) △이종이식제제(30년) 등이다.
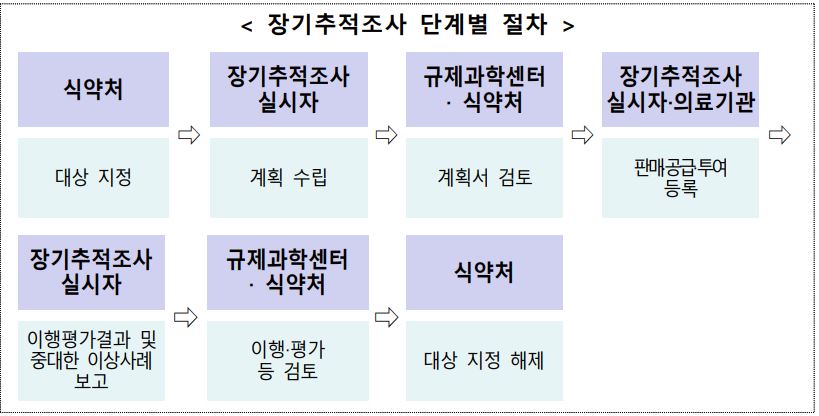
이번 지침서 발간 책임자인 김상현 식품의약품안전처 바이오생약국 첨단바이오의약품TF 팀장은 "국내 제약사, 개발사가 장기추적조사 계획을 수립‧실시하는 데 도움을 주기 위해 해당 업무의 처리 절차를 안내한 '중대한 이상사례 검토‧처리 지침서'를 마련했다"고 밝혔다.
지침서 주요 내용은 △관련 규정‧가이드라인 △적용범위 △용어 정의 △검토 자료‧절차 흐름도 등 검토지침 △접수‧검토‧보완‧결과회신 등 검토 절차로 구성돼 있다.
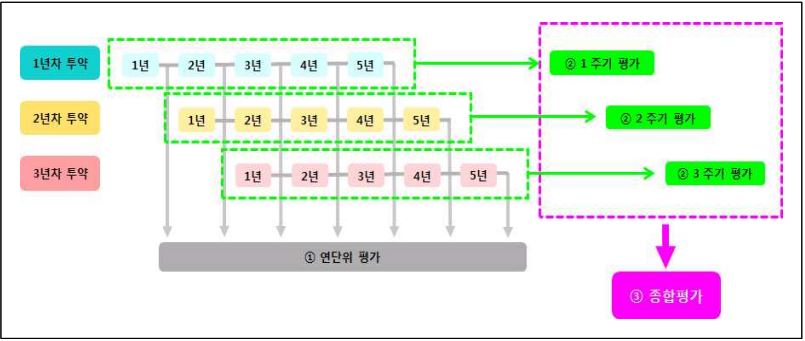
김상현 팀장은 또한 "추적‧평가 3주기가 종료된 첨단바이오의약품의 장기추적조사 결과를 종합적으로 평가하여 장기추적조사 지속 여부를 결정하도록 하는 '장기추적조사 지정 해제 절차'도 마련했다"고 설명했다.
예를 들어 추적조사 지정기간이 5년인 경우 3주기 종료 후, 15년간의 3세트 추적조사 결과를 종합해 평가해야 한다.
지침서 주요 내용은 △지정해제 검토대상 △평가자료 △종합평가‧지정해제 절차 등이다. 식약처는 향후 안정적인 운영을 위해 '첨단바이오의약품 장기추적조사 관리기준(식약처고시)'에도 해당 절차를 반영할 것이라는 입장이다.
한편, 식약처는 지난해 9월 첨단바이오의약품 장기추적조사 제도의 안정적 정착을 위해 '첨단바이오의약품 장기추적조사 실시 절차 안내서'를 발간한 바 있다.

