식약처, MCL 치료제 브루킨사캡슐 승인
3주 간격 2회 접종...화이자 코로나19 소아백신
SK바이오팜 세노바메이트 적응증 확대

중국 제약사 베이진의 한국지사 첫번째 국내 품목허가 의약품이 나왔다. 식품의약품안전처는 베이진코리아의 외투세포 림프종(MCL)치료제 '브루킨사캡슐80밀리그람(자누브루티닙)' 품목허가를 승인했다.
한국화이자제약은 소아(5~11세)용 코로나19 백신 '코미나티주0.1mg/mL' 품목허가를 획득했다.
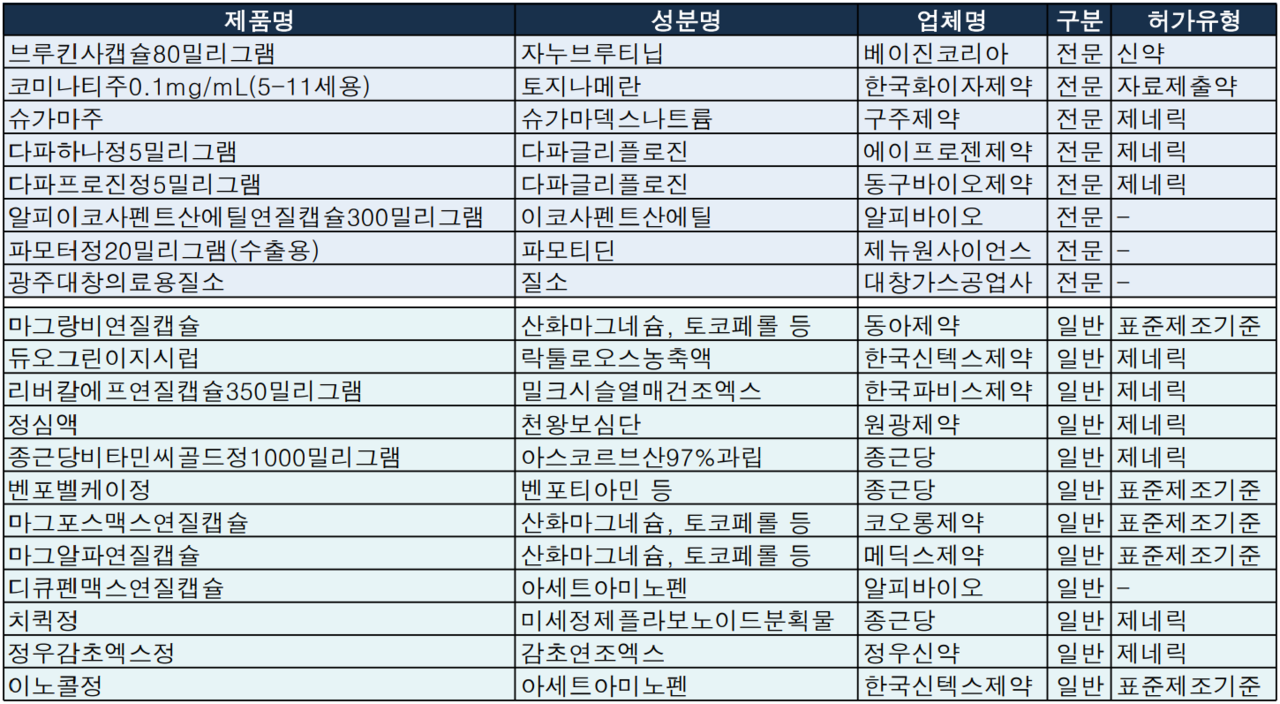
지난주(2022.02.21~2022.02.27) 식약처는 의약품 20품목(전문약: 8개, 일반약: 12개), 임상시험 27건(1상: 21개, 2상: 1개, 3상: 2개, 연구자: 3개)을 각각 승인했다.
베이진 첫 품목 국내 진입
3주 간격 2회 접종...화이자의 코로나19 소아백신
한국화이자제약의 코미나티주는 0.2mL로 희석된 백시늘 3주 간격 2회 투약하는 소아용 코로나19 백신이다. 허가사항에 따르면 중증 면역저하자의 경우 2차 투여 후 3차 접종은 가능하며 다른 백신과의 호환성은 아직 확인되지 않았다.
식약처에 따르면 코미나티주는 미국, 유럽, 호주, 캐나다 등 62개국에서 허가 또는 긴급사용승인을 획득한 바 있다.
베이진의 브루킨사캡슐80밀리그램은 BTK(Bruton’s tyrosine kinase) 억제제로 한 가지 이상의 치료를 받은 적 있는 MCL 및 발덴스트롬 마크로글로불린혈증(WM) 2차 단독 요법으로 품목허가를 획득했다.
자체개발신약으로 앞서 2019년 FDA 품목허가를 승인받았으며 2021년 11월 EMA 퓸목허가를 획득하기도 했다. 최근에는 만성 림프구성 백혈병을 적응증으로 FDA 승인에 도전하고 있다.
SK바이오팜 세노바메이트 적응증 확대
SK바이오팜이 뇌전증 치료성분 '세노마메이트' 적응증 확대에 시동을 걸었다. 이번에 승인받은 임상시험 3상은 부분 발현 발작이 있는 소아 140명(국내 10명)을 대상으로 진행되며 고대 구로병원, 서울대병원, 보라매병원, 아주대병원, 세브란스병원, 충북대병원 등이 실시한다.
앞서 SK바이오팜은 한국, 중국, 일본 등 아시아 성인 환자 540명을 대상으로 부분 발작 치료에 대한 임상시험 3상을 승인받은 바 있는데, 이번 임상시험 승인으로 지역외 연령군을 넓히는 전방위 적응증 확대에 나서는 모양새다.
임상시험 수탁기관인 한국아이큐비아는 아밀로이드증 치료물질 'CAEL-101' 임상시험 3상을 승인받았다.
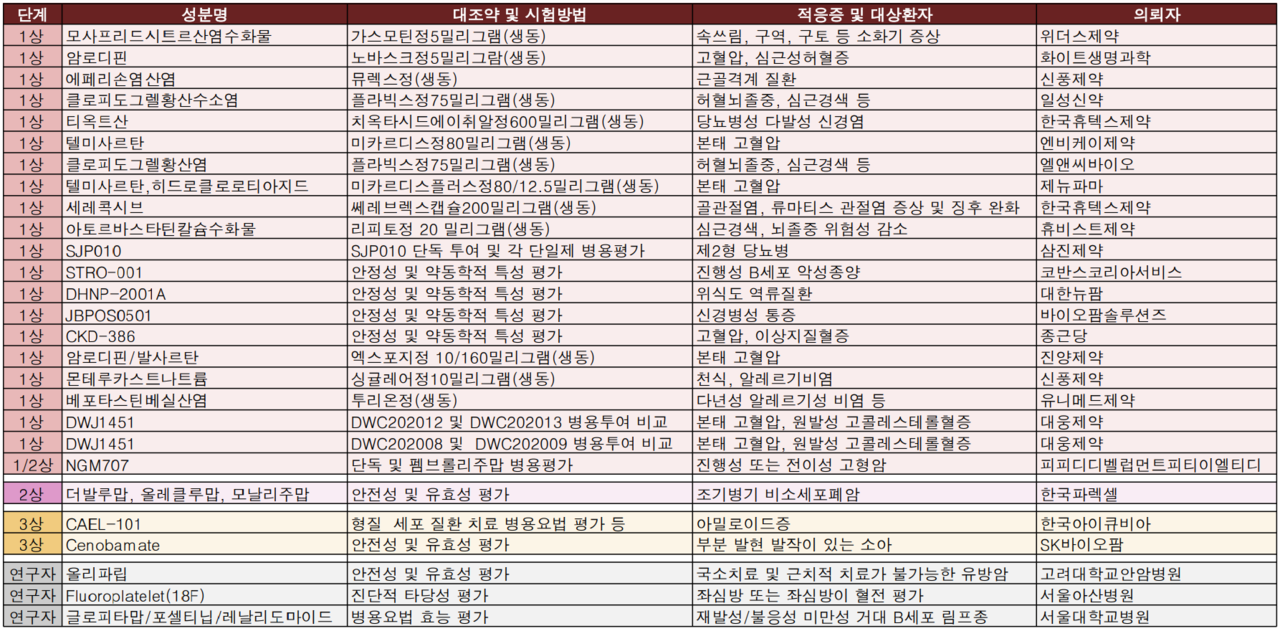
승인내역에 따르면 대상환자는 Mayo stage IIIb AL 아밀로이드증이 있으며 형질 세포 질환 치료 경험이 없는 시험대상자 111명(국내 10명)으로, CAEL-101 과 형질 세포 질환 치료 병용요법을 평가할 예정으로, 삼성서울병원, 서울대학교병원, 세브란스병원, 서울성모병원이 실시한다.

