약평위-건정심-고시까지 3분기 안에 종료 예상
비티스비니페라 등 5개 성분에 대한 임상적 유용성 자료제출 기한이 완료됨에 따라 남은 급여적정성 재평가 일정에 관심이 모인다.
관련업계에 따르면 건강보험심사평가원이 비티스비니페라, 아보카도-소야, 은행엽엑스, 빌베리건조엑스, 실리마린 등 5개 성분을 보유한 제약사들에게 자료제출 요청을 요구한 기한은 지난 19일까지다.
임상적 유용성, 비용효과성, 사회적 요구도 등의 급여적정성을 평가할 수 있는 자료를 제출하라는 것이다.
지난달 건강보험정책심의위원회에 보고된 내용에 따르면 5개 성분은 A8 국가 중 1개국 이하로 급여등재 돼 있고 주요외국에서는 건강기능식품으로 분류되고 있는 만큼, 제약사들이 추가로 제출한 자료는 많이 없는 것으로 알려진다.
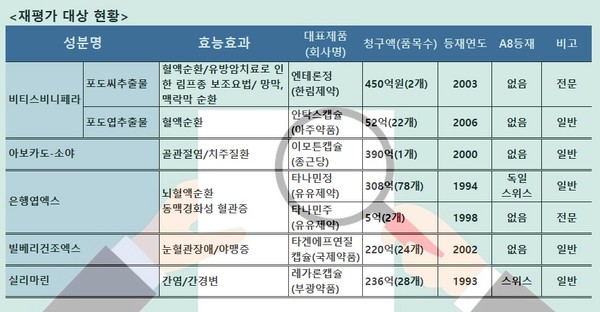
이 과정에서 유유제약과 위더스제약은 은행엽엑스 주사제인 타나민주와 트나민주를 취하하기도 했다.
자료제출 기한이 종료되면서 심평원의 검토, 건정심 보고, 고시 등의 일정이 진행될 것으로 보인다.
앞서 진행된 콜린알포세레이트 급여적정성 재평가 일정을 비교해보면, 심평원은 사후평가소위원회를 열어 임상적 유용성을 살펴봤다.
이후 약제급여평가위원회에서 급여적정성에 대해 논의했다. 콜린의 경우 적응증별 선별급여를 적용하는 것으로 결정됐는데, 5개 성분도 선별급여를 적용할지, 급여권에서 제외할지 지켜봐야 한다.
심평원은 평가 내용을 제약사에 통보한 후 30일 이의신청을 받았고, 이를 검토한 후 사후평가소위원회와 약평위에 재상정했다. 이때 이의신청 기회는 1번이다.
약평위 재검토 이후 건정심 보고를 거쳐 고시 발령됐다.
날짜로 보면, 작년 5월 임상적 유용성 자료제출, 6월 심평원 사후평가소위원회 및 약평위 급여적정성 평가, 7월 제약사 이의신청, 7월 말 약평위 재검토, 건정심 보고, 9월 급여기준 개정으로 4개월 일정으로 진행됐다.
이번 5개 성분 급여적정성 재평가도 이 같은 일정을 밟을 것으로 보이며 복지부에서 밝힌 바와 같이 3분기까지 마무리될 것으로 전망된다.
국내 제약사 관계자는 "일부 회사가 실리마린 관련 자료를 제출한 것으로 알고 있다. A8 등재된 나라도 없고 대부분 일반약으로 허가받아 회사들이 추가로 제출할 수 있는 국내외 자료는 많지 않다"며 "앞으로의 진행과정을 지켜보면서 대응방안을 찾아야 하는 상황"이라고 전했다.

