식약처, 무균 생동 재평가 첫해 '속도 조절'…면제 트랙 가동
현장 부담 완화·수급 리스크 관리 방점

식품의약품안전처가 무균제제 생물학적동등성 재평가에 착수하면서 자료 제출 기한 유예, 일부 품목 재평가 면제, 제출자료 완화 방안을 동시에 내놓았다.
올해 용액 주사제를 시작으로 무균제제 재평가를 본격화하되 히알루론산 제제와 일부 대용량 수액제 등 75개 품목은 제외하고, 1차 자료 제출 시한도 6월 말까지 늦추기로 했다.
30일 식약처는 서울 명동 포스트타워에서 열린 '의약품 시판 후 안전 관리 정책 설명회'에서 시판 후 의약품 품질 신뢰도 제고를 위해 운영 중인 동등성 재평가 제도의 추진 경과와 향후 계획을 공개했다.
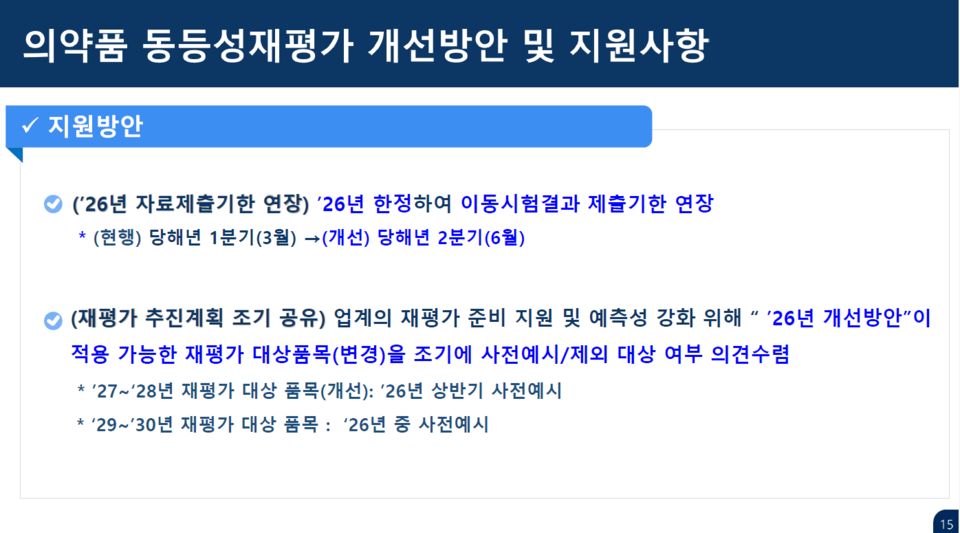
1차 자료 제출 기한을 3월 말에서 6월 말까지 유예
식약처는 2007년부터 동등성 재평가 제도를 운영해 왔으며 2020년 총리령 개정을 통해 전 성분·전 제형으로 확대 적용하는 중장기 계획을 수립했다. 이후 2023년부터 2025년까지 경구제를 대상으로 재평가를 진행해왔다.
정명훈 사무관은 "2023년 정제 재평가가 완료됐고, 2024년 필름코팅정도 일부 허가 변경 품목을 제외하면 대부분 마무리 단계"라며 "2025년 캡슐제 등은 약 80% 수준까지 진행되며 제도 안착이 이뤄졌다"고 설명했다.
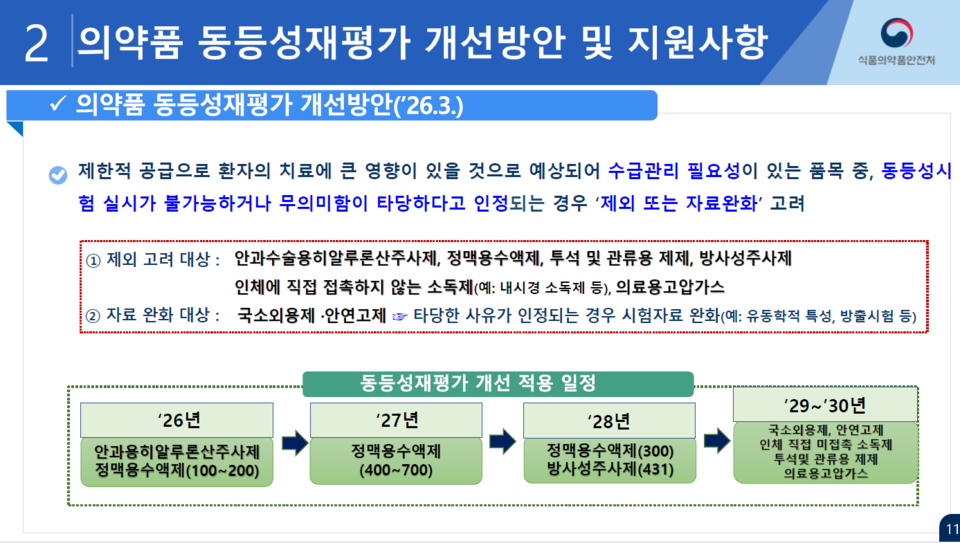
식약처는 경구제 재평가 경험을 토대로 2026년부터 2028년까지 3개년에 걸쳐 무균 제제(주사제, 점안제, 안연고제 등)를 대상으로 생물학적 동등성 재평가를 추진할 예정이다.
특히 올해는 용액 주사제를 중심으로 첫 시행에 들어가며, 신경계·기관계 의약품이 대상이다.
식약처는 설명회 현장에서 1차 자료 제출 기한을 3월 말에서 6월 말까지 유예한다고 전했다.
정명훈 사무관은 "시험을 진행 중인 업체의 부담을 고려한 조치"라면서 "단, 6월까지 내 자료를 제출하지 않을 경우 판매업무 정지 등 행정처분이 가능하고 부적합 시 회수 및 판매 중지 조치가 뒤따르는 만큼 일정 준수가 중요하다"고 강조했다.
히올루론산 제제, 수액제 등 수급 불안정 우려 품목 재평가 제외
동시에 식약처는 단순한 일정 유예를 넘어 동등성 입증이 과학적으로 어렵거나 수급 영향이 큰 품목에 대해서는 재평가 대상에서 제외하는 방안도 안내했다.
정명훈 사무관은 "무균 제제의 경우 품목 특성상 수급 불안정 가능성이 상대적으로 높은 품목이 다수 재평가에 포함된 점을 고려했다"며 "올해는 안과 수술용 히알루론산 제제와 일부 대용량 수액제 등 75개 품목을 생동 재평가 제외 대상으로 확정했다"고 말했다.

식약처는 향후 방사성 의약품, 의료용 고압가스, 투석용 제제 등도 재평가 대상에서 제외할 계획이다. 동등성 입증 자체가 기술적으로 어려운 경우 수급 차질 가능성을 사전에 차단하기 위한 조치로 풀이된다.
이에 따라 식약처는 2026년 대상 품목 변경 공고를 통해 용액 주사제 75개 품목을 생동 재평가 제외 대상으로 조정할 예정이다. 다만 2027~2028년 제외 대상 품목은 내년 상반기 중 품목을 공개하고 업계 의견을 추가로 수렴한다는 방침이다.
정명훈 사무관은 "사전 예시 기간 동안 제외 대상에 해당한다고 판단되는 품목은 과학적 근거를 포함한 사유서를 제출해달라"며 "검토를 거쳐 최종 대상 품목을 확정할 계획"이라고 설명했다.
내국소 외용제와 안연고제 등 일부항목 사유서로 대체
일부 재평가 품목의 자료 제출 완화도 병행된다. 식약처는 국소 외용제와 안연고제 등 일부 제형과 관련 약동학적 동등성 시험의 일부 항목을 사유서로 대체할 수 있도록 하는 방안을 검토 중이라고 밝혔다.
정명훈 사무관은 "제제 특성상 시험 자체가 어렵거나 불필요한 경우가 있다"며 "과학적 타당성을 전제로 자료 일부를 대체할 수 있도록 유연하게 운영할 계획"이라고 말했다.
한편 식약처는 대조약 공급 부족 문제를 해소하기 위해 제약협회와 협력해 공급 정보 공유 체계를 구축했으며, 필요 시 업체로부터 직접 의견서를 제출받아 후속 지원 방안도 검토할 예정이다.

