특별기고|
법무법인 태평양 안명수 전문위원
2026 의료기기 정책, 제도, 행정 탈탈 털기

인공지능(AI)과 디지털 혁신 등 기술환경 변화를 따라 의료기기 법·제도가 빠르게 변하고 있다. <히트뉴스>는 2026년 한 해 동안 <법무법인 태평양>과 함께 바이오헬스케어 혁신의 이정표가 될 의료기기 정책·제도와 주요 행정 해석을 짚어본다.
① 연재를 시작하며
② 웰니스 제품, 유헬스케어 의료기기, 디지털의료제품
③ 융복합의료제품, 디지털융합의약품, 조합의료기기, 한벌구성의료기기
디지털 치료제와 체외진단 기반 맞춤의료, 약물 전달 디바이스와 AI 소프트웨어가 결합된 치료 솔루션이 잇따라 등장하며 융복합 의료제품에 대한 관심과 수요가 커지고 있다. 하나의 치료 과정에 의료기기·의약품·체외진단·소프트웨어가 동시에 작동하는 사례가 늘어나면서, 기존의 단일 제품 중심 규제 체계는 새로운 도전에 직면했다.
식품의약품안전처는 2024년 디지털의료제품법 시행을 계기로 규제 패러다임 전환에 나서고 있다. 이에 따라 제품 개발 단계부터 분류 기준과 적용 법령, 허가·관리 방식을 어떻게 판단할 것인지가 기업과 의료기관 모두에게 중요한 이슈로 떠올랐다.
이에 따라 두 개 이상의 의료제품이 결합되거나 하나의 제품으로 함께 포장·사용되는 융복합의료제품을 중심으로, 제품 분류와 관리 방식의 핵심 쟁점을 살펴본다.

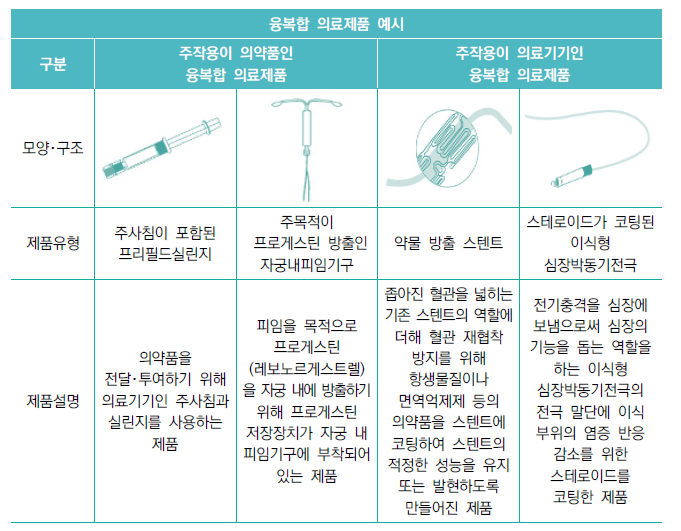
▶ 융복합의료제품 : '약사법' 제2조 제4호와 제7호에 따른 의약품과 의약외품 및 '의료기기법' 제2조 제1항에 따른 의료기기가 물리적, 화학적 또는 그 밖의 방법에 의해 서로 복합적으로 결합된 제품
▶ 디지털융합의약품 : '약사법' 제2조 제4호에 따른 의약품과 디지털의료기기 또는 디지털의료·건강지원기기가 조합된 의약품. 단, 주된 기능이 디지털의료기기에 해당하는 경우는 제외
▶ 조합의료기기(조합체외진단의료기기 포함) : 2가지 이상의 의료기기가 모여 하나의 의료기기가 되는 것으로서 복합적인 기능을 발휘하는 의료기기
▶ 한벌구성의료기기(한벌구성체외진단의료기기 포함) : 2가지 이상의 의료기기를 하나의 포장단위로 구성한 의료기기
전통적으로 의료제품은 질병의 진단·치료·경감·처치 또는 예방 목적으로 사용되기 때문에 제조·수입·판매에 이르는 과정이 엄격하게 관리되며, 품목별로 식약처의 허가·인증을 받거나 신고를 해야 한다.
조합의료기기와 한벌구성의료기기는 두 개 이상의 제품으로 구성되더라도 각각의 제품이 모두 의료기기이기 때문에 의료기기법(또는 체외진단의료기기법)에 따른 의료기기로 품목 허가·인증을 받거나 신고하면 된다.
조합의료기기의 품목명은 주된 기능을 발휘하는 의료기기로 하고, 조합된 각 의료기기의 등급이 다른 경우, 그 의료기기 중 가장 높은 위해도 등급인 하나의 제품으로 품목 허가·인증을 받거나 신고를 해야 한다. GMP 심사는 품목군별로 받아야 하며 각기 다른 품목군의 의료기기로 조합된 경우, 개별 품목군에 대한 GMP심사를 받아야 한다.
한벌구성의료기기는 주된 사용목적 또는 기능을 발휘하는 의료기기의 품목명을 사용하고, 한벌 구성된 의료기기의 등급이 각각 다를 경우 가장 높은 위해도 등급인 하나의 제품으로 품목 허가․인증을 받거나 신고를 하면 된다.
조합의료기기나 한벌구성의료기기를 각각의 의료기기로 분리하려면 각각의 의료기기에 대해 품목 허가·인증을 받거나 신고를 해야 한다.
반면, 융복합의료제품(디지털융합제품 포함) 허가 과정은 다소 복잡하다. 우선 융복합의료제품 해당 여부 및 분류에 대한 판단이 먼저 이뤄져야 한다. 융복합제품은 의약품과 의료기기로 구성되어 있기 때문에 어떤 제품의 허가 방식을 따를 것인지가 매우 중요하기 때문이다.
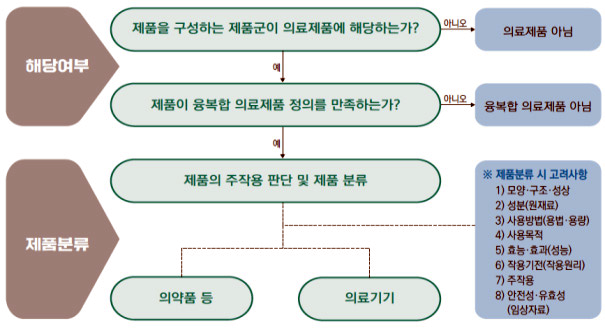
융복합의료제품의 경우, 주작용(primary mode of action)에 따라 해당 제품의 적용 법령과 담당 부서를 정하고 있다. 먼저 융복합의료제품 분류(의약품 또는 의료기기)를 결정해 허가를 신청하면 해당 부서 검토를 거쳐 품목허가가 이루어진다.
융복합의료제품 해당 여부 및 분류에 관한 식약처 검토를 받으려면 ‘융복합 의료제품 해당 여부 검토 신청서’를 작성해 식약처에 제출하면 된다. 신청서에 전자민원시스템(의약품안전나라) 또는 등기우편을 통해 해당 제품의 사용목적, 주작용, 보조작용, 원재료, 사용방법 등을 기술하고, 추가 설명자료를 첨부해 제출하면, 14일 이내에 검토 결과를 회신 받을 수 있다. 융복합의료제품 조정협의회 개최가 필요한 경우에는 안전상정 통지일로부터 60일 이내에 결과를 알 수 있다.
식약처는 2019년 3월 29일부터 융복합의료제품 전담 상담과 지원 업무를 담당하는 창구를 개설․운영해 2023년 12월 기준 654건의 제품 분류 민원을 받았다. 654건 중 융복합의료제품으로 분류된 건은 158건으로 약 24%를 차지했으며, 융복합의료제품에 해당하지 않는다고 판단한 건은 162건으로 약 25% 비중이었다. 이밖에 민원인의 자진취하 148건(23%), 자료 미비로 인한 판단불가 186건(28%)이 있었다.
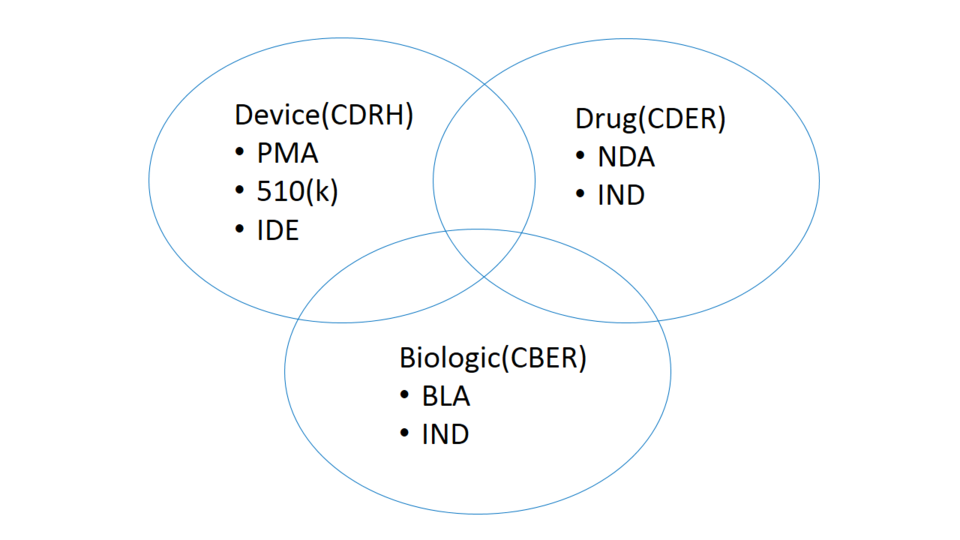
융복합의료제품 분류와 관련해 유명한 미국 판례가 있다.(Bracco Diagnostics, Inc. v. Shalala, 1997 / Prevor v. FDA, 2014) 이 판례를 보면 제조업체가 융복합제품의 분류에 얼마나 많은 관심과 노력을 기울이고 있는지 엿볼 수 있다. 비록 2009년도 자료지만 융복합제품이 의약품으로 분류돼 허가받는 것은 의료기기로 허가받는 것보다 허가 비용이 3500만 달러 더 소요될 수도 있다고 설명하고 있다.(Brougher JT, Dykeman DJ, "Navigating the FDA Process: Patent Strategy for Combination Products", 2009)
조합의료기기나 한벌구성의료기기의 경우 기존의 허가제품을 이용할 수 없다는 점에 유의해야 한다. 또한 융복합의료제품은 주된 작용(primary mode of action)을 면밀히 살펴 제품 개발 및 허가를 진행할 필요가 있다. 융복합의료제품 관련 규정이 법률
도 주목할 부분이다. 디지털의료제품법에 디지털융합의약품 규정은 있으나 디지털융합의료기기에 대한 규정이 없다는 점이 제도 개선이 필요할 것이다.
알아두면 쓸모 있는 식약처 질의·회신
① 제조업자가 두 개의 GMP 품목군이 모인 조합의료기기(2등급)를 제조하는 경우, 각각의 품목군 별로 GMP 적합인정을 받아야 하나요? 아니면 주된 기능을 발휘하는 의료기기 품목군에 대하여 GMP 적합인정을 받아야 하나요? (2017)
"GMP 적합인정은 품목군별로 실시하며, 각기 다른 품목군의 의료기기(2등급)가 조합된 조합의료기기를 제조할 경우, 각각의 품목군에 대해 GMP 적합인정을 받아야 합니다."
②수입의료기기와 국내 타 제조원에서 제조된 의료기기와 자사 제품을 함께 구성하는 경우, 한벌구성의료기기로 인증 가능한가요? (2019 상)
"타사에서 제조·수입허가(인증 또는 신고)를 받아 제조·수입된 의료기기는 허가(인증 또는 신고)된 사항의 제품 그대로 유통(판매)해야 합니다. 해외제조사(또는 국내판매원) 제품을 구매한 후 자사에서 제조한 의료기기와 함께 포장해 한벌구성의료기기로 제조하는 경우라면, 해외제조사(또는 국내제조원)와 일부 공정에 대한 위·수탁계약을 맺고 해당 제조원으로부터 의료기기를 직접 구매해 자사에서 추가공정(포장 및 라벨링 등) 후 완제품 상태의 한벌구성의료기기로 제조해야 합니다."
③ 의료기기 A, B를 한벌구성의료기기(C)로 허가받는 경우, 한벌구성의료기기(C) 허가로 A 또는 B만을 판매할 수 있나요? (2022)
"A와 B를 한벌구성의료기기(C)로 허가(인증·신고) 받은 경우 허가(인증·신고)받은 사항(C)대로 제조·수입·판매해야 합니다."

