성균관대학교 박미혜 교수, "글로벌 의약품-의료기기 평가에 적극 활용"

환자들의 경험과 선호도가 의료제품 개발을 좌우하는 핵심 요소로 등장하면서 신약, 신의료기기 개발 단계부터 환자 참여를 제도화하려는 움직임이 본격화되고 있다. 연구자와 의료진 중심이던 제품 개발 패러다임이 바뀌면서 국내 제도 변화에도 영향을 미칠 것으로 예상된다.
성균관대학교 박미혜 교수는 27일 상성코엑스 더 플라츠홀에서 히트미디어/히트뉴스, 한국바이오의약품협회(KoBIA), 한국보건산업진흥원(K-헬스미래추진단)이 공동주최한 '미정복 질환 정복을 위한 환자 중심 혁신 전략 세미나'에서 '의료제품 개발 및 규제 의사결정에서 환자 참여'를 주제로 발표했다.
박 교수는 "과거 의료제품 개발은 연구개발자와 의료제공자 등이 중심적인 위치를 차지했으나 최근 들어 최종 소비자의 중요성이 부각되면서 환자가 개발 및 규제 의사 결정에 중요한 역할을 하고 있다"며 "환자의 요구와 선호도를 반영해 신약 및 신의료기기 개발 실패율을 낮추고 치료 효과와 만족도를 제고하려는 것"이라고 설명했다.
박 교수에 따르면 글로벌 규제기관도 의약품 및 의료기기 개발에 환자 경험데이터(Patient Experience Data, PED)와 환자 선도호 정보(Patient Preference Information, PPI)를 앞다퉈 반영하고 있다.
FDA·EMA, 환자 선호도·위험 수용도 평가한 승인 사례 나와
ICH, 2026년까지 '환자 중심 개발' 글로벌 가이드라인 제시
미국은 2012년 FDA 안전 및 혁신법(FDASIA, Safety and Innovation Act)을 제정해 환자 중심 의약품 개발(PFDD, Patient Focused Drug Development)을 제도화했다. 2016년 21세기 치유법(21st Century Act), 2017년 FDA 재승인법(FDARA, Reauthorization Act)을 통해 환자 참여의 중요성을 재확인했으며 2020년 6월 환자 중심 의약품 개발 가이드라인을 발표했다.
유럽은 2022년 '환자 참여 프레임워크'를 제시하며 환자 선호도를 의약품 개발에 체계적으로 반영할 수 있는 방법론을 마련했다.
대표적으로 치료 저항성 우울증 치료제 '스프라바토'(SPRAVATO®)는 임상시험 결과와 함께 환자 선호도 정보와 환자 보고 결과를 제출해 FDA 승인을 받았으며, 원형탈모증 치료제 '리트풀로'(Litfulo)는 미국 및 유럽 5개국 환자의 선호도 정보를 평가해 EMA 승인을 받았다.
의료기기 분야도 환자 선호도 자료를 적극 활용하고 있다. 성과가 나타났다. FDA는 2012년과 2016년 환자선호도를 고려한 유익성-위해성 평가지침 등을 제공했으며, 이를 토대로 유효성 기준을 충족하지 못한 체중감량기기에 대한 환자 수용도를 반영해 허가했다.
또한 환자 설문조사를 통해 혈액투석 환자들이 사망률 30% 수준의 위험을 감수하더라도 의료기관보다 가정 내 투석을 선호한다는 사실이 확인됨에 따라 의료기관 내에서만 사용하던 급성 또는 만성신부전증 관리용 혈액투석기의 적응증을 가정용으로 확대한 사례도 있다.
국제의약품규제조화위원회(ICH)는 2020년부터 환자 중심 의료제품 개발을 위한 효능(E) 가이드라인(E22)을 새롭게 마련했다. ICH는 2026년까지 지침 작업을 완료해 환자 선호도 연구(PPS)를 의약품 개발 및 규제 의사결정에 적용하는 방안을 제시할 예정이다.
박 교수는 "현재 환자 선호도 측정 방법으로 이산선택 실험(DCE)을 가장 많이 활용하고 있다"며 "환자들이 가상의 치료 대안 중에서 가장 선호하는 것을 선택하도록 요청해 환자 선호도를 정량화하는 방법"이라고 소개했다.
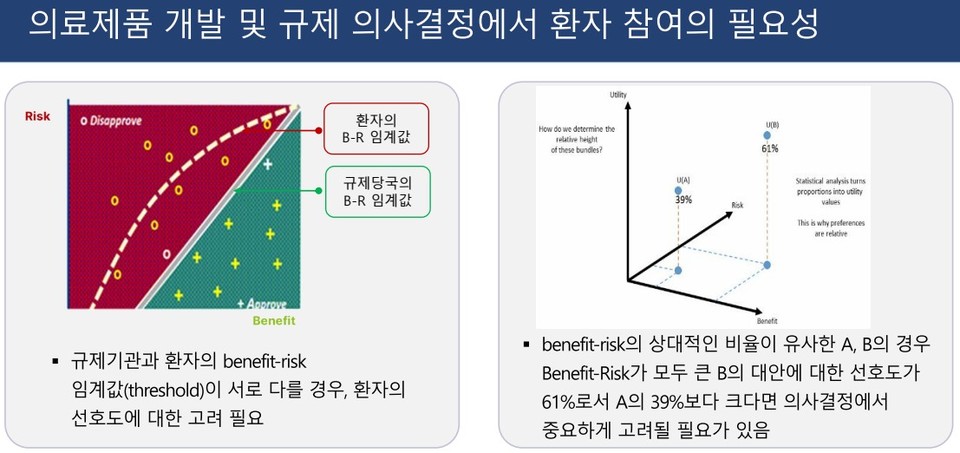
박 교수는 이어 "의료제품의 유익성과 위해성(risk-benefit)에 대한 규제기관과 환자의 임계값(threshold)가 다른 경우 환자 선호도를 고려할 필요가 있다"며 "명백한 치료대안이 존재하지 않을 때, 치료 방법에 대한 근거가 불확실하거나 가변적일 때, 환자들의 견해가 하위 집단 또는 규제기관과 다를 때 유용한 의사결정 근거로 활용할 수 있다"고 설명했다.

