美 리듬파마슈티컬스에 희귀비만증 후보물질 L/O… 선급금 1300억
지난해 1월 아베오 인수 마무리… '항암신약' 글로벌 제약사 도약
지난달 통풍 치료제 '티굴릭소스타트' 유럽 임상 3상 조건부 승인
최근 LG화학이 미국 리듬파마슈티컬스(Rhythm Pharmaceuticals)에 희귀비만증 신약 후보물질에 대한 기술수출(L/O) 계약을 체결한 가운데, 항암 신약 및 통풍 치료제 개발에도 박차를 가할 전망이다.
LG화학은 지난 5일 미국 리듬파마슈티컬스와 희귀비만증 신약 'LB54640(개발코드명)'의 글로벌 개발 및 판매 권리를 이전하는 기술수출 계약을 체결했다고 밝혔다. 총 계약 규모는 3억500만달러(약 4000억원)다. LG화학은 선급금(Upfront)으로 1억달러(약 1300억원)를, 향후 개발 및 상업화 단계별 마일스톤(Milestone)으로 최대 2억500만달러(약 2700억원)를 수령한다. 이와 함께 리듬파마슈티컬스의 연매출에 따른 로열티도 매년 별도로 받는다.
LB54640은 경구제형 MC4R 작용제로, 임상 1상 결과 용량의존적 체중 감소 경향성과 안전성이 확인됐다. 이를 바탕으로 지난해 10월 희귀비만증 환자 대상으로 미국 임상 2상에 돌입했다. 향후 리듬파마슈티컬스는 이를 이관받아 시험자 모집을 본격화할 계획이다.
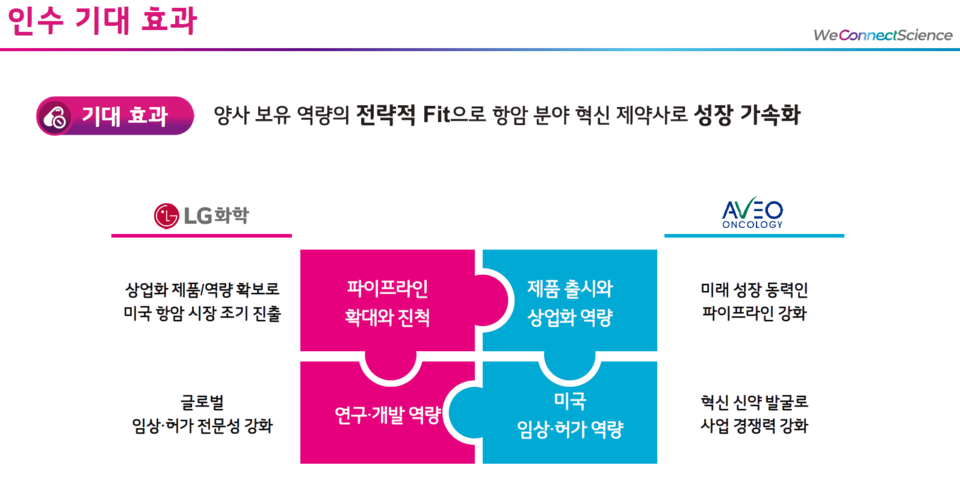
LG화학은 희귀비만증을 비롯한 대사질환 파이프라인(신약 후보물질)뿐만 아니라 항암신약 파이프라인 개발에도 집중하고 있다. 앞서 회사는 2022년 10월 미국 항암제 개발기업 아베오파마슈티컬스(AVEO Pharmaceuticalsㆍ이하 아베오)를 인수한다고 밝혔다. 5억6600만달러(약 8000억원)에 아베오 지분 100%를 인수하는 내용이다.
당시 신학철 LG화학 대표는 보도자료를 통해 "미국 상업화 역량의 지속적인 강화를 통해 현지 매출 확대에 적극 나서는 한편, 항암 중심의 미국 임상 및 허가 역량을 한층 높여 글로벌 혁신 제약사 도약에 속도를 낼 것"이라고 밝힌 바 있다.
LG화학은 2023년 1월 아베오 인수합병(M&A)을 마무리 지었다. 합병 이후 아베오는 LG화학의 종속회사로 편입됐는데, 기존처럼 독립적인 경영 체제로 운영된다. 아베오는 2002년 미국 매사추세츠주 보스턴에서 설립된 임상 개발ㆍ허가ㆍ영업ㆍ마케팅 등 항암 시장에 특화된 기업이다. 2010년 나스닥에 상장했고, 2021년 신장암을 표적으로 하는 치료제 '포티브다(FOTIVDA)'가 미국 식품의약국(FDA)으로부터 허가를 받은 후 매분기 매출 성장세를 이어가고 있다는 게 회사 측 설명이다.
아베오를 품은 LG화학은 현재 임상 1상 단계의 △LR19129 △LR19127 △LR19125 △LR20011 파이프라인 개발에 나서고 있다. 이 중 LR20011(화합물명 GEN-001)은 진행성 고형암을 타깃으로 하는 경구용 마이크로바이옴 치료제다. LG화학은 2020년 4월 지놈앤컴퍼니와 GEN-001에 대한 라이선스 계약을 체결했다. 이 계약에 따라 LG화학은 GEN-001에 대한 한국 및 기타 동아시아 권역에서 옵션권리 실행에 따라 독점적 임상시험, 허가 및 상업화 권리를 갖게 됐다.
LG화학 관계자는 히트뉴스와의 통화에서 "회사에서 가장 초점을 맞추고 있는 분야는 '항암'이다. 항암신약 중심의 글로벌 제약사로 도약하는 것을 목표로 하고 있다. 향후 유망 항암신약 후보물질에 대한 투자를 집중할 계획"이라며 "비만을 비롯한 대사질환 분야에도 계속 투자를 진행할 예정"이라고 말했다.

LG화학은 지난달 이탈리아 의약품기관(AIFA)으로부터 통풍 치료제 '티굴릭소스타트(Tigulixostat)'의 3상 임상시험계획(IND)의 조건부 승인을 받았다고 공시했다. 티굴릭소스타트는 요산 생성 효소 잔틴 옥시다제(Xanthine OxidaseㆍXO)의 발현을 억제하는 작용기전을 가졌다.
회사에 따르면 이번 임상 3상은 고요산혈증 통풍 환자들을 대상으로 실시되며, 대조군인 '알로퓨리놀(Allopurinol)' 대비 혈중 요산 강하 유효성, 통풍 발작 발현율, 통풍 결절 감소 및 안전성이 평가될 예정이다. 임상 대상자 수는 약 2600명으로 설정됐다.
앞선 관계자는 "요청 자료 제출 및 규제기관 검토가 마무리된 후 유럽에서도 시험자 모집을 본격화할 계획이다. 1분기 내 변경 승인이 될 것으로 전망하고 있다"며 "유렐리아(EURELIAㆍ임상시험명)1, 2 모두 원래 계획대로 시험자 모집이 원활히 이뤄지고 있다"고 설명했다.
그러면서 "유렐리아1은 미국, 필리핀 등 4개 국가에서 진행되고 있다"며 "유렐리아2는 미국, 아시아, 중남미, 오세아니아 등 10여개 국가에서 진행되고 있다. 유렐리아2 유럽 임상이 본격화되면 20여개국으로 임상이 확장될 것"이라고 덧붙였다.

