이아날루맙, 루프스신염·쇼그렌 증후군 이어 면역 혈소판감소증 3상 승인
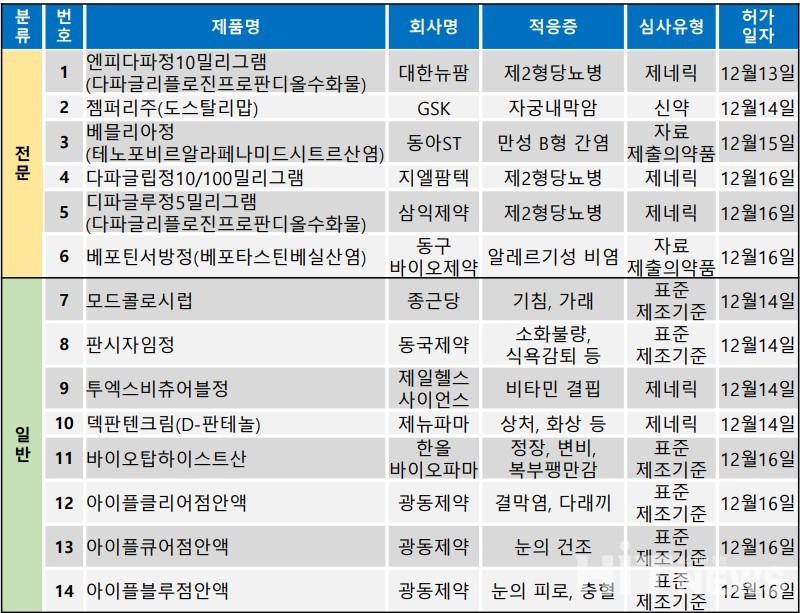
지난 주(12월 12일~12월 18일)에는 총 14개 품목이 식품의약품안전처로부터 품목허가를 받았다. 이 중 전문의약품은 6건, 일반의약품은 8건이었다.
이번 허가 전문의약품들은 제2형당뇨병이 주를 이뤘으며, 자궁내막암, B형 간염, 알레르기성 비염 치료제 등의 적응증으로 대상으로 하는 의약품들이었다.
GSK는 지난 14일 자궁내막암 환자를 대상으로 한 PD-1 단클론항체 ‘젬퍼리주(성분명 : 도스탈리맙)’의 품목허가를 획득했다.
젬퍼리는 T세포의 면역관문 수용체인 PD-1(세포 예정사 1)을 표적으로 하는 단클론항체로, PD-1은 CD28 계열에 속하는 억제성 면역관문 수용체로 활성화된 T세포, B세포, NK세포, 골수 계통 세포에서 발현돼 면역조절에서 중추적인 역할을 한다.
이 약은 면역세포 표면에 발현된 PD-1을 이용, 면역세포의 공격을 회피하는 암세포 생존 기전을 차단해 면역세포가 암세포를 제거할 수 있도록 돕는다.
식약처는 이 약을 '이전 백금기반 전신 화학요법의 치료 중이거나 치료 후 진행을 나타낸 재발성 또는 진행성 불일치 복구결함 (mismatch repair deficient, dMMR)/고빈도 현미부수체 불안정 (microsatellite instability-high, MSI-H) 자궁내막암이 있는 성인 환자의 치료'를 대상으로 허가했다.
젬퍼리의 허가로 국내 PD-1 단클론항체 치료제는 BMS 옵디보(성분명 : 니볼루맙), MSD 키트루다(성분명 : 펨브롤리주맙)에 이어 3개가 됐다. 옵디보와 키트루다는 최초 흑색종 환자를 대상으로 허가된 후 적응증을 확대하고 있는 반면, 젬퍼리는 자궁내막암을 최초 허가 적응증으로 삼았다.
한편, 이번 허가 전문의약품 중 절반을 제2형당뇨병 치료제가 차지했다. 이 약들은 모두 SGLT-2 저해제 계열 다파글리플로진 성분이 포함된 제네릭이다.
대한뉴팜 엔피다피정, 삼익제약 디파글루정은 다파글리플로진 단일제며, 지엘팜텍 다파글립정은 DPP-4 계열 성분 시타글립틴과의 복합제다.
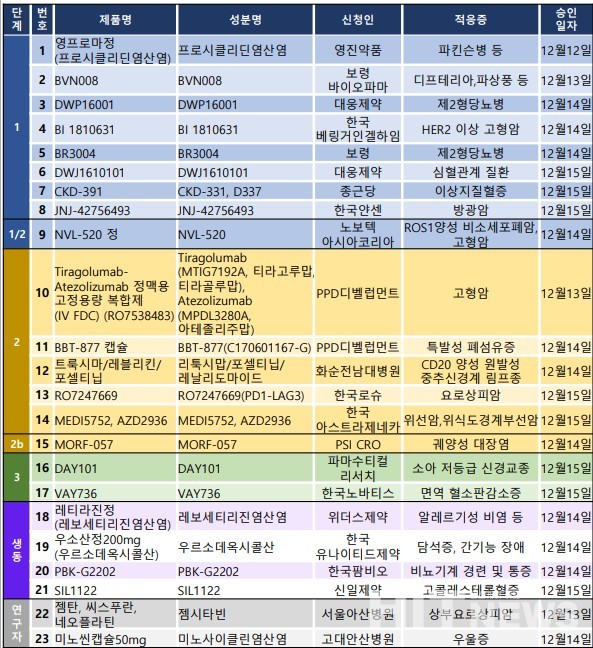
지난주 임상시험계획은 총 23건이 승인 완료됐다. 세부적으로 △1상 8건 △1/2상 1건 △2상 5건 △2b상 1건 △3상 2건 △생물학적동등성 4건 △연구자임상 2건 등이다.
이 임상시험들은 제2형당뇨병, 파킨슨병, 고형암, 방광암, 면역 혈소판감소증 등 다양한 적응증에 대해 승인됐다.
한국노바티스가 개발 중인 면역 혈소판감소증 치료 약물 '이아날루맙(성분명 : VAY736)'의 임상 3상 시험계획이 지난 15일 승인됐다.
이번에 시행되는 시험은 '1차 스테로이드 치료 후 불충분한 반응을 보이거나 재발한 원발성 면역 혈소판감소증 (ITP) 환자에서 엘트롬보팍과 병용하는 이아날루맙 대 위약의 제3상 무작위 배정, 이중 눈가림 임상시험(연구명 : VAYHIT2)'이다.
이번 임상은 삼성서울병원과 화순전남대학교병원에서 진행될 예정이며, 8명의 국내 환자(글로벌 150명)를 대상으로 한다.
회사는 이 약물을 다양한 적응증을 대상으로 2018년부터 진행해왔다.
2018년 10월 전신 홍반성 루프스(SLE)를 시작으로, 2021년 8월 비호지킨 림프종(NHL), 지난 2월 활동성 루프스 신염, 지난 9월 활성 쇼그렌 증후군을 대상으로 한 임상을 승인받은 바 있다.

