SK케미칼, 리루졸 성분 루게릭병 치료제 중 정제 외 제형 최초 허가
다이이찌산쿄, 비소세포폐암 대상 '파트리투맙' 임상 3상 IND 승인


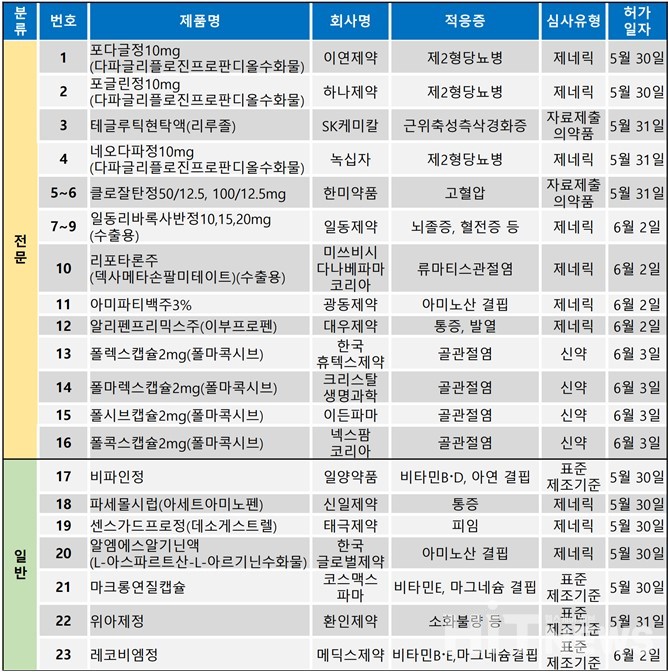
지난 주(5월 28일~6월 3일)에는 총 23개 품목이 식품의약품안전처로부터 품목허가를 받았다. 이 중 전문의약품은 16건, 일반의약품은 7건이었다.
이번 허가 전문의약품들은 제2형당뇨병, 근위축성측삭경화증(amyotrophic lateral sclerosis, ALS), 뇌졸중, 고혈압 등 적응증이 주를 이뤘다.
SK케미칼은 지난 5월 31일 근위축성측삭경화증 치료제인 '테글루틱현탁액(성분명 리루졸)'의 품목허가를 획득했다. 이 의약품은 기존에 존재하던 리루졸 성분 치료제를 현탁액으로 제형변경한 자료제출의약품이다.
근위축성측삭경화증은 '루게릭병'이라고도 불리며, 서울대학교병원 측에 따르면 발병 원인은 아직 밝혀져 있지 않지만 지금까지 유전자 돌연변이로 인한 '가족성 루게릭병'과 비유전성 '산발성 루게릭병', 특수 바이러스에 의한 발병 등 여러 가지 요인들이 원인으로 제기되고 있다.
이 질환자는 서서히 사지의 위약 및 위축이 진행되고, 결국 호흡근 마비로 수년 내에 사명에 이르게 된다.
'테글루틱현탁액'을 제외하고 리루졸 성분 제제는 사노피-아벤티스코리아의 리루텍정, 유영제약의 유리텍정 등 현재 국내에 '정제' 제형만 허가된 상태다.
이번 현탁액 제형 출시로 기존 정제의 '삼킴곤란' 문제를 겪던 환자들에게 복약편의성을 개선할 수 있을 것으로 판단된다.
식약처는 리루절 성분 제제를 '근위축성측삭경화증 환자의 생존기간을 연장시키거나 기관절개시점을 늦추어 준다'는 효능·효과로 사용을 허가 했다.
현재까지 국내 허가된 ALS 치료제들은 생존 기간을 수개월 정도 연장시키는 효과를 가질 뿐 직접적인 근력회복, 삶의질 개선 등 임상적 치료 효과를 입증한 의약품은 아직 없는 상태다.
한편, 미국 FDA는 해당 현탁액 제제를 2018년 9월 경 희귀의약품 지정 및 신속심사를 통해 품목허가한 바 있다.
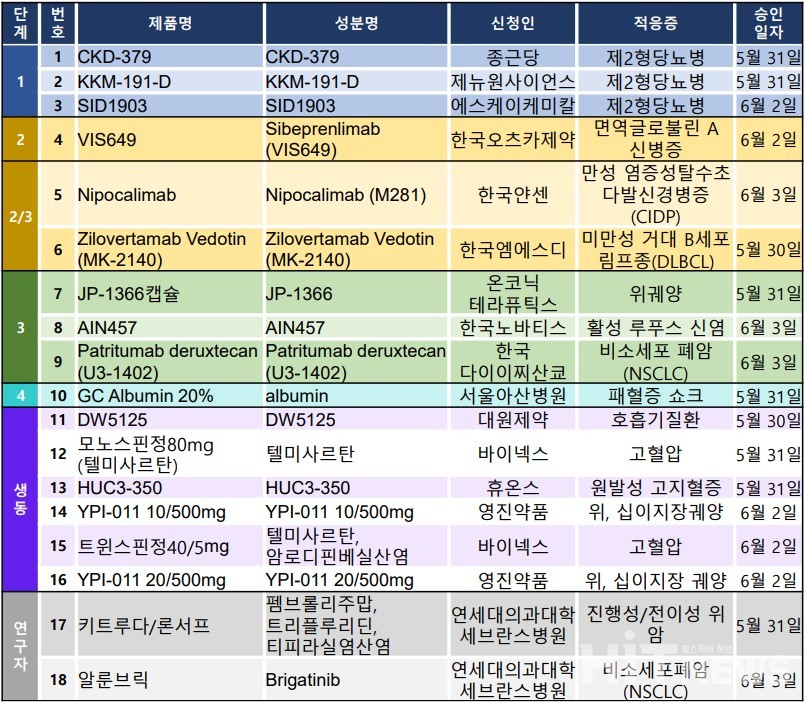
지난주 임상시험계획은 총 18건이 승인 완료됐다. 세부적으로 △임상1상 3건 △2상 1건 △2/3상 2건 △3상 3건 △4상 1건 △생물학적동등성 6건 △연구자임상 2건 등이다.
해당 임상시험은 제2형당뇨병, 면역글로불린 A 신병증, 비소세포폐암, 위·십이지장 궤양, 고혈압 등 다양한 적응증에 대해 승인됐다.
한국다이이찌산쿄는 HER3 표적 항체약물접합체(ADC)로 개발하고 있는 ‘파트리투맙(Partritumab deruxtecan)의 국내 임상3상 시험계획을 식약처로부터 승인받았다.
이번 임상시험은 '표피 성장 인자 수용체(EGFR) 티로신 키나아제 억제제(TKI) 요법 실패 후 전이성 또는 국소 진행성 표피 성장 인자 수용체-돌연변이(EGFRm) 비소세포 폐암 환자'를 대상으로 진행된다.
ADC는 항체와 약물을 결합시켜 암세포를 선택적으로 표적해 제거하는 치료제다. 특정 암세포를 인식해 작용하기 때문에 최소 투여량으로 약물의 효과를 극대화할 수 있다.
회사는 유방암과 비소세포폐암을 타겟으로 파트리투맙을 개발 중이며, 미국임상종양학회 연례학술대회인 ASCO를 통해 임상1·2상 결과 및 임상적 결과를 발표했으며, 지난해 12월 24일 미국 FDA로부터의 '혁신 치료제 지정(Breakthrough Therapy Designation, BTD)' 소식을 밝힌 바 있다.
또한 회사는 현재 ADC 개발에 집중하고 있는 것으로 확인되며, 주요 제품은 HER2 표적 ADC '엔허투(Enhertu, trastuzumab deruxtecan)', Trop2 표적 ADC '다토(Dato-DXd, datopotamab deruxtecan)', HER3 표적 ADC '파트리투맙(patritumab deruxtecan)' 등 3가지다.
한편, 국내에서 ADC 치료제를 주요 파이프라인으로 개발하고 있는 회사는 △레고캠바이오 △인투셀 △알테오젠 △지놈앤컴퍼니 △에이비엘바이오 △앱티스 △온코젠 △피노바이오 등이 있다.

