MSD '윈레브에어', 얀센 '옵신비' 폐동맥고혈압 치료제로 허가
비카드로스타트+자디앙 병용, 만성신장병ㆍ심부전 대상 연구 진행 중

지난주(7월21~25일) 총 49개 품목이 식품의약품안전처에서 품목허가를 받았다. 전문의약품 38개, 일반의약품 11개 품목이다. 이들은 고혈압, 제2형당뇨병, 파킨슨증, 뇌전증, 궤양성 대장염, 원발성 담즙성 담관염 등 적응증으로 허가됐다.
새로운 작용 기전의 성분, 새로운 조합의 폐동맥 고혈압 치료제가 줄지어 등장했다.
폐동맥고혈압은 폐소동맥의 벽이 비정상적으로 두꺼워지고 협착되어 압력이 상승하는 희귀·중증 난치질환이다. 증상이 진행되면 호흡곤란, 흉통, 실신 등이 나타날 수 있으며, 돌연사 위험도 높아진다.
한국MSD는 지난 23일 '윈레브에어주(성분 소타터셉트)', '윈레브에어키트주(성분 소타터셉트)'를 허가받았다. 원리브에어는 작년 식약처 '글로벌 혁신제품 신속심사(Global Innovative products on Fast Track, GIFT)' 24호 약제로 지정된 바 있다.
윈레브에어는 다른 폐동맥고혈압 치료와 병용해 WHO 기능분류(FC) II-III 단계에 해당하는 성인 폐동맥고혈압(WHO Group I) 치료를 통한 운동 능력 개선을 목적으로 사용할 수 있다. 허가 용량은 45mg, 60mg 두 종류이며, 3주의 투약 주기를 가진다.
윈레브에어는 '액티빈 신호전달 억제제(Activin Signaling Inhibitor, ASI)'로 구성된 새로운 기전의 치료제(First-in-Class)이다. 폐동맥 혈관 내 세포 증식을 유발하는 단백질 복합체 '액티빈'의 과도한 증식 신호를 차단하고, 세포 성장을 억제하는 항증식 신호와의 균형을 조정해 변형된 혈관 구조를 다시 정상화하는 역재형성(reverse remodeling)을 유도한다.
허가 임상인 'STELLAR' 연구에 따르면, 윈레브에어는 24주 시점에 위약 대비 6분 보행 거리(Hodges–Lehmann 추정치)를 40.8m 증가시켰으며(95% CI : 27.5-54.1, P<0.001), 임상적 악화 또는 사망 위험을 84% 감소시켰다(HR 0.16, 95% CI : 0.08-0.35). 또, WHO-FC, 폐혈관 저항(PVR) 및 심부전 바이오마커인 NT-proBNP 수치 등 2차 유효성 평가 지수 8개 지표에서 위약 대비 유의미한 개선을 확인했다.
현재 회사는 제2차 허가-평가-협상 병행 시범사업에 윈레브에어가 선정돼 급여 등재를 위한 절차도 진행 중인 것으로 나타났다.
한편, 한국얀센은 지난 24일 마시텐탄 성분과 타다라필 성분의 복합제 ‘옵신비정’을 허가받았다. 회사는 마시텐탄 오리지널 제제인 '옵서미트'에 더해 복합제까지 제품 포트폴리오를 넓히게 됐다.
마시텐탄은 엔도텔린 수용체 길항제(ERA)로, WHO FC II-III 폐동맥 고혈압 환자에게 사용되어온 치료제다. PDE-5 억제제인 타다라필은 국내에서는 발기부전 치료제로만 사용돼 왔지만, 옵신비정의 허가로 처음으로 폐동맥 고혈압 적응증을 획득하게 됐다.
레브에어가 기존 치료제들과 병용 투여하도록 허가됨에 따라 향후 옵신비 또는 옵서미트와 처방 시너지도 기대할 수 있을 것으로 전망된다.
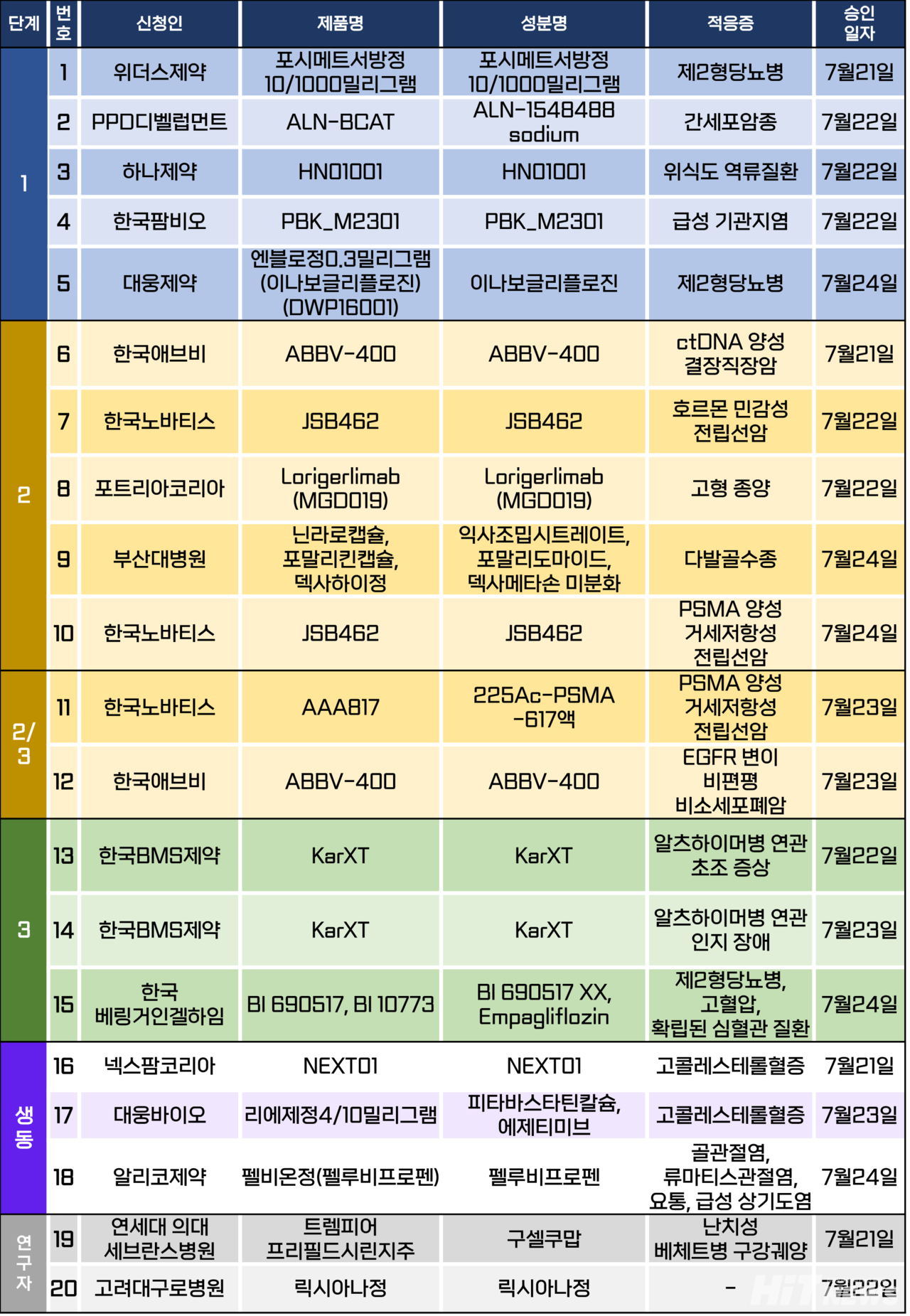
임상시험계획은 총 20건이 승인됐다. 세부적으로 △1상 5건 △2상 6건 △2/3상 2건 △3상 3건 △생물학적 동등성 3건 △연구자 임상 2건 등이다. 이 임상시험들은 제2형당뇨병, 위식도 역류질환, 고혈압 등 질환과 간세포암, 결장직장암, 전립선암, 다발골수종, 비소세포폐암 등 암종을 대상으로 승인됐다.
베링거인겔하임이 개발 중인 선택적 알도스테론 합성효소 억제제 신약물질 '비카드로스타트(VICADROSTATㆍBI 690517)'와 SGLT-2 억제제 '자디앙(성분 엠파글리플로진)' 병용요법의 3상 임상시험이 제2형당뇨병, 고혈압 환자를 대상으로 시작된다.
한국베링거인겔하임은 제 2 형 당뇨병, 고혈압 및 확립된 심혈관 질환 환자를 대상으로 비카드로스타트+자디앙 병용요법의 유효성 및 안전성을 평가하기 위한 이중 눈가림, 무작위배정, 평행군 우월성을 확인하기 위한 3상 임상시험계획을 지난 24일 승인받았다.
알도스테론은 신장에서 전해질과 수분 균형을 조절하는 호르몬으로, 체내 과다 존재할 경우 신장을 손상시켜 만성 신장병을 유발하거나, 혈압을 상승시킬 수 있다. 비카드로스타트는 바로 이 알도스테론 합성을 억제하는 기전을 가진다.
이번 임상은 오는 2030년 4월까지 190명(글로벌 11800명) 참여를 목표로 △서울대병원 △세브란스병원 △인제대 부산백병원 △서울아산병원 △강북삼성병원 △아주대병원 △충남대병원 △연세대 원주세브란스기독병원 △전남대병원 △부산대병원 △인하대 의대부속병원 △가톨릭대 부천성모병원 △가톨릭대 서울성모병원 △대전을지대병원 △고려대 의대부속안산병원 △고려대 의대부속병원 △분당서울대병원 등 의료기관에서 진행될 예정이다.
연구진은 이번 연구의 1차 유효성평가변수를 심혈관(CV) 사망 또는 심부전 사건(HFE)의 최초 사례까지의 시간으로 설정했다. 여기서 HFE는 심부전으로 인한 입원(HHF) 또는 긴급한 심부전(HF)으로 인한 의료기관 방문을 뜻한다.
한편, 한국베링거인겔하임은 현재 비카드로스타트+자디앙 병용요법을 심장·신장·대사(CRM) 질환 분야에 사용할 수 있도록 개발을 추진하고 있다. 지난 2월에는 해당 요법을 만성 신장병 환자를 대상으로 3상 임상시험계획을 승인받고, 연구를 진행 중이며, 더불어 심부전 환자를 대상으로 한 글로벌 3상 임상도 진행 중에 있다.
자디앙의 물질특허가 오는 10월 23일로 다가오면서, 엠파글리플로진 성분의 제네릭의 허가가 줄지어 이어지고 있다. 향후 비카드로스타트와 병용요법 허가 후 만성질환 전반으로의 시장 확대와 더불어 제네릭 등장으로 인한 점유율 하락을 방어할 수 있을지 주목된다.

