심평원 제3회 약제급여평가위원회 심의
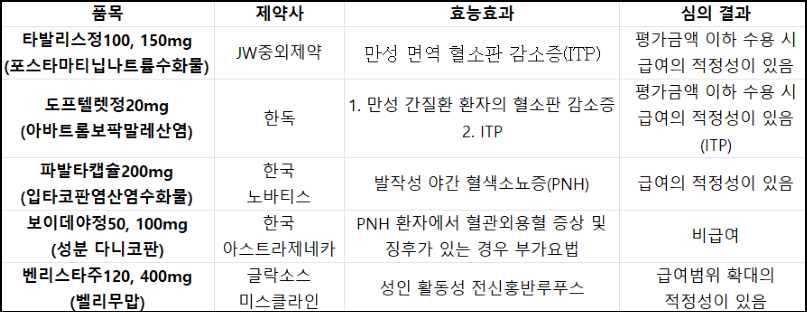
타발리스·도프텔렛 평가금액 이하 수용 시 통과

한국노바티스의 발작성 야간 혈색소뇨증(PNH) 치료제 '파발타캡슐200㎎(성분 입타코판염산염수화물)'이 급여 적정성을 인정 받았다.
건강보험심사평가원은 6일 제3회 약제급여평가위원회의 심의 결과를 공개했다.
PNH는 파괴된 적혈구가 혈액으로 흘러 헤모글로빈이 유출되는 용혈현상으로 인해 발현되는 희귀질환이다. 혈전증, 신부전, 골수부전 등이 주요 증상으로 나타나며 용혈 조절이 치료 핵심이다.
파발타는 혈관 내 용혈(IVH)과 혈관 외 용혈(EVH)을 모두 조절할 수 있고, 경구제형으로 환자의 편의성 및 복용 순응도를 높였다는 평가를 받는다. 이 평가를 바탕으로 이번 약평위를 통과했고, 국민건강보험공단과 약가협상을 앞두게 됐다.
반면, 또다른 PNH 치료제인 한국아스트라제네카의 '보이데야정50·100㎎(성분 다니코판)'은 비급여 판정을 받았다. 'PNH 환자에서 EVH 증상이나 징후가 있는 경우 부가요법'에서다.
보이데야는 지난해 6월 PNH 환자의 보조치료제로 식품의약품안전처의 품목 허가를 획득했으며, 최초의 경구용 D인자 저해제로 알려졌다. 기존 C5 억제제를 투여 중인 PNH 환자에서 EVH 증상이나 징후가 있는 경우 부가요법으로 사용할 수 있다.
'울토미리스(성분 라불리주맙)'와 '솔리리스(성분 에쿨리주맙)' 등의 PNH 치료제를 보유하며 시장을 선점한다는 평가를 받는 아스트라제네카가 보이데야의 급여 도전으로 보조치료에서도 자리매김할 것으로 예상된다.
IPT 치료제는 JW중외제약의 만성 면역 혈소판 감소증(ITP) 치료제 '타발리스정100·150㎎(성분 포스타마티닙 나트륨수화물)'과 한독의 '도프텔렛정20㎎(성분 아바트롬보팍말레산염)'이 약평위를 통과했다.
두 약제 모두 평가금액 이하 수용 시 조건을 달았다. 여기에 도프텔렛은 동시에 신청한 '만성 간질환(CLD) 환자의 혈소판 감소증'에서는 급여 적정성을 인정받지 못했다.
글락소스미스클라인의 성인 활동성 전신홍반루푸스 치료제 '벤리스타주120·400㎎(성분 벨리무맙)'는 위험분담계약(RSA) 사용범위 확대에 성공했다.