셀트리온, 스텔라라 바이오시밀러 '스테키마' 허가
디바라십, 소토라십·아다그라십과 유효성 및 안전성 비교 임상
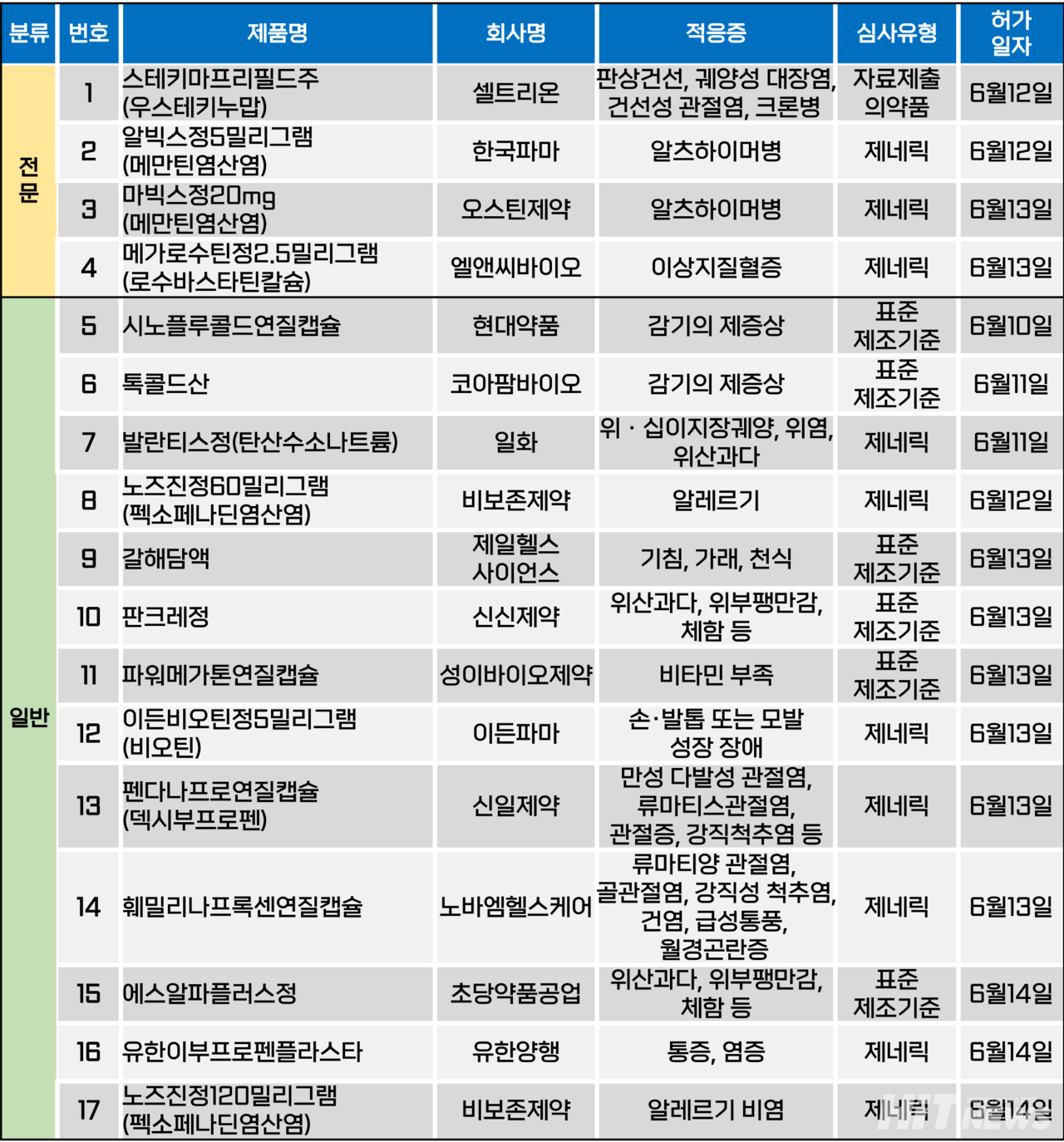
지난주(6월 10~14일) 총 17개 품목이 식품의약품안전처로부터 품목허가를 받았다. 전문의약품은 4개 품목, 일반의약품은 13개 품목이다. 이들은 판상 건선, 궤양성 대장염, 알츠하이머병, 이상지질혈증 등 다양한 적응증으로 허가됐다.
셀트리온이 인터루킨 억제제 스텔라라(성분 우스테키누맙)의 바이오시밀러 '스테키마(개발명 CT-P43)'를 지난 13일 허가받아 자가면역질환 치료제 포트폴리오를 확대했다.
회사는 작년 6월 스테키마의 품목허가를 식약처에 신청했다. 이후 약 1년 이 지난 시점 판상 건선, 건선형 관절염, 크론병, 궤양성 대장염 등 스텔라라가 보유한 모든 적응증을 획득하게 됐다.
우스테키누맙은 사이토카인(cytokine)의 일종인 IL-12(인터루킨-12)와 IL-23(인터루킨-23)에 작용하는 항체치료제로, 체내의 과도한 면역반응을 억제한다.
셀트리온은 현재 자가면역질환 치료제 시장에서 종양괴사인자 알파(TNF-α) 억제제인 인플릭시맙(제품명 램시마·램시마SC)과 아달리무맙(제품명 유플라이마)을 주성분으로 하는 3개 제품을 공급하고 있다. 향후 회사가 류마티스 관절염치료제 악템라(성분명 토실리주맙) 바이오시밀러 'CT-P47' 허가까지 획득하면 TNF-α 억제제와 인터루킨 억제제 등을 아우르는 자가면역질환 포트폴리오를 구축하게 된다.
회사 측은 이번 스테키마 허가를 시작으로 미국, 유럽 등 글로벌 주요국에서도 허가를 획득해 본격적인 글로벌 시장 공략에 나선다는 방침이다. 의약품 시장조사 기관인 아이큐비아(IQVIA)에 따르면, 지난해 글로벌 우스테키누맙 시장 규모는 203억2300만달러 규모였다.
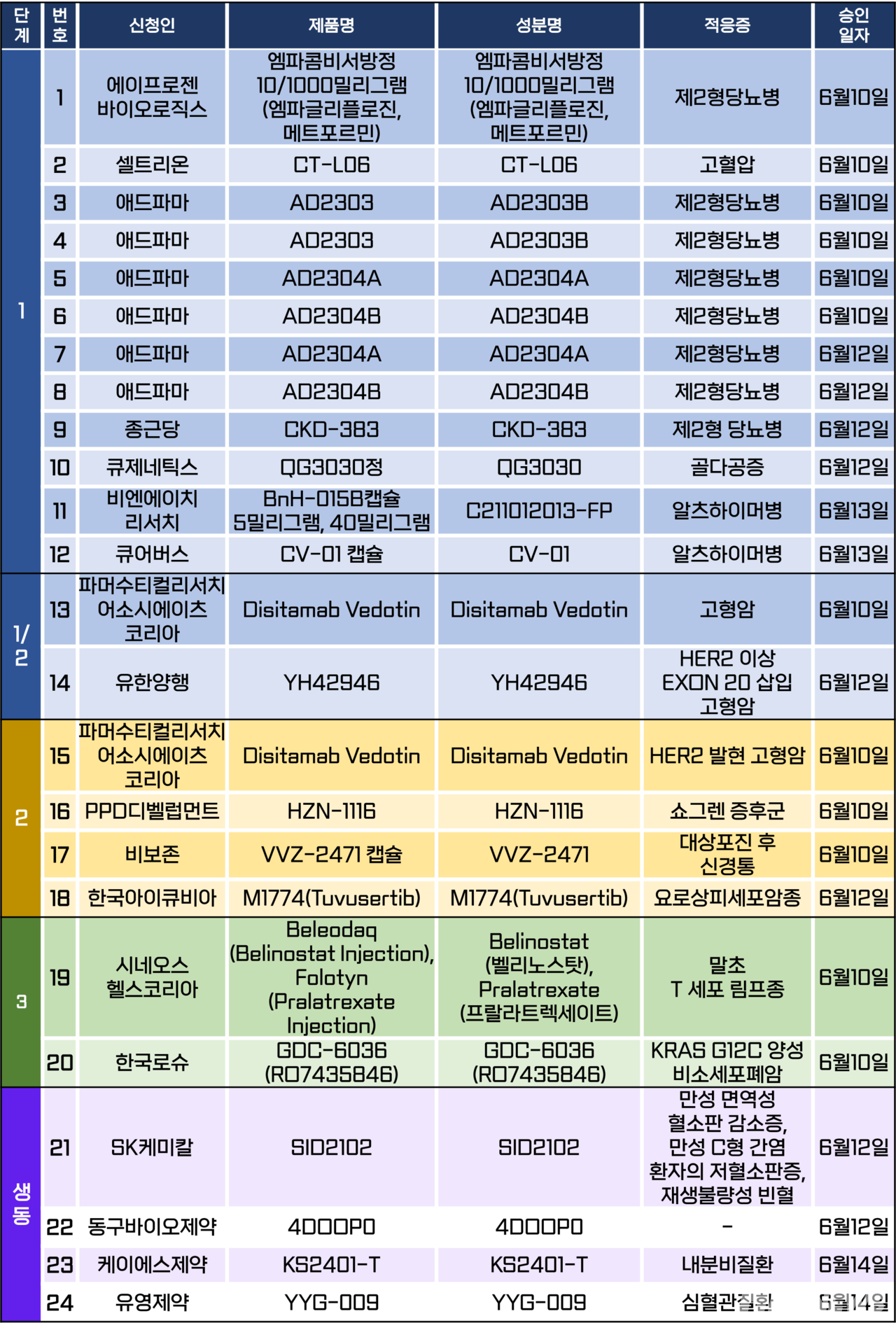
임상시험계획은 총 24건이 승인됐다. 세부적으로 △1상 12건 △1/2상 2건 △2상 4건 △3상 2건 △생물학적 동등성 4건 등이다. 이 임상시험들은 제2형당뇨병, 고혈압, 골다공증, 알츠하이머병, 쇼그렌 증후군 등 질환과 요로상피세포암종, KRAS G12C 양성 비소세포폐암, 말초 T세포 림프종 등 암종을 대상으로 승인됐다.
로슈와 제넨텍이 개발 중인 KRAS G12C 돌연변이 타깃 표적치료제 ‘디바라십(Divarasib)’의 비소세포폐암 2차 치료 대상 3상 임상시험계획이 지난 10일 승인됐다.
디바라십은 KRAS G12C 돌연변이 단백질에 비가역적으로 결합하는 공유결합 억제제(covalent inhibitor)다. KRAS는 비소세포폐암, 췌장암, 비뇨생식기암, 대장암 등 고형암의 약 25% 이상에서 발생하는 빈번한 돌연변이 종양 유전자(oncogene)로 알려져 있다.
이번 3상 임상은 '이전 치료 경험이 있는 KRAS G12C 양성 진행성 또는 전이성 비소세포폐암 환자'를 대상으로 디바라십의 유효성과 안전성을 소토라십(제품명 루마크라스) 또는 아다그라십(제품명 크라자티)과 비교 평가하는 무작위배정, 공개, 다기관 연구다.
임상은 30명(글로벌 320명)의 환자 참여를 목표로 오는 2029년 9월까지 △길 병원 △ 고려대 의대부속병원 △계명대동산병원 △양산부산대병원 △가톨릭대 성빈센트병원 △화순전남대병원 △칠곡경북대병원 △부산대병원 △고려대 의대 부속 구로병원 △충북대병원 △분당서울대병원 △서울대병원 △삼성서울병원 △부산대병원 등 의료기관에서 진행될 예정이다.
연구진은 임상의 일차유효성평가변수를 무진행생존기간(PFS)으로 설정했으며, 이차유효성평가변수를 △전체생존기간(OS) △객관적 반응(ORR) △반응기간(DOR) △이상사례 발생률 및 중증도 등으로 설정했다.
한편, 현재 국내에서 KRAS G12C 변이 타깃 비소세포폐암 치료제로 사용되고 있는 제품은 암젠이 개발한 루마크라스가 유일하다. 회사는 2022년 7월 출시 간담회를 열고, KRAS 종양세포 유전자가 발견된 지 약 40여년 만에 등장한 계열 최초의 신약(First-in-class)으로 루마크라스를 소개한 바 있다.
루마크라스는 현재 KRAS G12C 변이 국소 진행성 또는 전이성 비소세포폐암 2차 치료제로 허가돼 있다. 이 약은 허가 당시 희귀의약품으로 심사를 받았기 때문에 반응률 및 반응기간에 근거해 유효성이 입증됐지만, 아직 생존기간의 개선 입증 자료는 제출되지 않은 것으로 나타났다.

